Ацетат серебра в уксусной кислоте является ценным реагентом для замещения атомов хлора или брома в алкилгалогени-дах без какого-либо элиминирования галогеноводорода, поскольку в этом случае ионы галогена удаляются сольволити-чески и немедленно улавливаются в виде нерастворимых солей серебра. Уинстейн и Баклер [9] показали, что этой реакцией можно управлять по желанию, получая из транс — l, 2-диброми-дов или цис -, или гранс-продукты. Если транс — l, 2-дибромцик-логексан обработать ацетатом серебра в безводной уксусной кислоте или уксусном ангидриде, то конечным продуктом является гране — 1, 2-диацетоксициклогексан, однако если использовать в качестве растворителя влажную уксусную кислоту, то образуется цыс-1 — окси-2 — ацетоксициклогексан. [1]
Ацетат серебра , AgGH3COO, осаждают путем концентрирования раствора Ag2C03 в уксусной кислоте; это бесцветные кристаллы, растворимые в воде и спирте. [2]
Ацетат серебра , как менее растворимый, чем нитрат серебра, и более ковалентный адсорбируется на поверхности частиц иодида серебра сильнее, чем нитрат серебра. Анионы органических красителей хорошо адсорбируются на поверхности положительно заряженных частиц галогенидов серебра, так как молекулы их серебряных солей ковалентны. Малодиссоциированные молекулы сероводорода сильно адсорбируются на поверхности сульфидов металлов. [3]
Ацетат кальция и ацетон
Ацетат серебра CH3COOAg образуется в виде белого кристаллического осадка при добавлении раствора AgN03 к умеренно концентрированному раствору ацетатов щелочных металлов. [4]
Ацетат серебра менее активен. [5]
Ацетат серебра осаждают, добавляя избыток водного раствора ацетата калия к 0 125 моля нитрата серебра, растворенного в воде. Осадок отфильтровывают и трижды промывают ледяной уксусной кислотой, разбавленной уксусной кислотой, а затем обрабатывают таким количеством уксусного ангидрида, чтобьГраствор стал безводным. К ацетату серебра добавляют 0 1 моля / пранс-1 2-дибромциклогексана, выдерживают в течение 11 ч при температуре 100 — 110 С, охлаждают и фильтруют для удаления бромистого серебра. Фильтрат концентрируют при пониженном давлении. Остаток, состоящий преимущественно из соответствующего диацетата, омыляют в течение 2 ч действием 40 мл 35 % — ного водного раствора едкого натра и 40 мл этилового спирта. [6]
Использование ацетата серебра [2] значительно снижает выход. [7]
Для ацетата серебра в качестве растворителя пригодна ледяная уксусная1 кислота, для трифторацетата серебра — СС14 и до 150 С — нитробензол. Как кояку — рнруюпцш процесс может протекать реакция Бородина — Хунсдпкера [ 379] ( стр. [8]
К раствору ацетата серебра в пиридине добавляют ацетангидрид, взятый в избытке, при перемешивании и 20 С. В течение нескольких секунд выпадает аддукт кетена серебра с пиридином. После осторожной отгонки уксусной кислоты и пиридина получают Ag2C2O с количественным выходом. [9]
Произведение растворимости ацетата серебра при 25 С равно 4 4 — Ю 3, Сливаются растворы нитрата серебра и ацетата натрия. Осадок ацетата серебра не обнаружен. При [ Ag ] [ СН3СОО — ] 4 4 Ы0 — 3 замечено образование золя ацетата серебра. [10]
Получение ацетата меди
Рассчитайте растворимость ацетата серебра в чистой воде и количество выпадающей в осадок окиси серебра ( если осадок образуется), учитывая образование комплексов ацетата серебра ( см. табл. VIII. [11]
Сколько миллиграммов ацетата серебра может раствориться в 2 мл 0 5 М раствора азотной кислоты. [12]
Сколько миллиграммов ацетата серебра может раствориться-в 2 мл 0 5 М раствора азотной кислоты. [13]
Вная, что ацетат серебра менее растворим, чем нитрат серебра, укажите. [14]
Источник: www.ngpedia.ru
Ацетат серебра
Ацетат серебра является неорганическое соединение с эмпирической формулой CH 3CO2Ag (или AgC 2H3O2). Это светочувствительное, белое кристаллическое твердое вещество. Это полезный реагент в лаборатории в качестве источника ионов серебра без окисляющего аниона. Он использовался в некоторых противокурящих препаратах.
Синтез и структура
Ацетат серебра можно синтезировать реакцией уксусной кислоты и карбонат серебра при 45–60 ° C. После охлаждения до комнатной температуры твердый продукт осаждается.
2 CH 3CO2H + Ag 2CO3→ 2 AgO 2 CCH 3 + H 2 O + CO 2
Его также можно осаждать из концентрированных водных растворов нитрата серебра обработкой раствором ацетата натрия.
. Структура ацетата серебра состоит из 8- членные кольца Ag 2O4C2, образованные парой ацетатных лигандов, соединяющих пару центров серебра.
Ацетат серебра находит применение в определенных превращениях в органическом синтезе.
Сульфенамид синтез
Ацетат серебра используется для получения сульфенамидов из дисульфидов и вторичных аминов :
R2NH + AgOAc + (RS) 2 → R 2 NSR + AgSR + HOAc
Гидрирование
Раствор ацетата серебра в пиридине поглощает водород с образованием металлического серебра :
2 CH 3CO2Ag + H 2 → 2 Ag + 2 CH 3CO2H
Прямое орто-арилирование
Ацетат серебра является реагентом для прямого орто-арилирования. n (для установки двух соседних заместителей в ароматическом кольце) бензиламинов и N-метилбензиламинов. Реакция катализируется палладием и требует небольшого избытка ацетата серебра. Эта реакция короче, чем предыдущие методы ортоарилирования.
Окислительное дегалогенирование
Ацетат серебра можно использовать для превращения некоторых галогенорганических соединений в спирты. Несмотря на свою высокую стоимость, его можно использовать в случаях, когда требуется мягкий и селективный реагент.
Цис-гидроксилирование Вудворда
Ацетат серебра в сочетании с йодом составляет основу цис-гидроксилирования Вудворда. Эта реакция избирательно превращает алкен в цис- диол.
Применение
В области здравоохранения продукты, содержащие ацетат серебра, используются в жевательной резинке, спреях и пастилках. удерживать курильщиков от курения. Серебро, содержащееся в этих продуктах, при смешивании с дымом создает неприятный металлический привкус во рту курильщика, тем самым препятствуя курению. Пастилки, содержащие 2,5 мг ацетата серебра, показали «умеренную эффективность» на 500 взрослых курильщиках, испытанных в течение трехмесячного периода. Однако через 12 месяцев профилактика не увенчалась успехом. В 1974 году ацетат серебра был впервые представлен в Европе как безрецептурная таблетка для предотвращения курения (Repaton), а затем три года спустя как жевательная резинка (Tabmint).
Ацетат серебра также хорошо известен прекурсор, используемый в печатной электронике. В частности, сообщалось, что комплексы ацетата серебра образуют «реактивные чернила» без частиц, которые образуют следы, приближающиеся к объемной проводимости серебра (в пределах одного порядка величины).
Безопасность
LD 50 ацетата серебра у мышей составляет 36,7 мг / кг. Низкие дозы ацетата серебра у мышей вызывали повышенную возбудимость, атаксию, угнетение центральной нервной системы, затрудненное дыхание и даже смерть. FDA США рекомендует ограничить потребление ацетата серебра до 756 мг в течение короткого периода времени; чрезмерное потребление может вызвать аргирию.
Источник: alphapedia.ru
Ацетат серебра
Ацетат серебра — неорганическое соединение, соль металла серебра и уксусной кислоты с формулой CH3COOAg, белые кристаллы, растворяется в воде.
1S/C2H4O2.Ag/c1-2(3)4;/h1H3,(H,3,4);/q;+1/p-1
CQLFBEKRDQMJLZ-UHFFFAOYSA-M
Получение
- Растворение карбоната серебра(I) в уксусной кислоте:
Физические свойства
Ацетат серебра образует белые кристаллы.
Растворяется в воде и этаноле.
Похожие материалы

Органические кислоты 0
Лацериновая кислота CH3(CH2)30COOH — одноосновная предельная карбоновая кислота. Лацериновая кислота Общие Систематическоенаименование Дотриаконтановая кислота

Органические кислоты 0
Гентриаконтановая кислота CH3(CH2)29COOH — одноосновная предельная карбоновая кислота. Гентриаконтановая кислота Общие Систематическое наименование Гентриаконтановая

Органические кислоты 0
Гексатриаконтановая кислота H(CH2)35COOH — одноосновная предельная карбоновая кислота. Гексатриаконтановая кислота Общие Систематическоенаименование Гексатриаконтановая кислота

Органические кислоты 0
Геддовая кислота CH3(CH2)32COOH — одноосновная предельная карбоновая кислота. Геддовая кислота Общие Систематическое наименование
Органические кислоты 0
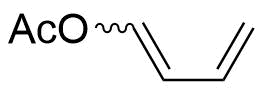
1-Ацетоксибутадиен-1, 3 — органическое вещество, принадлежащее к классу сложных эфиров. Формально является производным уксусной кислоты
Органические кислоты 0
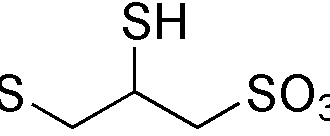
«Унитиол» — дезинтоксикационное лекарственное средство, сходное с димеркапролом. Как и димеркапрол, он имеет две готовые
Подкатегории
- Соединения азота
- Соединения актиния
- Соединения алюминия
- Соединения америция
- Соединения аргона
- Соединения астата
- Соединения бария
- Соединения бериллия
- Соединения берклия
- Соединения бора
- Соединения брома
- Соединения ванадия
- Соединения висмута
- Соединения вольфрама
- Соединения гадолиния
- Соединения галлия
- Соединения гафния
- Соединения германия
- Соединения гольмия
- Соединения диспрозия
- Соединения европия
- Соединения железа
- Соединения золота
- Соединения индия
- Соединения иода
- Соединения иридия
- Соединения иттербия
- Соединения иттрия
- Соединения кадмия
- Соединения калия
- Соединения кальция
- Соединения кислорода
- Соединения кобальта
- Соединения кремния
- Соединения криптона
- Соединения ксенона
- Соединения кюрия
- Соединения лантана
- Соединения лития
- Соединения лютеция
- Соединения марганца
- Соединения меди
- Соединения молибдена
- Соединения мышьяка
- Соединения натрия
- Соединения неодима
- Соединения нептуния
- Соединения никеля
- Соединения ниобия
- Соединения олова
- Соединения осмия
- Соединения палладия
- Соединения платины
- Соединения плутония
- Соединения полония
- Соединения празеодима
- Соединения прометия
- Соединения протактиния
- Соединения радия
- Соединения рения
- Соединения родия
- Соединения ртути
- Соединения рубидия
- Соединения рутения
- Соединения самария
- Соединения свинца
- Соединения селена
- Соединения серебра
- Соединения серы
- Соединения скандия
- Соединения стронция
- Соединения сурьмы
- Соединения таллия
- Соединения тантала
- Соединения теллура
- Соединения тербия
- Соединения технеция
- Соединения титана
- Соединения тория
- Соединения тулия
- Соединения углерода
- Соединения урана
- Соединения фосфора
- Соединения фтора
- Соединения хлора
- Соединения хрома
- Соединения цезия
- Соединения церия
- Соединения цинка
- Соединения циркония
- Соединения эрбия
- Все соединения
- Все предприятия
- Все элементы и определения
- ГОСТы
- Таблица Менделеева
Источник: chemicalportal.ru