Свойства. Конфигурация внешней электронной оболочки атома кальция 4s 2 ; в соединениях проявляет степень окисления +2, редко +1 ; электроотрицательность по Полингу 1,00, атомный радиус 180 пм, радиус иона Са 2+ 114 пм (координационное число 6). кальций — серебристо-белый мягкий металл; до 443 °С устойчива модификация с кубической гранецентрированной кристаллической решёткой, выше 443 °С — с кубической объёмно-центрированной решёткой; tпл 842°С, tкип1484 °С, плотность 1550 кг/м 3 ; теплопроводность 125,6 Вт/(м·К).
Кальций — металл высокой химической активности (хранят в герметически закрытых сосудах или под слоем минерального масла). При нормальных условиях легко взаимодействует с кислородом (образуется кальция оксид СаО), при нагревании — с водородом (гидрид СаН2), галогенами (кальция галогениды), бором (борид СаВ6), углеродом (кальция карбид СаС2), кремнием (силициды Ca2Si, CaSi, CaSi2, Ca3Si4), азотом (нитрид Ca3N2), фосфором (фосфиды Са3Р2, СаР, СаР5), халькогенами (халькогениды состава СаХ, где Х — S, Se, Те).
Кальций это химический элемент с символом Ca и атомным номером 20
Кальций взаимодействует с другими металлами (Li, Cu, Ag, Au, Mg, Zn, Al, Pb, Sn и др.) с образованием интерметаллидов. Металлический кальций взаимодействует с водой с образованием кальция гидроксида Са(ОН)2 и Н2. Энергично взаимодействует с большинством кислот, образуя соответствующие соли (например, кальция нитрат, кальция сульфат, кальция фосфаты).
Растворяется в жидком аммиаке с образованием тёмно-синего раствора с металлической проводимостью. При испарении аммиака из такого раствора выделяется аммиакат [Ca(NH3)6]. Постепенно кальций взаимодействует с аммиаком с образованием амида Ca(NH2)2. Образует различные комплексные соединения, наибольшее значение имеют комплексы с кислородсодержащими полидентатными лигандами, например комплексонаты Са.
Биологическая роль. Кальций относится к биогенным элементам. Суточная потребность человека в кальции — около 1 г. В живых организмах ионы кальция участвуют в процессах сокращения мышц, передачи нервных импульсов.
Получение. Металлический кальций получают электролитическим и металлотермическим способами. Электролитический способ основан на электролизе расплавленного хлорида кальция с катодом касания или жидким медно-кальциевым катодом. Из образующегося медно-кальциевого сплава отгоняют кальций при температуре 1000-1080 °С и давлении 13-20 кПа.
Металлотермический способ основан на восстановлении кальция из его оксида алюминием или кремнием при 1100-1200 °С. При этом образуется алюминат или силикат кальция, а также газообразный кальций, который затем конденсируют. Мировое производство соединений кальция и материалов, содержащих кальций, около 1 миллиарда т/год (1998).
Применение. Кальций применяют в качестве восстановителя при получении многих металлов (Rb, Cs, Zr, Hf, V и др.). Силициды кальция, а также сплавы кальция с натрием, цинком и другими металлами используют в качестве раскислителей и десульфураторов некоторых сплавов и нефти, для очистки аргона от кислорода и азота, в электровакуумных приборах в качестве поглотителя газов. Хлорид СаСl2 используют в качестве осушителя в химическом синтезе, гипс применяют в медицине. Кальция силикаты являются основными компонентами цемента.
Кальций — САМЫЙ НУЖНЫЙ МЕТАЛЛ ДЛЯ КОСТЕЙ!
Лит.: Родякин В. В. Кальций, его соединения и сплавы. М., 1967; Спицын В. И., Мартыненко Л. И. Неорганическая химия. М., 1994. Ч. 2; Неорганическая химия / Под редакцией Ю. Д. Третьякова. М., 2004. Т. 2.
Л. Н. Комиссарова, М. А. Рюмин.
Источник: knowledge.su
Все о кальции как химическом элементе
Кальций представляет собой химический элемент, относящийся ко второй подгруппе периодической таблицы с символическим обозначением Ca и атомной массой в 40,078 г/моль. Он представляет собой довольно мягкий и химически активный щелочноземельный металл с серебристым цветом.

Статьи по теме:
- Все о кальции как химическом элементе
- К каким элементам относится кальций
- В каких продуктах содержится больше всего кальция
Инструкция
С латинского языка «кальций» переводится как «известь» или «мягкий камень», а своим открытием он обязан англичанину Хэмфри Дэви, который в 1808 году смог выделить кальций электролитическим методом. Ученый тогда взял смесь влажной гашеной извести, «приправленную» оксидом ртути, и подверг ее процессу электролиза на платиновой пластине, фигурирующей в эксперименте в качестве анода. Катодом же выступала проволока, которую химик погрузил в жидкую ртуть. Интересно и то, что такие соединения кальция, как известняк, мрамор и гипс, а также известь, были известны человечеству за много столетий до эксперимента Дэви, в течение которых ученые полагали некоторые из них простыми и самостоятельными телами. Только в 1789 году француз Лавуазье опубликовал труд, в котором он предположил, что известь, кремнезий, барит и глинозем являются сложными веществами.
Кальций обладает высокой степенью химической активности, в силу чего в чистом виде в природе практически не встречается. Но ученые подсчитали, что на долю этого элемента приходятся около 3,38% от общей массы всей земной коры, что делает кальций пятым по распространенности после кислорода, кремний, алюминия и железа. Есть этот элемент в морской воде – около 400 мг на один литр.
Входит кальций и в состав силикатов различных горных пород (к примеру, гранит и гнейсы). Много его в полевом шпате, меле и известняках, состоящих из минерала кальцита с формулой СаСО3. Кристаллическая форма кальция – это мрамор. В общей же сложности путем миграции этого элемента в земной коре он образует 385 минералов.
К физическим свойствам кальция относится его способность проявлять ценные полупроводниковые способности, хотя он и не становится полупроводником и металлом в традиционном смысле этого слова. Меняется данная ситуация при постепенном повышении давления, когда кальцию сообщается металлическое состояние и способности проявления сверхпроводящих свойств. Легко взаимодействует кальций с кислородом, влагой воздуха и углекислым газом, в силу чего в лабораториях для работы этот химический элемент хранят в плотно закрытых банках, покрытых слоем керосина или парафина в жидком виде.
Главная и основная сфера применения кальция – восстановление при получении металлов (никель, медь и нержавейка). Элемент и его оксид также используется для получения трудновосстанавливаемых металлов – хрома, тория и урана.
Совет полезен?
Статьи по теме:
Добавить комментарий к статье
Похожие советы
- Какие химические элементы входят в состав клеток
- Какие химические элементы входят в состав клетки
- Как получить оксид кальция
- Какие продукты содержит кальций
- Гашеная известь: получение, свойства, применение
- Как хромировать металл
- Какими свойствами обладает алюминий
- Химические и физические свойства мела
Источник: www.kakprosto.ru
Строение атома кальция

Кальций (Ca) – щелочноземельный металл, входящий в состав минералов. Из-за строения атома кальций проявляет активные восстановительные свойства. Играет важную роль в метаболизме и постройке организма.
Строение
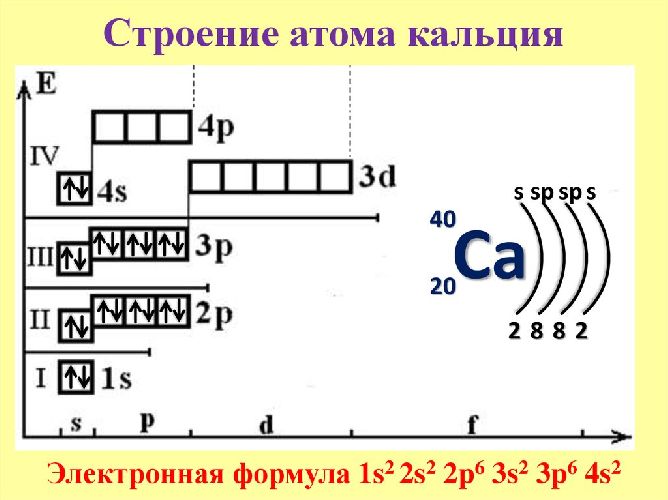
Кальций – 20 элемент периодической таблицы. Находится во второй группе, четвёртом периоде. Относится к элементам s-семейства. Электронное строение атома кальция – 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 или +20 Ca)2)8)8)2.
Ядро атома содержит 20 протонов и 20 нейронов, имеет положительный заряд +20. Вокруг ядра по четырём орбитам движется 20 электронов. Последний энергетический s-уровень содержит два спаренных электрона, поэтому постоянная валентность кальция – II.
В соединениях атом кальция отдаёт два электрона, выполняя функцию восстановителя. Степень окисления кальция – +2.
Кальций не может переходить в возбуждённое состояние.
Общее описание
Основным источником кальция является карбонат кальция – CaCO3, который является главным соединением известняка, мела, мрамора. Также кальций входит в состав доломита, гипса, апатита, шпата и других минералов.
Кальций – металл серебристого цвета с температурой плавления 854°С. При высоком давлении проявляет свойства полупроводника. Легко окисляется на воздухе.

Кальций получают электролизом расплавленного хлорида кальция – CaCl2.
Химические свойства
Схема строения атома определяет химические свойства элемента. Кальций активно реагирует с простыми и сложными веществами. Из-за способности быстро присоединять кислород, образуя на поверхности оксидную плёнку, кальций хранят под слоем парафина или керосина в плотно закрытой таре. Основные реакции кальция с элементами и соединения приведены в таблице.
Взаимодействие
Продукты
Уравнение
С кислородом при нагревании (реакция горения)
Оксид кальция (негашёная известь)
С большинством неметаллов при нагревании
С фтором даже на холоде
Гидроксид кальция (гашёная или едкая известь) выпадает в осадок, выделяется водород
Большинство солей кальция (фторид, сульфат, карбонад кальция) не растворяются в воде. Хорошо растворимы бромид (CaBr2), хлорид (CaCl2), йодид (CaI2), нитрат (Ca(NO3)2) кальция.
Элемент в составе соединений используется в строительстве, пищевой и химической промышленности, медицине.
Что мы узнали?
Кальций – активный щелочноземельный металл, являющийся восстановителем. На внешнем энергетическом уровне атома находится два электрона, определяющие валентность. Кальций входит в состав минералов, быстро окисляется на воздухе, реагирует с неметаллами при нагревании, водой и кислотами. Оксид кальция называется негашёной известью, гидроксид – гашёной известью.
Большинство солей кальция плохо растворяются в воде. Кальций входит в состав костей, крови, участвует в метаболизме, применяется в промышленности, строительстве и медицине.
Источник: obrazovaka.ru