PCl3 — Не уверен, вроде ионная связь и ионная решетка
Br2 — Ковалентно неполярная связь и Молекулярная кристаллическая решетка
Li3N — Ионная связь и ионная кристаллическая решетка
H2 — Ковалентно неполярная связь и молекулярная кристаллическая решетка
Ba — металлическая связь и металлическая кристаллическая решетка
Na2S — Ионная связь и ионная кристаллическая решетка
K — Металлическая связь и металлическая кристаллическая решетка
I2 — Ковалентно неполярная связь и Молекулярная кристаллическая решетка
CO — Ковалентно полярная связь и Молекулярная кристаллическая решетка
CaF2 — ионная связь и ионная кристаллическая решетка
P4 — Ковалентно неполярная связь и Молекулярная кристаллическая решетка
Источник: megaurok.com
Определите тип кристаллической решётки для элементов:
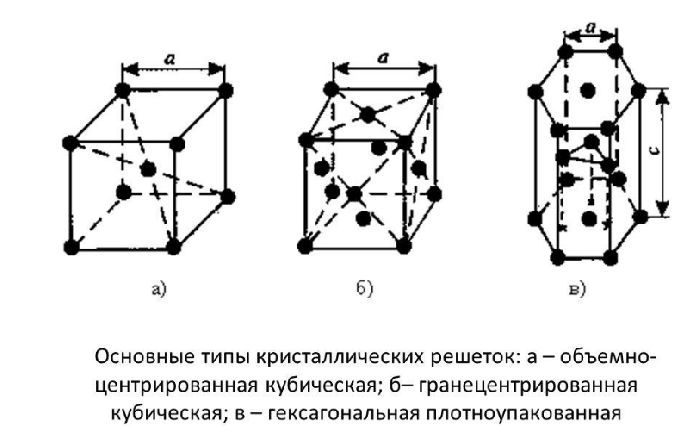
Типы кристаллических решеток
Найди верный ответ на вопрос ✅ «Определите тип кристаллической решётки для элементов: Cao, N2O5, Cl2, MgBr2, HF, K, Zn (OH) 2. Na2Cr2O7. . » по предмету Химия, а если ответа нет или никто не дал верного ответа, то воспользуйся поиском и попробуй найти ответ среди похожих вопросов.
Новые вопросы по химии
Что произойдёт с железом при взаимодействии с водой? 3 класс.
C8h18 формула глюкозы
1. Цинк растворили в концентрированной азотной кислоте. Полученный газ растворили в горячей воде. В ходе этого взаимодействия образовался бесцветный газ. Он легко окисляется кислородом воздуха до образования бурого газа.
Закончите формулы. H2+CuO= Na+HCl =
Что такое макроэлементы и ультромикроэлементы?
Главная » Химия » Определите тип кристаллической решётки для элементов: Cao, N2O5, Cl2, MgBr2, HF, K, Zn (OH) 2. Na2Cr2O7.
Источник: urokam.net
Оксид кальция

Негашёная известь – это оксид кальция. Его получают в лабораториях и промышленным путём из природных материалов. Вещество активно используется в строительстве и промышленности.
Физические свойства
Оксид кальция – неорганическое кристаллическое вещество в виде белого или серо-белого порошка без запаха и вкуса. Твёрдое вещество кристаллизуется в кубические гранецентрированные кристаллические решётки по типу хлорида натрия (NaCl).
Общее описание вещества представлено в таблице.
Признак
Значение
Формула соединения оксид кальция
В глицерине. В этаноле не растворяется, с водой образует гидроксид
Кристаллические решетки: заучить или понять за 20 минут? | Химия ЕГЭ 2023 | Умскул
Химическая связь в кристалле
Оксид кальция – едкое вещество, относящееся ко второму классу опасности. Агрессивные свойства проявляет при взаимодействии с водой, образуя гашёную известь.

Получение
Оксид кальция также называют жжёной известью из-за способа получения. Получают негашёную известь путём нагревания и разложения известняка – карбоната кальция (CaCO3).
Это природное вещество, встречающееся в форме минералов – арагонита, ватерита, кальцита. Входит в состав мрамора, мела, известняка.
Реакция получения оксида кальция из известняка выглядит следующим образом:
CaCO3 → CaO + CO2.
Кроме того, негашёную известь можно получить двумя способами:
-
из простых веществ, наращивая оксидный слой на металле –
2Ca + O2 → 2CaO;
Ca(OH)2 → CaO + H2O; 2Ca(NO3)2 → 2CaO + 4NO2 + O2.
Химические свойства
Оксид кальция является высшим оксидом и максимально проявляет окислительные свойства. Соединения взаимодействует с неорганическими веществами и свободными галогенами. Основные химические свойства оксида приведены в таблице.
Что образуется
Молекулярное уравнение
Образуется гидроксид (гашёная известь). Реакция протекает бурно с выделением тепла
Растворяется, образуя соли
С оксидами неметаллов (кислотными остатками)
С углеродом при нагревании
Образуется карбид кальция
CaO + 3С → СаС2 + CO
Восстанавливает кальций. Образуется оксид алюминия
Применение
Оксид используется в пищевой промышленности в качестве:
- улучшителя муки и хлеба;
- пищевой добавки Е529;
- регулятора кислотности;
- питательной среды для дрожжей;
- катализатора гидрогенизации (присоединения водорода) жиров.
Кроме того, негашёная известь применяется в химической и строительной промышленности для производства различных веществ:

- масел;
- стеарата кальция;
- солидола;
- огнеупорных материалов;
- гипса;
- высокоглиноземистого цемента;
- силикатного кирпича.
Что мы узнали?
Оксид кальция или негашёная известь – кристаллическое вещество, бурно реагирующее с водой и образующее гашёную известь. Широко используется в промышленности, в частности пищевой и строительной. Зарегистрирован как пищевая добавка Е529. Имеет высокие температуры плавления и кипения, растворяется только в глицерине. Образуется при сжигании карбоната кальция.
Проявляет окислительные свойства, образует соли с оксидами и кислотами, взаимодействует с углеродом и алюминием.
Источник: obrazovaka.ru