Для технологических цианистых растворов с концентрацией золота и серебра выше 40-50 г/м 3 часто наиболее экономичным оказывается электролитический метод осаждения, не требующий применения химических реагентов и позволяющий многократно использовать растворы в обороте. Потребность в применении электролиза возникает при цианистой переработке богатых концентратов и при использовании угольно-сорбционной технологии в цикле щелочной десорбции золота и серебра с угля.
Существует два типа электролизеров: циркуляционные и проточные. Циркуляционные работают в периодическом режиме и требуют использования крупногабаритной баковой аппаратуры. Электролизеры проточного типа не требуют дополнительного оборудования, они имеют многоступенчатую конструкцию, обеспечивающую необходимую степень (96-99%) осаждения металлов за однократный проток раствора. Сложная многоступенчатая конструкция ограничивает возможность конструирования высокопроизводительных электролизеров и затрудняет их обслуживание.
Восстановление золота после электролиза
В ОАО «Иргиредмет» разработана принципиально новая конструкция проточного однокамерного электролизера с сетчатым катодом — «ЭПС» (электролизер проточный сетчатый). Новый электролизер ЭПС дешевле, экономичнее и удобнее в эксплуатации, чем электролизеры других конструкций.
Два проточных электролизера ЭПС изготовлены и установлены на ЗИФ «Валунистая». Электролизеры работают в цикле осаждения золота и серебра из элюатов процесса угольной десорбции. Производительность одного электролизера 2-3 м 3 элюата в час. Степень осаждения металлов — 98%. Электроосаждение металлов идет в режиме самоосыпания осадка.
Операцию выгрузки осадков проводят в течение 20-30 минут без остановки процесса электролиза.
Работа электролизеров в течение пяти лет показала их надежность и удобство в обслуживании.
Электролизеры изготавливаются по заказу различной производительности: ЭПС-0,4 — производительностью 0,4 м 3 /ч и ЭПС-2,5 — производительностью 2,5 м 3 /ч.
Технические характеристики электролизеров Иргиредмета
ЭПС-0,4
ЭПС-2,5
Источник: zolotodb.ru
Аффиннаж золота и серебра
Аффинаж является процедурой, в ходе которой из благородных металлов удаляются всевозможные примеси. У нас для ее осуществления используют централизованные заводы, обладающие соответствующим оборудованием, и имеющими возможность обеспечить условия, при которых передел будет проведен с минимальными потерями.
Аффинажные заводы занимаются переработкой шлихового и самородного золота, которое выделяется в ходе гравитационного обогащения россыпей и руд, золота из амальгам и т.п. Кроме того, здесь происходит переработка производственного и бытового лома, старых монет, сплавов и т.п. материалов.
Во время переработки представляется возможным получение не только золота и серебра, но и платиновых металлов, меди, свинца, сурьмы, олова, висмута и т.п. примесей.
Электролиз золота какая нужна зарядка для электролиза
Чаще всего для отражения того, сколько же в сплаве находится благородного металла, используется термин пробы (тысячная доля массы). Лигатура – это общий объем неблагородных примесей.
Металл доре из электролитных шламов меди
То же, со свинцовых заводов
Для отделения лигатуры и основной массы серебра, жидкий сплав должен пройти процедуру продувки хлором в графитовых тиглях. Далее осуществляется хлорирование всех металлов, а хлориды преимущественно должны при этом раствориться в шлаке (для его получения пользуются бурой, содой и песком).
В первую очередь происходит возгонка и переход в шлак хлоридов, состав которых представлен элементами лигатуры, после этого – AgCl, и только после этого – AuCl3. Как только появляются первые признаки, подтверждающие хлорирование золота, процесс продувки прекращается, металл должен быть разлит по изложницам, и передан в валютный фонд. Кроме того, представляется возможным проведение нижеописанной процедуры электролиза, которая позволяет получить более высокое качество очистки. Ее осуществление необходимо для случаев, когда состав материала представлен платиноидами.
Состав хлоридного шлака преимущественно представлен AgCl и CuCl, он подвергается дроблению, после чего грузится в мешки, и располагается в ванной, где находится разбавленная серная кислота и листы железа. При этом ионы Fe2+ используются для восстановления серебра:
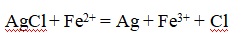
Хлорид меди подвергается окислению:
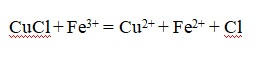
В результате того, что Cu2+ проникается сквозь ткань мешка, осуществляется его цементирование железом. Железо также используется для восстановления ионов Fe3+, поэтому их массовая часть в растворе является очень маленькой, следовательно, происходит сдвижение вправо равновесия реакции, в ходе которой серебро восстанавливается железом. Для того чтобы процедура была завершена в достаточной мере, требуется порядка двух суток, а температуры раствора при этом должна находиться в пределах 90-100 ° C.
Далее осадок цементного серебра подвергается прессовке, плавке и отливке в аноды по 10кг (плиты, толщина которых порядка 10мм). Их состав должен быть представлен не более чем 200 пробами золота и 75 пробами лигатуры.
Процесс электролиза серебра
Роль электролита в данном случае отводится раствору AgNO3, активность которого составляет 1моль/л (до 100 г/л Ag).
После того, как аноды растворяются, раствор пополняется серебром, медью, свинцом, висмутом и иными примесями. Золото выпадает как порошкообразный шлам, состав которого представлен платиновыми металлами, селеном, теллуром, серой и иными примесями, которые не растворяются в электролите.
Для изготовления катодных основ пользуются тонкими алюминиевыми или серебряными листами.
Для катодного осадка серебра характерно наличие рыхлой крупнокристаллической структуры; он может быть легко счищен с катодной основы, и оказаться на дне ванны. Для избегания смешивания осадка чистого серебра с золотым шламом, аноды должны располагаться в тканевых мешках.
Для растворения 10мм анодов требуется порядка суток. После этого происходит возвращение нерастворенного осадка на плавку, из анодных чехлов происходит выгрузка золотого шлама, а извлечение кристаллов чистого серебра со дна ванны осуществляется при помощи алюминиевых дырчатых черпаков.
При этом показатель плотности тока должен находиться в пределах 0,4-0,6 кА/м2, электролит должен быть подвержен энергичному перемешиванию. Недопустимо, чтобы в нем существенно накапливались примеси, в т.ч. медь, превышение массовой доли которой в растворе показателя в 4-5 % может стать причиной загрязнения катодного осадка.
Когда золота будет свыше 200 проб, оно будет приводить к пассивированию анодов, следовательно, начинается процесс выделения кислорода, а также происходит существенный скачок напряжения в ванной.
Для изготовления ванн, емкость которых не превышает 0,6 м3, используется винипласт, а для их укрепления используется каркас из железа или дерева. Выделяемое током тепло используется, чтобы поддерживать комфортную для электролита температуру на уровне 40 градусов. Чтобы перемешивать раствор используется воздух. Состав электролита и плотность тока во многом оказывают влияние на показатель напряжения в ванной.
Чистота осадка серебра, когда им была пройдена промывка при помощи разбавленной азотной кислоты, воды, а также процедура переплавки, составляет 999,9 проб. Использование электролиза дает возможность получения металла с 999,99 или 999,999 пробой.
Отдельные ванные с анодами, представленными низкопробными сплавами, используются для обеднения отработанного электролита серебром.
Электролиз золота
Поступлению металла на электролиз предшествует процедура хлорирования. Кроме того, в данном процессе используются и полученные в ходе электролиза серебра шламы, которые проходят химическую очистку. Все должно быть расплавлено в индукционной печи, и впоследствии отлито в аноды прямоугольной формы, масса каждого из которых составляет 2-3 кг.
Роль электролита отводится раствору НАuСl4 и НСl (до 200 г/л Аu и 80 г/л НСl). Для растворения золота используется реакция:
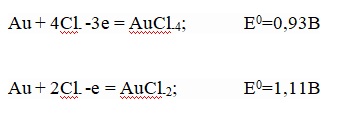
Ионы AuCl-2 могут появляться в результате концентрационной поляризации или в результате того, что на аноде формируется корка AgCl. Но практически сразу происходит процесс их диспропорционации, при котором выделяются выпадающий в шлам осадок металла:
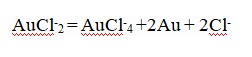
Если кислотность и температура будут недостаточными, то происходит пассивирование золотых анодов, они перестают растворяться, и начинает выделяться хлор

Если кислород перенапрягается на золоте, то он не будет выделяться. Оптимальная температура для осуществления электролиза составляет 50-60 градусов. Кроме того, происходит процесс растворения и накопления в электролите палладия и платины:
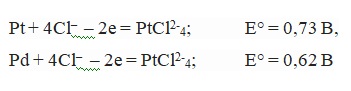
На основании составляющих лигатуры – меди, свинца, висмута, железа, олова, сурьмы и т.п. металлов, происходит формирование простых ионов или же комплексных хлоридов. В большинстве случаев они не приводят к затруднениям при растворении анода. В результате переходящего в раствор в виде Fe2+ железа происходит восстановление золота, в результате чего возрастает его переход в шлам.
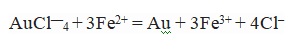
Серебро дает нерастворимый хлорид.
![]()
Если сплав представлен менее чем полусотней проб серебра, его хлорид не будет вызывать осложнений. Если же проб больше, то анод покроется коркой из АgCl, которая будет мешать растворению золота.
Способ Вольвиля используется для растворения золотых анодов, состав которых представлен до 200 проб серебра, с использованием ассиметричного тока. Для этого через ванную одновременно должны пропускаться одинаковые по силе переменный и постоянный токи.
Необходимо отметить минимальную вероятность того, что катодный осадок будет загрязнен при помощи примесей. Однако вполне вероятным видится то, что вместе с золотом осядет платина и палладий, особенно, если плотность тока будет высокой. Чтобы избежать этого, в каждом литре раствора должно быть не более 15г палладия и до 50г платины. Других примесей в растворе, содержащем не менее 100 г/л золота, не должно быть больше Сu 90 г/л; Рb 1,5 г/л; Те 4 г/л и 2 % Fe.
Для обеднения отработанного электролита по золоту используются отдельные ванны с анодами из графита, затем для выделения из него золота и платиноидов могут быть использованы самые различные способы.
Для осуществления электролиза золота используются фарфоровые (иногда винипластовые) ванны, емкость которых составляет 25 литров. Аноды должны быть выстроены в ряд и подвешены на штанги из серебра, после чего напротив каждого ряда располагается катод, на котором устанавливается 0,2 мм рифленая золотая фольга. Установка ванн происходит в водяных банях, а для перемешивания электролита используется воздух.
Общий показатель суммарной плотности постоянного и переменного тока может доходить до 1,5 кА/м2, показатель напряжения в ванной находится на уровне 1 В. Механическая очистка при помощи щеток, а также промывка при помощи аммиака и соляной кислоты позволяет добиться чистоты катодного осадка на уровне 999,9 проб.
Источник: metallplace.ru
Электролитическое рафинирование золота
Аффинаж золота электролизом позволяет получать металл высокой чистоты. Аноды отливают из рафинируемого сплава, содержащего в качестве примесей серебро, платиновые металлы и некоторые неблагородные металлы. Электролитом служит водный раствор золотохлористоводородной кислоты с добавкой соляной кислоты:

Золотохлористоводородная кислота является сильной и полностью диссоциирует на ионы:

В свою очередь анионы Аu частично диссоциируют с образованием катионов Аu 3+ :

Однако константа диссоциации Кд этого комплекса очень мала:


т. е. равновесие реакции (2) смещено влево. В водном растворе ионы АuСlмогут подвергаться гидролизу:


Однако в кислом растворе гидролиз практически неидет. Таким образом, можно считать, что золото в электролите находится в форме аниона . Основной катодный процесс при электролитическом рафинировании золота представляет собой восстановление анионов до металлического золота:

Стандартный потенциал этого процесса равен +0‚99 В, поэтому конкурирующий с ним процесс восстановления водорода практически исключен.
На аноде происходит растворение рафинируемого сплава с переходом золота в раствор:

Так как стандартные потенциалы хлора и кислорода значительно элехтроположительнее, чем потенциал золота:

то выделение их на аноде в нормальных условиях электролиза невозможно. Однако характерная и весьма важная особенность анодного поведения золота — его склонность к пассивированию. При переходе золота в пассивное состояние растворение анода прекращается, потенциал его смещается в положительную сторону и достигает такой величины, при которой становится возможным выделение газообразного хлора.
Явление пассивирования крайне нежелательно: на аноде вместо полезного процесса растворения золота происходит вредный процесс — окисление ионов хлора, приводящее к обеднению электролита золотом и отравлению атмосферы цеха.
Электролиз золота ведут в небольших ваннах из фарфора или винипласта вместимостью 20-65 л.
В отечественной практике применяют фарфоровые ванны вместимостью 25 л. В качестве катодов используют золотую жесть толщиной 0‚1-0‚25 мм, изготовляемую прокаткой чистого электролитного золота. Для придания катодам жесткости их подвергают рифлению на специальном прессе. В ванны (рис. 5) подвешивают 18 катодов (на рисунке не показаны) на шести штангах (по три катода в ряд)‚ и 15 анодов на пяти штангах (по три анода в ряд). Масса одного анода составляет примерно 2 кг.
Аноды подвешивают к штангам с помощью золотых ленточек, вплавленных в металл при отливке анодов. Для поддержания необходимой температуры электролита ванны устанавливают в водяных банях. Электролит перемешивается сжатым воздухом, подаваемым в ванны по стеклянным трубкам. Так как при электролизе выделяется хлор, ванны помещают в специальном вытяжном шкафу.
Ток подводят снаружи шкафа по медным шинам, а внутри — серебряным как более стойким в атмосфере хлора. Из серебра же делают штанги для подвески электродов.
Электролит содержит 70-200 г/л Au и 40-100 г/л НСl]. Температура электролита 50-60 °С. Электролиз ведут асимметрическим током плотностью 6ОО-1500 А/м 2 . Сила переменного тока обычно на 10 % выше, чем постоянного. Напряжение на ванне 0,5-1 В. Золото осаждается на катоде в виде плотного блестящего осадка. Катоды разгружают 3-4 раза в сутки в зависимости от плотности применяемого тока.
Катодное золото промывают горячей водой, очищают щетками, обрабатывают соляной кислотой или аммиаком (для растворения случайно приставших частиц хлорида серебра), снова промывают водой, сушат и плавят в индукционной печи в слитки. Чистота катодного золота 999,8-999‚9 пробы. Основными примесями в нем являются серебро‚ медь, железо.
Анодный шлам выгружают из ванн и отмывают водой от электролита. Промывные воды используют для доливки ванн. Шлам загружают в сетчатый серебряный барабан, помещенный в наполненную водой ванну. При вращении барабана хлорид серебра через отверстия смывается в ванну, а более крупные частицы золотого анодного скрапа и дендриты катодного золота остаются в барабане.
Золотые остатки сушат и возвращают в плавку на аноды. Хлористое серебро восстанавливают железным скрапом или порошком в солянокислой среде, промывают водой и плавят в аноды для серебряного электролиза. Выход анодного скрапа при электролизе золота зависит от чистоты анодов и колеблется от 10 до 20 % массы исходных анодов. Так же, как и шлам, остатки анодов отмывают в сетчатом барабане от хлорида серебра и электролита, сушат и плавят в аноды.
В процессе электролиза электролит обогащается примесями и обедняется по золоту. При работе на грязном электролите возможно загрязнение катодных осадков вследствие соосаждения примесей. Помимо этого, при загрязнении электролита на катоде начинается рост дендритов, что приводит к замыканию электродов, а на аноде — кристаллизация солей, ведущая к пассивации анодов. Электролит негоден к дальнейшему использованию, если концентрация золота в нем ниже 100 г/л, а концентрация примесей выше следующих пределов, г/л: 90 Сu, 50 Рt, 15 Рd, 1,5 РЬ, 4 Те, 2 Fе.
Для переработки отработанный электролит заливают в специальные ванны, где электролизом с нерастворимыми анодами из него извлекают большую часть золота. Катодами служат тонкие золотые пластины, аноды изготавливают из графита. Процесс ведут, применяя постоянный ток плотностью 200-500 А/м 2 . Из полученного раствора хлористым аммонием осаждают платину и палладий, а затем с помощью раствора хлористого железа доосаждают остатки золота. Медь цементируют железом.
Возможны и другие методы переработки отработанного электролита, в частности, с применением ионообменных смол.
Свежий электролит готовят электрохимическим растворением относительно чистых сплавов золота, получаемых чаще всего в результате обработки анодного шлама серебряного электролиза. Растворение ведут в специальных ваннах круглой формы (рис. 6), снабженных диафрагмами из пористого фарфора, глины или ионообменной пленки.
В диафрагму завешивают 6-8 анодов и заливают соляную кислоту плотностью 1,19, разбавленную водой в отношении 3: 1. По обе стороны от диафрагмы подвешивают катоды — тонкие пластины из золота или графита. В катодное пространство заливают более разбавленную (1 : 3) соляную кислоту, При пропускании постоянного тока на аноде
растворяется золото, на катоде — восстанавливается водород. Суммарная реакция выражается следующим уравнением:

Процесс ведут с помощью постоянного тока плотностью 800-2000 А/м 2 . Напряжение на ванне для диафрагмы из ионообменной пленки составляет до 4 В, для диафрагмы из глины — до 14 В. Температура электролита 60-90°С.
Полученный раствор содержит 200-300 г/л Аu и 45-80 г/л соляной кислоты. Его разбавляют водой и заливают в ванны основного электролиза. Свежий электролит можно также готовить растворением катодного золота в соляной кислоте при пропускании газообразного хлора.
Достоинством процесса электролитического рафинирования золота является не только возможность получения высокочистого металла, удовлетворяющего требованиям современной техники, но и попутное извлечение платиновых металлов, теряемых при аффинаже хлорированием.
В ЮАР электролитическому рафинированию подвергают часть золота, прошедшего аффинаж хлорированием. При этом на электролиз направляют предпочтительно те партии золота, в которых содержатся платиновые металлы.
Источник: vuzlit.com