Файл «K_shestomu_seminaru_2013» внутри архива находится в папке «Семинары по физической химии». Документ из архива «Семинары по физической химии», который расположен в категории » «. Всё это находится в предмете «физическая химия» из 6 семестр, которые можно найти в файловом архиве МГУ им. Ломоносова. Не смотря на прямую связь этого архива с МГУ им. Ломоносова, его также можно найти и в других разделах. .
Онлайн просмотр документа «K_shestomu_seminaru_2013»
Текст из документа «K_shestomu_seminaru_2013»
Фазовая диаграмма воды. В пределах каждой из областей диаграммы, ограниченных линиями АО, ВО и СО, существует единственная фаза и число степеней свободы равно f = 3 – 1 = 2, следовательно, можно одновременно изменять оба параметра – температуру и давление – не вызывая этим изменения числа фаз. Линии на диаграмме соответствуют условиям сосуществования (равновесия) двух фаз: линия АО отображает равновесие лед ⇄ пар, ВО – равновесие лед ⇄ жидкость, линия СО – жидкость ⇄ пар. Во всех точках, лежащих на этих линиях,
Насыщенный пар. Зависимость давления пара от температуры | Физика 10 класс #35 | Инфоурок
f = 3 – 2 = 1, и независимо можно изменять только один параметр – температуру или давление. В этом случае две фазы будут оставаться в состоянии равновесия, только если другой параметр – давление или температура – будет изменяться строго определенным образом, в соответствии с уравнением Клапейрона-Клаузиуса. Точка О называется тройной точкой.
В ней в равновесии существуют три фазы, а число степеней свободы равно f = 3 – 3 = 0. Координаты тройной точки являются индивидуальной характеристикой каждого вещества. Поскольку Hсубл Hпл, кривая АО имеет больший наклон, чем кривая СО (см. уравнение Клапейрона-Клаузиуса). Пунктирная линия ОС’ отражает зависимость давления пара над переохлажденной жидкой водой от температуры. Состояние переохлажденной жидкости является метастабильным (неустойчивым). Из рисунка видно, что при температурах ниже температуры кристаллизации (например, при температуре T1)
pж ртв, где pж и ртв – давления насыщенного пара над переохлажденной жидкостью (точка 1) и твердой фазой (точка 2) соответственно. Учитывая, что при двухфазных равновесиях ж = п = п(T) + RTlnpж и тв = п = п(T) + RTlnpтв , можно сделать вывод, что ж тв.
Это означает, что в этих условиях жидкое состояние является термодинамически неустойчивым, и вода с ходом времени должна самопроизвольно закристаллизоваться. Кривая ОС обрывается в точке, которая называется критической (для справки – критические параметры воды 374ºС и 218 атм).
Кривая ОВ для воды имеет обратный наклон, то есть температура плавления понижается с ростом давления. Причина этого заключается в том факте, что Vпл у воды при невысоких давлениях имеет отрицательное значение, поскольку плотность льда меньше плотности жидкой воды (зимой лед находится на поверхности водоемов).
В области высоких давлений кривая ОВ изменяет свой наклон и разветвляется, что связано с существованием в этих условиях различных кристаллических модификаций льда, между которыми возможны фазовые переходы. Некоторые формы льда имеют высокие температуры плавления; так, одна из модификаций плавится при 100С и давлении около 25000 атм. Пример 4.
Давление насыщенного пара
Почему лед в теплом помещении плавится, а твердый CO2 («сухой лед») возгоняется (сублимируется), минуя жидкое состояние? Решение. Чтобы ответить на этот вопрос, рассмотрим и сравним диаграммы состояния воды и углекислого газа.
 Из диаграмм хорошо видно, что при нагревании воды при атмосферном давлении (1 атм) возможны два фазовых превращения: «лед → жидкость» и «жидкость → газ», а у СО2 возможно всего одно фазовое превращение: «твердый СО2 → газ». Давление тройной точки СО2 составляет 5.12 атм, и при любом меньшем давлении существование жидкого СО2 невозможно (раньше летом мороженое охлаждали твердым «сухим льдом», а вот в баллонах со сжатой двуокисью углерода обычно содержится жидкий СО2).
Из диаграмм хорошо видно, что при нагревании воды при атмосферном давлении (1 атм) возможны два фазовых превращения: «лед → жидкость» и «жидкость → газ», а у СО2 возможно всего одно фазовое превращение: «твердый СО2 → газ». Давление тройной точки СО2 составляет 5.12 атм, и при любом меньшем давлении существование жидкого СО2 невозможно (раньше летом мороженое охлаждали твердым «сухим льдом», а вот в баллонах со сжатой двуокисью углерода обычно содержится жидкий СО2).
Еще один пример твердого вещества, возгоняющегося при атмосферном давлении – кристаллический иод I2, образующий при нагревании красивые фиолетовые пары. Пример 5.
Зависимость давления (в Па) насыщенных паров серебра от температуры выражается уравнениями:  (для твердого серебра);
(для твердого серебра);  (для жидкого серебра). Определите координаты тройной точки серебра и величины ΔHпл, ΔSпл и ΔGпл вблизи тройной точки.
(для жидкого серебра). Определите координаты тройной точки серебра и величины ΔHпл, ΔSпл и ΔGпл вблизи тройной точки.
Решение. В тройной точке давления паров твердого и жидкого серебра равны, следовательно  Ттр.т. =
Ттр.т. =  = 1247.7 К; ртр.т. = 452.3 Па.
= 1247.7 К; ртр.т. = 452.3 Па.
Из уравнения Клаузиуса-Клапейрона  с учетом соотношения ln p = 2.303·lg p, получим ΔHисп = 8.31 2.303 13340 = 255.42 кДжмоль –1 ; ΔHсубл = 8.31 2.303 14020 = 268.44 кДжмоль –1 . Воспользуемся тем, что ΔHпл = ΔHсубл – ΔHисп; ΔHпл = 268.44 – 255.42 = 13.02 кДжмоль –1 ; ΔSпл =
с учетом соотношения ln p = 2.303·lg p, получим ΔHисп = 8.31 2.303 13340 = 255.42 кДжмоль –1 ; ΔHсубл = 8.31 2.303 14020 = 268.44 кДжмоль –1 . Воспользуемся тем, что ΔHпл = ΔHсубл – ΔHисп; ΔHпл = 268.44 – 255.42 = 13.02 кДжмоль –1 ; ΔSпл = 
Источник: studizba.com
Давление насыщенного пара серебра
Ch emist L ab.ru
Группа: Пользователи
Сообщений: 3
Статус: Offline
Группа: Супермодераторы
Сообщений: 6490
Статус: Offline
Группа: Пользователи
Сообщений: 3
Статус: Offline
Цитата FilIgor ( )
Свои идеи есть?
Последнюю я кое-как решил. В тройной точке давления пара над жидким и твердым серебром равны, значит приравниваем два уравнения и находим Т, потом подставляем Т в любое и находим давление.
А первую никак не получается. Вроде и куча формул под рукой, но не могу понять какую конкретно применить к этой задаче. Разве что моли бензола и толуола посчитал, но что дальше с ними делать не знаю.
Группа: Супермодераторы
Источник: chemistlab.ru
Семинар по теме «Фазовое равновесие в однокомпонентных системах» № 1
1. Давление пара над кристаллическим ацетиленом при 132 К равно 2,3 * 10 2 Па, а при 153 К равно 36,8 * 10 2 Па. Рассчитайте теплоту плавления ацетилена, если удельная теплота испарения ацетилена составляет 828 Дж/г.



Данные о теплоте испарения приведены в условии, теплоту возгонки получим с помощью уравнения Клапейрона – Клаузиуса:



Проинтегрируем в приближении :


Выразим :

Переведём теплоту испарения из  в
в  :
:


Ответ: ∆Нвозг = 22170 кДж/моль; ∆Нисп = 21530 кДж/моль; ∆Нпл = 640 Дж/моль.
2. Тангенс угла наклона к зависимости температуры от внешнего давления для металлического висмута равен -3,7 * 10 -8 К/Па. Рассчитайте теплоту плавления висмута при температуре 256 ºС, если изменение объёма в процессе плавления составляет -0,78 см 3 /моль.
Воспользуемся уравнением Клаузиуса:


Ответ: 11,15 кДж/моль.
3. При какой температуре закипит вода, находящаяся под давлением 25008 Па. Найдите среднее значение теплоты испарения в интервале 65 – 70 ºС.
В таблице 21 – Давление насыщенного пара воды, льда и переохлаждённой воды при различной температуре найдём значение давления насыщенного пара над водой при температурах 65 и 70 ºС:
P65 = 25008 Па; P70 = 31161 Па;

Ответ: ∆Нисп = 42,41 кДж/моль.
4. Зависимости давления насыщенного пара над жидким и твёрдым серебром в полулогарифмических координатах lgP = f (1/T) представляет собой ломанную линию с двумя линейными участками. Значения тангенсов угла наклона этих прямых соответственно равны: tgα = -13340 К -1 и tgβ = -14020 К -1 . Рассчитайте теплоту плавления 1 моля серебра в тройной точке.

Левая верхняя часть ломанной кривой описывает зависимость равновесного давления над жидкостью, а правая нижняя над твёрдым телом. В этом легко убедиться двумя способами:
1. Левая верхняя находится в области более высоких давлений и температур;
2. Угол наклона левой верхней части, связанный с теплотой испарения, меньше, т.к. теплота испарения меньше теплоты возгонки.
Тангенс угла наклона касательной к кривой в данных координатах равен значению производной функции по оси ординат по функции по оси абсцисс:


Тогда
Аналогично  268440
268440 

Ответ: 13,02 кДж/моль.
5. Зависимость давления насыщенного пара от температуры над твёрдым серебром передаётся уравнением lgP (Па) = 13,9 – 14020/Т, а над жидким lgP (Па) = 13,3 – 13340/Т. Определите координаты тройной точки, теплоту плавления серебра и изменение энтропии в процессе плавления серебра при температуре тройной точки.
В тройной точке линии, описываемые уравнениями пересекаются, а уравнения имеют общий корень:




Расчёт по обоим уравнениям дал один ответ, однако иногда они несколько не совпадают – в таких случаях необходимо брать среднее число.
Преобразуем уравнения таким образом, чтобы заменить десятичные логарифмы натуральными:
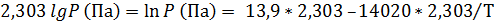
Тв.:
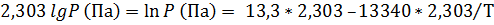
Ж.:
С помощью уравнение Клапейрона – Клаузиуса найдём теплоты испарения и возгонки:


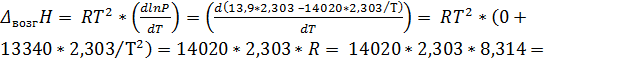 268440
268440 

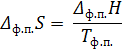

Ответ: TТТ = 1133 К; РТТ = 34 Па; ∆Нпл = 13,02 кДж/моль; ∆Sпл = 11,49 Дж/(моль * К).
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Это важно знать:
Машина для нарезки хлеба. Общая характеристика. Назначение, устройство, принцип действия, правила эксплуатации МРХ-200 Тема 1.7. Машины для нарезки хлеба и гастрономических товаров. Машины для нарезки хлеба. Общая характеристика.
Устройство.
Автоматика безопасности котельной установки. Принцип работы типовой схемы Для автоматизации котлов ДКВР, ДЕ, которые работают на топливе газ/мазут и котлов ТВГ, КВ-Г работающих на природном газе, используют.
Методология и методика научного исследования Научное исследование, его сущность и особенности Одной из главных определяющих целей научной деятельности является получение точных.
Классификация психодиагностических методик Психологическая диагностика (главным образом, на Западе) в настоhttps://studopedia.ru/23_11208_seminar-po-teme-fazovoe-ravnovesie-v-odnokomponentnih-sistemah—.html» target=»_blank»]studopedia.ru[/mask_link]