Для уравнивания химической реакции, введите уравнение реакции и нажмите кнопку Уравнять. Решенное уравнение появится сверху.
- Используйте заглавные символы для начального знака элемента и строчные символы для второго знака. Примеры: Fe, Au, Co, Br, C, O, N, F.
- Ионные заряды пока не поддерживаются и не будут приняты в расчет.
- Переместите неизменные группы в соединениях, чтобы не допустить неопределенность. Например, C6H5C2H5 + O2 = C6H5OH + CO2 + H2O не уравняется, но XC2H5 + O2 = XOH + CO2 + H2O уравняется.
- Промежуточные расстояния [такие, как (s) (aq) или (g)] не требуются.
- Вы можете использовать круглые () и квадратные скобки [].
Примеры
- AgNO3 + (Ag(NH3)2)Br = AgBr + (Ag(NH3)2)NO3
- AgNO3 + (AgNO3)NaOH = Ag2O + NaNO3 + H2O
- AgNO3 + (BO3)3 = Ag3BO3 + NO3
- AgNO3 + (C2O4)2 = Ag2C2O4 + NO3
- AgNO3 + (C6H5)2NH = Ag2NH + C6H5(NO3)
- AgNO3 + (CH3)2CO = Ag + CO2 + NH3 + H2O
- AgNO3 + (CH3)4NI3 = AgI + (CH3)4N + NO3
- AgNO3 + (CH3COO)2Ca = C2H3AgO2 + CaN2O6
- C8H9NO + C3H6O = C11H15NO2
- NaHO2 = NaOH + O5
- Na + N2O + NH3 = N3Na + NaOH + N2
- NaOH(Ac) + CuCl2(Ac) = Cu(OH)2(Ac) + NaCl(Ac)
Калькуляторы
Химическое уравнение
Серебрение Латуни Ляписным карандашом (серебрение нитратом серебра AgNO3) Часть 1
- Программа решения химических уравнений
- Калькулятор стехиометрических реакций
- Калькулятор Лимитирующего реагента
- Ionic Equation Calculator
- окислительно-восстановительные реакции
Источник: www.chemicalaid.com
Для проведения реакции серебряного зеркала используют раствор agno3 ag2o ag аммиачный раствор ag2o
Доказать наличие альдегидной группы в глюкозе можно с помощью аммиачного раствора оксида серебра. К аммиачному раствору оксида серебра добавим раствор глюкозы и подогреем смесь на водяной бане. Вскоре на стенках колбы начинает осаждаться металлическое серебро.
Эта реакция называется реакцией серебряного зеркала. Ее используют как качественную для открытия альдегидов. Альдегидная группа глюкозы окисляется до карбоксильной группы. Глюкоза превращается в глюконовую кислоту.
СН2ОН–(СНОН)4–СОН + Ag2O =
= СН2ОН–(СНОН)4–СООН + 2Ag↓
Реакцию серебряного зеркала используют в промышленности для серебрения зеркал, изготовления колб для термосов, елочных украшений.
Оборудование: колба круглодонная, горелка, стакан, штатив, прокладка огнезащитная.
Техника безопасности. Аммиачный раствор оксида серебра нельзя хранить. После опыта неиспользованный раствор нейтрализуют соляной кислотой.
Постановка опыта и текст – к.п.н. Павел Беспалов

Рубрики: ВИДЕООПЫТЫ
Источник: himija-online.ru
7 Найдите массу серебра, выпавшего на стенках пробирки в виде «серебряного зеркала», при взаимодействии 140 г 10%-го раствора формальдегида с избытком аммиачного раствора оксида серебра. Рассчитайте количество вещества оксида серебра, вступившего в реакци
7 Найдите массу серебра, выпавшего на стенках пробирки в виде «серебряного зеркала», при взаимодействии 140 г 10%-го раствора формальдегида с избытком аммиачного раствора оксида серебра. Рассчитайте количество вещества оксида серебра, вступившего в реакцию.
7. 1) рассчитаем массу вступившего в реакцию формальдегида:
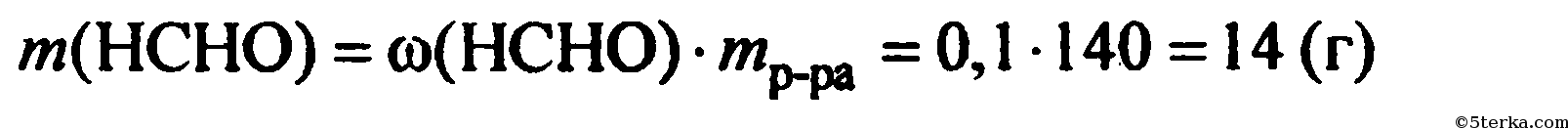
2) Запишем уравнение реакции «серебряного зеркала»
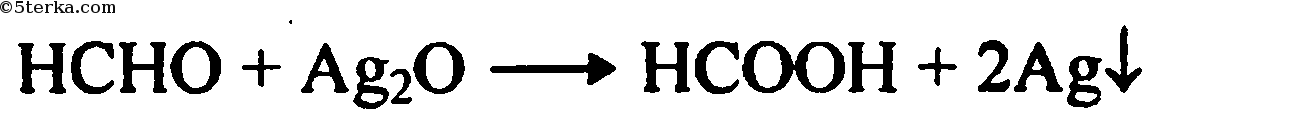
3) Найдем количество вещества формальдегида:
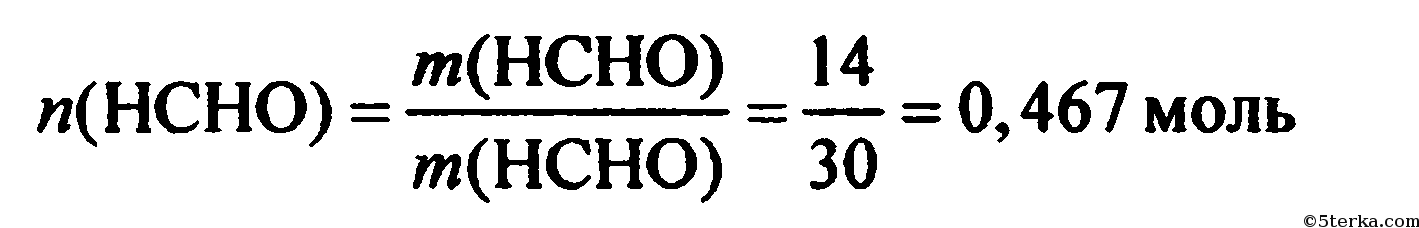
4) Рассчитаем количество вещества серебра и оксида серебра
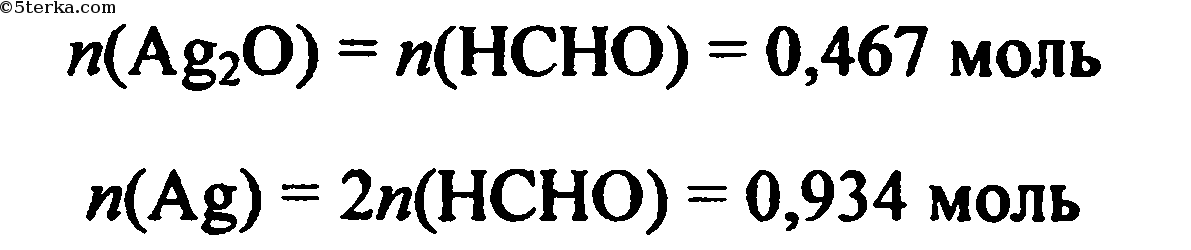
5) Рассчитаем массу серебра
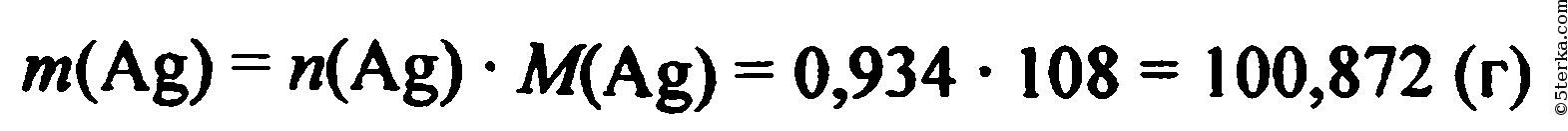
Ответ: 0,467 моль Ag2O, 100,872 Ag.
Источник:

Решебник по химии за 10 класс (О.С. Габриелян, 2011 год),
задача №7
к главе «§ 11 Альдегиды и кетоны».
Источник: 5terka.com