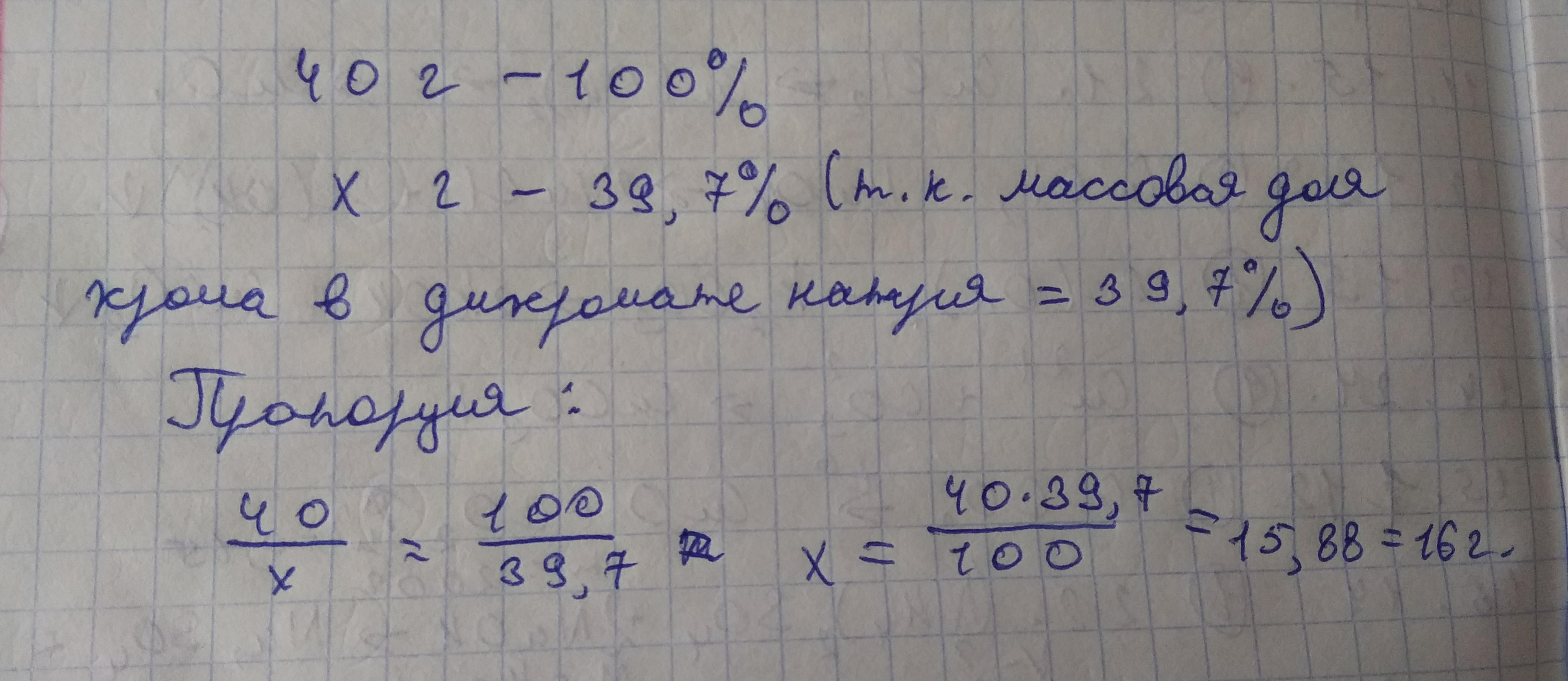
1) так прошел год, по окончании которого с Герасимом случилось не большое происшествие.
2) когда Герасима привезли из деревни, она чуть не обмеров от ужаса при виде его громадной фигуры, всячески старалась не встречаться с ним, даже жмурилась, бывало, когда ей случалось пробегать мимо него, спеша из дома в прачечную.
3) он бросил весла, приник головой к Муму которая сидела перед ним на сухой перекладине.
4)С детства привык он к полевыми работам, к деревенскому быту.
5) Гаврила посмотрел на Копитона и застучал пальцами по косяку окна.
6) Герасим снова взялся за ложку и продолжал хлебать щи.
Источник: sous-otvet.net
Для создания защитного покрытия изделия из серебра погружают в 1 л раствора содержащего 40 г дихрома

Цепи из серебра: ц-РДГ10Б, ц-РДГ10Д, ц-РДГ10, ц-РДГ10р и Браслет б-РДГ10Б
Дихромат натрия (Na2Cr2O7) содержит два атома хрома в каждой молекуле. Молярная масса Na2Cr2O7 равна:
2(молярная масса натрия, Na) + 2(молярная масса хрома, Cr) + 7(молярная масса кислорода, O)
Молярная масса натрия (Na) равна приблизительно 22,99 г/моль. Молярная масса хрома (Cr) равна приблизительно 52 г/моль. Молярная масса кислорода (O) равна приблизительно 16 г/моль.
Таким образом, молярная масса Na2Cr2O7 составляет:
2(22,99 г/моль) + 2(52 г/моль) + 7(16 г/моль) = 2(22,99) + 2(52) + 7(16) = 45,98 + 104 + 112 = 261,98 г/моль
Теперь мы можем рассчитать количество молей дихромата натрия в растворе, зная его массу. Для этого нам нужно разделить массу дихромата натрия на его молярную массу:
Моли Na2Cr2O7 = масса Na2Cr2O7 / молярная масса Na2Cr2O7
Масса Na2Cr2O7 в растворе составляет 40 г. Подставляя значения, получаем:
Моли Na2Cr2O7 = 40 г / 261,98 г/моль
Моли Na2Cr2O7 ≈ 0,152 моль
Так как дихромат натрия содержит два атома хрома в каждой молекуле, количество молей хрома в растворе будет равно:
Количество молей Cr = 2 * Моли Na2Cr2O7
Количество молей Cr = 2 * 0,152 моль
Количество молей Cr ≈ 0,304 моль
Для преобразования количества молей хрома в массу, мы можем умножить его на молярную массу хрома:
Масса Cr = Количество молей Cr * молярная масса Cr
Масса Cr = 0,304 моль * 52 г/моль
Масса Cr ≈ 15,808 г
Таким образом, в 1 литре раствора, содержащего 40 г дихромата натрия, содержится приблизительно 15,808 г хрома.
Источник: uznavalka.pro
Для создания защитного покрытия изделия из серебра погружают в 1 л раствора,
содержащего 40 дихромата натрия. Вычислите, сколько грамм (г) хрома
содержится в таком растворе. Запишите число с точностью до целых.
Задание 19 — Как быстро его решить? | Химия ОГЭ 2023
ответ:
С решением и объяснением

Амети́ст (др.-греч. αμέθυστος, от α- «не» + μέθυστος «быть не пьяным») — синяя, синевато-розовая или красно-фиолетовая разновидность кварца. прозрачный аметист относится к полудрагоценным камням. непрозрачный — ценный поделочный камень. весьма высоко ценится как коллекционный минерал. встречается обычно в виде свободно сидящих в пустотах и жилах среди кристаллических горных пород кристаллов и их сростков. кристаллы образованы комбинацией плоскостей призмы и ромбоэдра, причём из всех кварцев именно для аметиста характерной чертой является преобладание граней ромбоэдра. реже кристаллы имеют длиннопризматический или скипетровидный облик. обычен в друзах и кристаллических щётках внутри агатовых жеод и в миндалинах и трещинах вулканических пород. название аметиста происходит из древнегреческого языка, где означает «не пьяный» или «неопьяняющий» и выражает собою поверие древних, что аметист предохраняет своего владельца от пьянства. красивый фиолетовый или вишнёво-синий цвет аметиста, которым он только и отличается от простого кварца и горного хрусталя, обусловлен не окислов железа и марганца, как думали прежде, а примесью органического красящего вещества[источник не указан 1325 иногда аметист заключает в себе тонкие кристаллические пластинки гематита или игольчатые кристаллики гётита и тогда получает название «волосистого». обычны для кристаллов аметиста, в особенности для крупных, жидкие и газово-жидкие включения; часто они имеют форму тончайших трубок-канальцев с пережимами и располагаются по радиусам от центра роста. естественная смесь аметиста и цитрина называется аметрин.

Ответ разместил:
1. Определяем массу соли в раствор. Принимаем эту массу за а и составляем пропорцию, при этом считаем, что 1 литр раствора равен 1 килограмму раствора:
0,6 кг — 100%, а кг — 40%;
а = (0,6 х 40) : 100;
2. Определяем массу нового раствора. Принимаем ее за а и составляем пропорцию:
0,24 кг — 12%, а кг — 100%;
о,24 : а = 12 : 100;
а = (0,24 х 100) : 12;
3. Определяем сколько воды содержится в новом растворе:
4. Определяем сколько воды первоначально было в растворе:
0,6 — 0,24 = 0,36 кг;
5. Определяем сколько воды нужно добавить в новый раствор:
1,76 — 0,36 = 1,4 кг.
Ответ: 1,4 килограмма воды нужно добавить в раствор.
Источник: otvetovik.com