ОТЛИЧИТЕЛЬНЫЕ ОСОБЕННОСТИ КРИСТАЛЛИЧЕСКИХ И АМОРФНЫХ ТЕЛ
1.3. Отличительные особенности кристаллических и аморфных тел.
1.4. Особые свойства кристаллов.
1.5. Виды связей в кристаллах.
1.6. Силы взаимодействия частиц.
1.7. Кристаллическая решётка. Элементарная ячейка.
1.8. Индексы Миллера.
1.9. Рентгеноструктурный анализ.
КРИСТАЛЛОГРАФИЯ КАК НАУКА
Кристаллография– наука об атомно-молекулярном строении, симметрии, физических свойствах, образовании и росте кристаллов. Как самостоятельная наука существует с середины XVIII века.
Сначала она развивалась как геометрическая кристаллография в тесной связи с минералогией, которая устанавливала закономерности огранки природных кристалликов, имеющих естественную форму правильных многогранников (Р. Гаюи). Затем появилась теория симметрии внешней формы кристаллов (А.В. Гадолини).
Геометрическая кристаллографияопределяет совокупность методов описания кристаллов и закономерности их огранки. В этой теории возникла гипотеза об упорядоченном трёхмерно-периодическом расположении частиц в кристалле с образованием кристаллической решётки (О. Браве, Е.С. Фёдоров, А. Шёнфлис).
Кристаллические решетки минералов
Экспериментальными исследованиями дифракции рентгеновских лучей на кристаллах было подтверждено решёточное строение кристаллов и положено начало структурной кристаллографии(М. Лауэ). В качестве основных структурная кристаллографияиспользует метод рентгеноструктурного анализа, электроно- и нейтронографии, а также методы оптической и электронной спектроскопии. В результате всех исследований к настоящему времени определена структура более 10 5 химических веществ.
Предметом кристаллохимии является изучение законов взаимного расположения атомов и молекул в кристаллах, их химических связей и плотнейших упаковок, а также явлений изо- и полиморфизма.
Кристаллооптика занимается вопросами прохождения света через прозрачные анизотропные кристаллы, сформулировала многие закономерности взаимного влияния симметрии и анизотропии физических свойств.
Кристаллофизикарассматривает в едином русле форму, симметрию и физические свойства кристаллов; занимается вопросами исследования механических, оптических, электрических, магнитных и других свойств кристаллов. В этой части кристаллография смыкается с физикой твёрдого тела.
В кристаллографии изучаются разнообразные дефекты построения идеальной кристаллической решётки: точечные, линейные (дислокации), поверхностные и объёмные. Многие из них появляются в результате роста кристалла или при внешнем воздействии на кристалл напряжением, облучением и т. д.
Для современной кристаллографиихарактерно дальнейшее изучение атомной и дефектной структур кристаллов, процессов их роста, поиск новых свойств и материалов. Основная задача кристаллографии как науки на сегодняшний день – получение новых материалов с важными физическими свойствами. К решению этой задачи необходимо подходить комплексно, рассматривая атомную структуру, анизотропию свойств, взаимодействие кристаллов с окружающей средой в их взаимодействии.
Строение и свойства кристаллических и аморфных тел | Физика 10 класс #37 | Инфоурок
В современной кристаллографии исследуются строение и свойства различных агрегатов из микрокристалликов (поликристаллов, текстур, керамик), а также вещества с атомной упорядоченностью, близкой к кристаллической (жидкокристаллические вещества, полимерные и композиционные материалы).
Симметричные и структурные закономерности, изучаемые в кристаллографии, используются при рассмотрении общих закономерностей строения и свойств аморфных тел и жидкостей, полимеров, квазикристаллов, макромолекул, надмолекулярных аморфно-кристаллических, а также биологических структур. Поэтому современная кристаллография представляет собой обобщённую кристаллографию,математический аппарат которой основан на дискретной геометрии, теории групп, тензорном исчислении и теории преобразований Фурье.
ВИДЫ ТВЕРДЫХ ТЕЛ
Твёрдое телосостоит из большого числа частиц. Этими частицами могут быть атомы, атомные остатки, ионы, молекулы, макромолекулы. Концентрация частиц в твёрдых телах высока: (10 26 – 10 29 ) м -3 . Расстояния между частицами составляют несколько нанометров.
Структуру твёрдых телисследуют дифракционными методами, основанными на дифракции рентгеновских лучей, электронов, нейтронов, используя при этом стандартные установки: рентгеновский дифрактометр, электронный микроскоп, ионный проектор и др. Физика твёрдого тела и кристаллография имеют прямое отношение к нанотехнологиям (рис. 1.1). Нанотехнологии разрабатываются на эффектах, возникающих на уровне атомных размеров.
Свойства твёрдых телобъясняются многими факторами и зависят от химического состава вещества, типа частиц, их внутреннего расположения, типа химической связи между частицами.
Свойства кристаллов широко применяются в оптике, акустике, радиоэлектронике, металловедении, металлургии, химии, медицине. Твёрдые тела встречаются в природе в виде кристаллических и аморфных тел, а также полимеров. В физике к твёрдым телам относят только кристаллические тела.

Рис. 1.1. Электронная микрофотография структуры алмаза вдоль направления [110]
Кристаллы– твёрдые тела, обладающие трёхмерной периодической атомной структурой и имеющие при равновесных условиях образования естественную форму правильных симметричных многогранников. Атомная структура кристалла описывается как совокупность повторяющихся в пространстве одинаковых элементарных ячеек, имеющих форму параллелепипеда.
Кристаллы, выросшие в равновесных условиях, имеют форму правильных многогранников той или иной симметрии. Грани кристалла плоские, а рёбра между гранями — прямолинейные. Выросшие в неравновесных условиях кристаллы не имеют правильной огранки, но сохраняют кристаллическую структуру и все присущие данной структуре свойства. Неравновесные условия кристаллизации приводят к отклонениям только формы от правильного многогранника – к округлости граней и рёбер. Примерами кристаллических тел являются горный хрусталь, поваренная соль, драгоценные камни.
В кристаллахчастицы расположены правильными, симметричными, периодически повторяющимися рядами, сетками, решётками. Кристаллы вырастают в форме многогранников (рис. 1.2). Способность кристалла приобретать конкретную форму – это проявление его физических свойств, определяющихся его структурой, симметрией и химическими связями между его частицами.

Рис. 1.2. Внешний вид кристаллических тел
Кристаллические тела встречаются в природе в виде моно- и поликристаллов. Монокристаллы(большие одиночные кристаллы) получают при создании специальных условий кристаллизации (рис. 1.3).

Рис. 1.3.Монокристаллы кремния
Монокристалл состоит из блоков мозаики,размер которых в монокристалле составляет (10 –6 –10 –8 ) м. Так как кристаллическая решетка в соприкасающихся блоках имеет различную ориентацию, то возникает переходный слой, в котором решетка постепенно переходит от одной ориентации, свойственной одному блоку, к другой ориентации, свойственной другому блоку. Поэтому решетка в этом слое искажена по сравнению с решеткой идеального кристалла. Поликристаллсостоит из беспорядочно ориентированных кристалликов (кристаллитов) малых размеров (рис. 1.2, справа). Размер кристаллитов порядка 10 –4 м.
Аморфные тела– вещества, в атомном строении которых нет порядка: частицы расположены беспорядочно, независимо друг от друга (воск, пластилин). Отличительной особенностью аморфных тел является изотропностьвсех физических и механических свойств.
Полимерысостоят из многочисленных звеньев одинакового химического состава – макромолекул. Например, полимерным материалом является политетрафторэтилен, химическая формула которого (СF2)n, где n = 13.
К особым видам твёрдых тел относятся жидкокристаллические тела,нашедшие широкое применение в телевидении и сотовой связи, и закристаллизованные жидкости,которые обладают особыми свойствами.
ОТЛИЧИТЕЛЬНЫЕ ОСОБЕННОСТИ КРИСТАЛЛИЧЕСКИХ И АМОРФНЫХ ТЕЛ
Рассмотрим некоторые свойства твёрдых тел, которые характеризуют их как кристаллические или аморфные тела.
1. Кристаллыимеютупорядоченное расположение частиц на сколь угоднобольших расстояниях. Частицы расположены в узлах кристаллической решётки.Аморфные тела имеют упорядоченноерасположение частиц на небольших расстояниях (в так называемых группах) (рис.1. 4).
Расположение частиц в веществе характеризуется наличием дальнего и ближнего порядков.
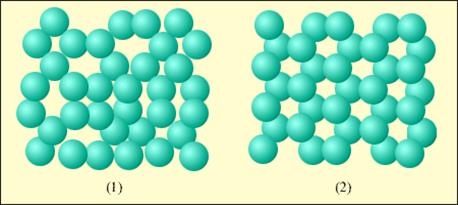
Рис. 1.4. Вещество H2O в двух агрегатных состояниях: воды (1) и льда (2)
2. Дальний порядок– упорядоченное расположение частиц на сколь угодно больших расстояниях от рассматриваемой частицы.
– характеризуется коэффициентом α.
Ближний порядок– упорядоченное расположение частиц на малых расстояниях от рассматриваемой частицы.
– характеризуется коэффициентом β.
| Агрегатное состояние вещества | коэффициент дальнего порядка α | коэффициент ближнего порядка β |
| кристаллические тела | 1 | 1 |
| аморфные тела | < 1 | > 0 |
| жидкости | 1 | |
| газы |
3. Кристаллические и аморфные тела различаются ходом температурной зависимости температуры плавления.
4. Для кристаллов характерно наличие анизотропии. Анизотропия– зависимость свойств вещества от направления в кристалле. Например, слюда по-разному разламывается в различных направлениях. Анизотропией диэлектрической проницаемости объясняется существование в кристаллах турмалина двойного лучепреломления (рис.
1.5).
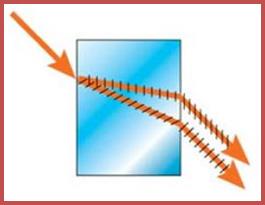
Рис. 1.5. Двойное лучепреломление в кристалле турмалина
Обладают анизотропией очень многие физические и механические свойства кристаллических тел, например: теплопроводность, электропроводность, скорость света, двойное лучепреломление. Аморфные тела изотропны,у них свойства одинаковы по всем направлениям в веществе. Примером является пластилин, который легко сжимается в любых направлениях.
Источник: studopedia.ru
Драгоценные камни аморфные или кристаллические
Мир самоцветов и цветных камней
О камнях – драгоценных, полудрагоценных, поделочных, цветных – написано большое количество научных и научно-популярных трудов.
Камень издревле привлекал внимание человека. Недаром определенный период развития человеческого общества называется каменным веком, т. е. временем, когда камни использовались во всех областях жизни – как орудия труда и войны, на охоте и в быту. Камень был защитником, орудием для нападения, целителем.
Долго был он человеку незаменимым помощником.
Из красивых, блестящих и цветных камней делались украшения. Редкость, красота, необычность, богатство красок и оттенков некоторых из них поражала. Казалось, что радуга подарила камню свои цвета. Камни стали символом магии – талисманами.
Они защищали от злых духов. Сверкающие гранями и богатством красок, драгоценные камни вызывали восторг, удивление, суеверный страх. Желая сохранить себя и быть здоровым, человек призывал на помощь камни. За три тысячи лет до н. э. появились фантастические представления о сверхъестественных силах, которые прошли сквозь все последующие эпохи.
Широко распространившаяся вера в магическую силу драгоценных и цветных камней вошла в повседневный быть человека и никто не мог поставить эту веру под сомнение. Она была непоколебимой.
Люди создали легенды, поверья, мифы о необычных камнях, а самоцветы окружали ореолом таинственности.
В папирусе » О приготовлении лекарств для всех частей тела», написанном за 1400 лет до н. э. упомянуто более десяти минералов, которые использовали для лечения.
Сказочные богатства из драгоценных камней найдены в египетских пирамидах.
В гробнице фараона Тутанхамона, жившего в XUI веке до н. э., хранились алебастровые сосуды, кубок в форме цветка лотоса из полупрозрачного алебастра, трон фараона, инкрустированный цветными камнями, стеклом, фаянсом, золотом. В погребальном покое гробницы был вскрыт кварцитовый саркофаг желтого цвета, перекрытый плитой из розового гранита. Под крышкой саркофага находился гроб, изображавший Тутанхамона. У глаз, выполненных из арагонита и обсидиана, необыкновенно живое выражение. Ювелирные изделия выполнены с использованием драгоценных камней: сердолика, бирюзы, лазурита, халцедона и т. д. Существует мнение, что красота рисунка и уровень исполнения ювелирных изделий гробницы Тутанхамона никогда не были превзойдены.
В четвертом – третьем тысячелетии до н. э. в Месопотамии и на островах Эгейского мора начинает развиваться искусство глиптики. В странах Древнего Востока, а также в Риме изготовляли перстни, которые подчеркивали право собственника на собственность. Камень широко используют для инкрустаций изделий из металла, дерева, слоновой кости и т. д.
Описания драгоценных камней имеются у античного автора Плиния Старшего, жившего в Риме в I веке н. э.
Драгоценные камни украшают одежду царей, королей, богослужебную одежду, оклады икон, дароносицы и т. д.
Перстни с драгоценными камнями на Руси стали носить в XIU веке. С тех пор драгоценные камни стали называть «самоцветами». Множество перстней, ожерелий и иных украшений носили русские цари и царицы.
Присутствовавшие при венчании царя Алексея Михайловича утверждали, что на царице было так много драгоценностей, что ее брачный наряд оказался слишком тяжелым и она была вынуждена переодеться. Такой же тяжелый от драгоценностей наряд был на Анне Иоановне во время ее коронации. Очень любила драгоценности Екатерина II, любил драгоценные камни и князь Потемкин, а последний фаворит Екатерины Платон Зубов носил медальон с миниатюрным портретом императрицы, осыпанный бриллиантами.
Промышленная огранка драгоценных камней на Руси началась по указу Петра Первого. В 1725 году в Петергофе начали строить гранильную фабрику или как тогда ее называли «Алмазную мельницу». Но она сгорела и была восстановлена при Анне Иоановне «для шлифования и полирования при академии наук всяких, найденных в здешнем государстве ясписных и прочих камней». Для обучения русских мастеров огранке из-за границы выписали наставников. При имератрице Екатерине II шлифовальное дело начало развиваться быстрее, были построены новые шлифовальные фабрики и завод в Екатеринбурге и его окрестностях, где изготавливали «для Кабинета Ее Величества » изделий на сумму 20000 рублей.
Промышленная добыча драгоценных камней в России впервые была начата в 1720 году на Урале. И по сей день здесь добывают прекрасные синие топазы, александриты и другие самоцветы. Большим центром добычи алмазов является Якутия. В наши дни добыча драгоценных камней для ювелирных изделий продолжает развиваться.
В разные времена считалось, что драгоценные камни оказывают влияние на счастье, здоровье, характер того, кто им владеет. Так, считалось, что карбункул (гранат-пироп) объединяет друзей, хризолит отводит ночные страхи, коралл охраняет от молний, жемчуг избавляет от меланхолического состояния, гранат веселит сердце, агат поправляет зрение, сардоникс дает покой, топаз усмиряет гнев, бирюза перед смертью своего владельца становится печальной и сгорает, сапфир охраняет целомудрие и способствует хорошему цвету лица.
С давних времен верили в то, что драгоценные камни могут сберечь, обеспечить счастье и отвести возможные несчастья в случае, если человек носит самоцвет, отвечающий месяцу его рождения и знаку Зодиака. Тягу к драгоценным камням испытывали многие поэты и писатели. В.И. Даль рассказывал о том, что перед смертью Александр Сергеевич Пушкин отдал ему свой изумрудный перстень, которым очень дорожил и называл своим талисманом, приписывая ему силу, дарующую талант.
Однажды пораженный богатством цвета, загадочным сверканием граней, человек навсегда становится пленником камня. С этого момента камень восхищает его, переносит его в мир возвышенного, прекрасного, фантастического и реального, постепенно входит в повседневный мир, становится источником вдохновения.
Обработка открыла возможности в выявлении красоты камня. Камень постепенно завоевывает славу материала для украшений. Он находит свое новое назначение используется в ювелирных изделиях. После появления некоторого опыта, человек стал замечать, что одни камни распространены повсеместно, другие встречаются реже, одни обрабатываются легко, другие – с большим усилием или совсем не поддаются обработке. По красоте он разграничил их на ценные и менее ценные.
Драгоценные камни отличали несколько важных достоинств, среди которых главные – красота, долговечность и редкость. Однако чтобы раскрыть красоту и богатство камня, требуется искусство мастера – профессионала или любителя. Тысячи лет искусство обработки камня оставалось под покровом тайны, но теперь многие, пользуясь современными достижениями в области обработки, ставшие общим достоянием, могут стать художниками по камню и исправить его природные недостатки, подчеркнуть красоту, превратить «сырой» материал в ювелирные изделия или другие предметы украшения.
Проникнуть в прекрасный мир камня поможет и умение их искать, собирать, что представляет не только профессиональный интерес для специалистов, но может доставить огромное удовольствие всем любителям камня. Камни разнообразны, красочны, неповторимы. Их коллекционирование доступно всем.
Успешные сборы красивых камней сопряжены с определенным умением, которое приходит с опытом и требует элементарных знаний геологии, горных пород и минералов, наиболее распространенных в окрестностях. Для раскрытия этих и некоторых других тем, и была написана эта книга.
В ней автор попытался представить утверждения и выводы, сделанные учеными, а также познакомить читателя с мифами и легендами о таинственном мире магии драгоценных камней, рассказать о некоторых физических и иных свойствах и характеристиках драгоценных и поделочных камней, рассказать о способах их художественной обработки – огранке, изготовлении кабошонов и т. д. Для любителей истории собраны сведения о некоторых так называемых исторических камнях, о камнерезном искусстве. Самая большая глава книги информирует о символическом, мистическом, магическом значении камней, их целебных свойствах и связи с зодиальными созвездиями.
Источник: и групп направлений с одинаковыми физическими свойствами. При изложении также «забыты» основы теории дислокаций и все подвиды псевдо аморфных тел, среди которых, например, опалы, халцедоны, синтетический ситал и . псевдоаморфные алмазы Попигайской астроблемы с неупорядоченными ковалентными связями, обеспечивающие этим камням твердость вплоть до 12-ти по шкале Мооса. Специфическое строение всех перечисленных псевдоаморфных камней нельзя рассмотреть без теории дальнего и ближнего порядка (группы трансляций). — Это в качестве защиты от сильно ученых критиков этого опуса. =
Татьяна, 05.12.2017
Буду читать и учебники. Постараюсь восполнить пробел в знаниях.
Источник: redkiekamni.ru
1. Различия между аморфными и кристаллическими веществами
Любое вещество может существовать в трёх агрегатных состояниях: твёрдом, жидком и газообразном. Всем известно, что жидкая при комнатной температуре вода становится твёрдой при охлаждении до (0) °С, а при нагревании до (100) °С превращается в пар.
Твёрдые вещества делят на аморфные и кристаллические .
Отличие аморфных и кристаллических веществ заключается в степени упорядоченности их внутреннего строения.
В кристаллических веществах все частицы располагаются в определённом п орядке.
В аморфных веществах этот порядок относительный .

Рис. (1). Строение кристаллических и аморфных веществ
Кристаллическими называют вещества, в которых частицы располагаются в строгом порядке.
Примеры кристаллических веществ: алмаз , сахар , металлы , соли , щёлочи , большинство оксидов и простых веществ .

Рис. (2). Кристаллы льда

Рис. (3). Кристаллы аметиста
Аморфными называют вещества, у которых нет строгого порядка в расположении частиц.
К аморфным веществам относятся: стекло , смола , воск , янтарь , пластилин , жевательная резинка , большинство пластмасс .

Рис. (4). Поделка из пластилина

Рис. (5). Янтарь
Кристаллические и аморфные вещества различаются свойствами .
При ударе кристаллические вещества распадаются на мелкие кристаллики определённой формы.
Аморфные вещества при разрушении образуют осколки неопределённой формы.
Слово «аморфный» переводится с греческого языка как «бесформенный».

Рис. (6). Осколки стекла
Кристаллические вещества имеют определённую температуру плавления , при которой они сразу становятся жидкими. Например, алюминий плавится при температуре (660) °С, а алмаз — при (3827) °С.
Если нагревать стекло, то оно сначала размягчается и превращается в пластичную массу.
Аморфные вещества не имеют точной температуры плавления — при нагревании они постепенно размягчаются и переходят в вязкое состояние. Способность аморфных веществ становиться вязкими при нагревании позволяет придавать им любую форму .
Источник: www.yaklass.ru