Приветствую вас, уважаемые читатели, на своем канале!
В данной статье разберем конкретные примеры задания 4 из ЕГЭ по химии.
В 2022 данное задание не претерпело изменений.
Элементы, проверяемые в данном задании:
— ковалентная химическая связь, её разновидности и механизмы образования;
— характеристики ковалентной связи (полярность и энергия связи);
— вещества молекулярного и немолекулярного строения;
— тип кристаллической решетки;
— зависимость свойств веществ от их состава и строения.
Теорию по данному вопросу можно посмотреть здесь.
Пример 1 (из демонстрационного варианта ЕГЭ 2022)
Из предложенного перечня выберите два вещества молекулярного строения с ковалентной полярной связью.
Веществами молекулярного строения являются вещества с молекулярной кристаллической решеткой.
Веществам с молекулярной кристаллической решеткой характерны следующие признаки:
— газообразное или жидкое агрегатные состояния (иногда — твердое, например: йод, сера, белый фосфор).
Ионная, ковалентная и металлическая связи | Химия. Введение
Давайте разберем варианты ответов:
1) Na2SO4 – вещество ионного строения, так как между ионами Na(+) и SO4(2-) – ионная связь. Данный вариант ответа не подходит.
2) HCOOH – вещество молекулярного строения, так как это жидкость, все связи ковалентные полярные. Этот вариант ответа подходит.
Рисунок 1. Структурная формула муравьиной кислоты
3) CH4 – вещество молекулярного строения, так как это газ, все связи ковалентные полярные. Этот вариант ответа также подходит.
Рисунок 2. Структурная формула метана
4) CaO – вещество ионного строения, так как между атомами Ca и O образуется ионная связь. Данный вариант ответа не подходит.
5) Cl2 – вещество молекулярного строения, так как это газ, но связь ковалентная неполярная между атомами хлора, поэтому данный вариант ответа не подходит.
Пример 2 (авторы: Е.А. Дацук и A.А. Степенин 2022)
Из предложенного перечня веществ выберите два вещества с атомной кристаллической решеткой.
1) карбид кремния
4) кристаллическая сера
Характеристики атомной кристаллической решетки:
— твердые вещества (горные породы);
Примеры веществ: С (алмаз, графит); Si (кремний); SiO2 (кварц, кремнезем, горный хрусталь); SiC(карборунд); Al2O3 (наждак, корунд, рубин, сапфир); P фосфор красный и др.
1) Карбид кремния (SiC) или карборунд — твердое вещество с ковалентной полярной связью. Характерна атомная кристаллическая решетка. Данный ответ подходит.
2) Цинк (Zn) – вещество с металлической связью. Не подходит.
3) Силан (SiH4) – газообразное вещество с ковалентными полярными связями, молекулярная кристаллическая решетка. Не подходит.
4) Кристаллическая сера (S6) – твердое вещество с ковалентными неполярными связями, но с молекулярной кристаллической решеткой. Не подходит.
5) Графит (С) – твердое вещество с ковалентными неполярными связями, атомная кристаллическая решетка. Подходит.
Графит
Пример 3 (авторы: Е.А. Дацук и A.А. Степенин 2022)
Из предложенного перечня выберите два вещества ионного строения, в которых присутствует связь, образованная по донорно-акцепторному механизму.
1) азотная кислота
2) хлорид аммония
3) тетрагидроксоцинкат калия
4) ацетат натрия
По донорно-акцепторному механизму образуются связи в ионах гидроксония H3O(+), аммония NH4(+), фосфония PH4(+); комплексных соединениях, например Na[Al(OH)4]; азотной кислоте HNO3 и ее солях, угарном газе CO, озоне O3, солях аминов.
Из данного перечня подходят три варианта: азотная кислота, хлорид аммония и тетрагидроксоцинкат калия.
Из данных трех ответов к веществам ионного строения можно отнести: хлорид аммония и тетрагидроксоцинкат калия.
Хлорид аммония (NH4Cl) – ионная связь образуется между ионами NH4(+) и Cl(-). В ионе NH4(+) имеется связь, образованная по донорно-акцепторному механизму.
Источник: dzen.ru
4.5.1. Графит
Графит – это материал состоящий из атомов углерода С, которые образуют слоистый кристалл (Рис.56.). Четыре электрона на внешней оболочке углерода образуют три ковалентные связи и одну металлическую. Прочные ковалентные связи объединяют атомы в атомные плоскости. Вследствие этого прочность кристалла графита вдоль этих атомных плоскостей очень высокая.
Между собой атомные плоскости связаны слабыми Ван-дер-ваальсовыми силами. Отсюда прочность графита перпендикулярно атомным плоскостям весьма малая. Одна металлическая связь придает ему хорошую электропроводность.

Рис.56. Строение кристалла графита.
акое необычное строение кристалла приводит к очень интересным сочетаниям свойств графита. Он сильно анизотропен: длина ковалентной связи 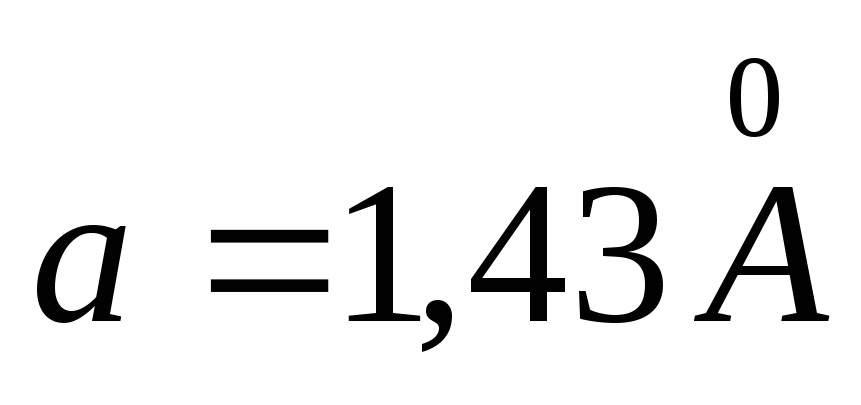 , а расстояние между атомными плоскостями намного больше и составляет
, а расстояние между атомными плоскостями намного больше и составляет  . Вследствие прочности ковалентных связей температура плавления графита чрезвычайно высока
. Вследствие прочности ковалентных связей температура плавления графита чрезвычайно высока 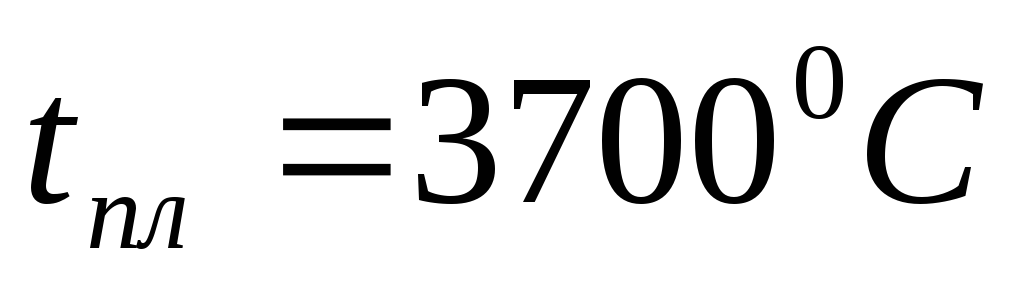 . Графит является абсолютным рекордсменом термостойкости среди всех существующих материалов. Слоистая структура графита и слабая связь между соседними плоскостями обусловливают анизотропию всех физических свойств кристаллов графита во взаимно перпендикулярных направлениях.
. Графит является абсолютным рекордсменом термостойкости среди всех существующих материалов. Слоистая структура графита и слабая связь между соседними плоскостями обусловливают анизотропию всех физических свойств кристаллов графита во взаимно перпендикулярных направлениях.
Графит встречается в природе в естественном виде, а также получается искусственным путем (технический и пиролитический графит). Потребительские качества природного графита невысоки, он содержит много примесей, порист, непрочен, его свойства почти изотропны. Используется только в качестве антифрикционного материала.
Более чистый технический графит получают из нефтяного кокса и каменноугольного пека при нагреве до температуры  . Степень анизотропии его свойств достигает значения 3:1. Ещё более качественный графит получают в результате реакции пиролиза углеводородов (метана).
. Степень анизотропии его свойств достигает значения 3:1. Ещё более качественный графит получают в результате реакции пиролиза углеводородов (метана).
Атомы углерода осаждаются на нагретых до температуры  поверхностях, изготовленных из технического графита или керамики. После охлаждения и кристаллизации получается пиролитический графит. В этом случае степень анизотропии свойств достигает значения 100:1 и более. Его свойства приведены в табл.12.
поверхностях, изготовленных из технического графита или керамики. После охлаждения и кристаллизации получается пиролитический графит. В этом случае степень анизотропии свойств достигает значения 100:1 и более. Его свойства приведены в табл.12.
Табл.12. Свойства пиролитического графита
Источник: studfile.net
ОГЭ по химии. Разбор задания № 5
Химия ОГЭ 2020, часть 1. Задание 5 с комментариями экспертов (разбор задания № 5 на 3 примерах). Материал для подготовки к экзамену.
СОДЕРЖАНИЕ (быстрый переход по клику) Скрыть
ОГЭ по химии. Разбор задания № 5
Ответами к заданиям 1–19 являются цифра или последовательность цифр.
Пример 1.
ОГЭ по химии. Задание 5
Из предложенного перечня выберите вещество, имеющее два типа связи.
- 1) оксид кремния
- 2) бромид калия
- 3) сероводород
- 4) пероксид натрия
Решение задания (с комментариями)
Базовые знания. Ионная связь образуется между противоположно заряженными ионами. Она возникает между катионами металлов (или катионами аммония NH4 + ) и простыми или сложными анионами (Сl – , О2 – , S2 – , ОН – , SO4 2– …). Ковалентная неполярная связь образуется между атомами одинаковых неметаллов.
Ковалентная полярная связь возникает между атомами различных неметаллов в сложных веществах (химических соединениях). Металлы образуются в результате объединения атомов металлов с помощью металлической связи. К металлам относят все элементы побочных подгрупп и элементы главных подгрупп, расположенные ниже условной линии, проведённой от бора (второй период, III группа) к астату (шестой период, главная подгруппа VII группы).
Вывод: необходимо определить положение элементов, входящих в соединение, в Периодической системе химических элементов Д.И. Менделеева, классифицировать их на металлы и неметаллы и определить тип химической связи между этими элементами.
1) Оксид кремния SiO2 состоит из атомов кремния и кислорода.
Кремний (Si) находится в главной подгруппе IV группы третьего периода, неметалл; кислород (О) находится в главной подгруппе VI группы второго периода, неметалл.
Вывод: вещество образовано двумя различными неметаллами (неМе(1)–неМе(2)), в SiO2 – связь ковалентная полярная. Ответ неверный.
2) Бромид калия КВr состоит из калия и брома.
Калий (К) находится в главной подгруппе I группы четвёртого периода, металл; бром (Вг) находится в главной подгруппе VII группы четвёртого периода, неметалл.
Вывод: вещество образовано металлом и неметаллом (М + не М – ), связь в КВr – ионная. Ответ неверный.
3) Сероводород H2S состоит из атомов водорода и серы.
Водород (Н) находится в главной подгруппе I группы первого периода, неметалл; сера (S) находится в главной подгруппе VI группы третьего периода, неметалл.
Вывод: вещество образовано двумя различными неметаллами (неМе(1)–неМе(2)), в H2S – связь ковалентная полярная. Ответ неверный.
4) Пероксид натрия Na2O2 состоит из атомов натрия и кислорода.
Натрий (Na) находится в главной подгруппе I группы третьего периода, металл; кислород (О) находится в главной подгруппе VI группы второго периода, неметалл.
Вывод: в соединении имеется два типа связи. Между катионами натрия (Na + ) и анионами кислорода (O2 2– ) – связь ионная (ответ правильный). Между атомами кислорода – связь ковалентная неполярная (связь между атомами с одинаковой электроотрицательностью).
Ответ: 1, 4.
Пример 2.
ОГЭ по химии. Задание 5
Какой вид химической связи в молекуле аммиака?
- 1) ковалентная неполярная
- 2) ковалентная полярная
- 3) металлическая
- 4) ионная
Решение задания (с комментариями)
Простые вещества – неметаллы образуются с помощью ковалентной неполярной связи. Компактные металлы образуются в результате возникновения металлической связи. В сложных веществах между атомами неметаллов могут возникать как полярные, если соединяются различные атомы, так и неполярные, между одинаковыми атомами, ковалентные связи. Между атомами типичных металлов и типичных неметаллов возникают ионные связи. Ионные связи имеются также в солях аммония.
Вывод: надо написать формулу аммиака и определить, между какими атомами имеются химические связи, и тип этих связей.
Формула аммиака NH3.
Элемент азот 7N находится в главной подгруппе V группы второго периода, неметалл.Элемент водород 1Н находится в главной подгруппе I группы первого периода, неметалл.
Вывод: связь между атомами N и Н – ковалентная полярная.
Ответ: 2.
Пример 3.
ОГЭ по химии. Задание 5
Одинаковый вид химической связи имеют графит и
- 1) медь
- 2) бромоводород
- 3) сера
- 4) аммиак
Решение задания (с комментариями)
Графит – простое вещество, образованное углеродом. Углерод – неметалл, связи в графите – ковалентные неполярные. Вывод: среди предложенных веществ необходимо определить простое вещество, образованное неметаллом.
1) Медь – металл. Вывод: ответ неверный.
2) Бромоводород НВг – сложное вещество, образованное атомами элементов–неметаллов, связь в молекуле ковалентная полярная. Вывод: ответ неверный.
3) Сера – простое вещество, образованное элементом–неметаллом. Связи – ковалентные неполярные. Вывод: правильный ответ найден, оставшийся вариант рассматривать не будем.
Ответ: 3.
Вы смотрели: Химия ОГЭ 2020, часть 1. Задание 5 с комментариями (разбор задания на трех примерах). Материал для подготовки к экзамену.
Источник: ogevip.ru