Имеется следующий перечень химических веществ: железо, нитрат серебра, серебро, нитрат железа(II), гидроксид кальция, карбонат натрия, карбонат кальция, гидроксид натрия. Используя этот перечень, выполните задания 6.1–6.5. 6.1.
Напишите химические формулы каждого из указанных веществ.
Железо – ____. Нитрат серебра – _____. Нитрат железа(II) – ____________________.
Гидроксид кальция – _______________. Карбонат натрия – _____________________.
Карбонат кальция – ________________. Гидроксид натрия – ______. Серебро – ____.
6.2. Какое из веществ, упоминаемых в перечне, соответствует следующему описанию: «Ковкий пластичный благородный металл серебристо-белого цвета, применяемый в ювелирном деле»?
6.3. Из данного перечня выберите ЛЮБОЕ СЛОЖНОЕ вещество. Запишите химическую формулу этого вещества и укажите, к какому классу неорганических соединений оно относится.
Вещество –_________________________. Класс соединений – ____________________.
6.4. Из приведённого перечня веществ выберите ЛЮБОЕ ХОРОШО РАСТВОРИМОЕ соединение, состоящее из атомов ТРЁХ элементов. Вычислите массовую долю кислорода в этом соединении.
6.5. Вычислите массу 0,25 моль карбоната кальция.
Подобные задания можно добавить в готовый типовой вариант и получить свой уникальный КИМ с ответами и критериями.
ESUO | Единая система универсального образования
Сайт является информационным ресурсом и создан в ознакомительных целях. Все задания формируются из открытых источников сети интернет и из образовательных ресурсов Министерства образования РФ и ФИПИ.
Мы не храним у себя варианты и не предоставляем официальные КИМы на Государственную итоговую аттестацию. Оплата производится только за функцию конструктора готовых уникальных вариантов.
Источник: esuo.ru
Нитрат железа (III)

Нитрат железа (III) — неорганическое химическое соединение, соль азотной кислоты и трехвалентного железа.

Физические свойства
При обычной температуре в зависимости от концентрации и содержания в растворе кислоты нитрат железа (III) кристаллизуется в виде почти бесцветных кубиков, имеющих состав Fe(NO3)3·6H2O, или в моноклинных кристаллах состава Fe(NO3)3·9H2O.
Нонагидрат нитрата железа (III) Fe(NO3)3·9H2O — очень гигроскопичные светло-фиолетовые кристаллы с моноклинной решёткой (a = 0,140 нм, b = 0,970 нм, c = 1,103 нм, β=95,52°, пространственная группа P21/с). Хорошо растворяются в воде. При нагревании плавится при 50,1 °C. Процесс сопровождается частичным разложением исходного продукта с выделением HNO3 и последующим кипячением раствора при 125 °C.
Таблица растворимости нитрата железа (III) в воде (в пересчете на безводную соль):
| Температура, °С | Концентрация, г/100 г воды | Концентрация, % |
| 67,08 | 40,15 | |
| 20 | 82,48 | 45,2 |
| 40 | 104,83 | 51,18 |
Растворяется также в ацетоне, эфире, этаноле.
Безводный нитрат железа (III) получить не удалось.
В растворе бледно-фиолетовый гексааквакатион [Fe(H2O)6] 3+ преобладает только в том случае, если pH~0. При более высоких значениях pH раствор желтеет из-за гидролиза, а если pH выше 2-3, происходит дальнейшая конденсация и начинается образование коллоидных гелей, и в конечном итоге образуется красновато-коричневый осадок гидратированного оксида железа (III).

Получение
- Нитрат железа (III) получают взаимодействием железной стружки с 20-30 % раствором азотной кислоты:
- В производстве этот процесс проводят, продувая через раствор воздух:
- В лабораторной практике нитрат железа (III) можно получить обменной реакцией:
- Добавив к гидроксонитрату церия (IV) азотную кислоту и сульфат железа (II), получим следующие продукты реакции:
Химические свойства
- В водных растворах нитрат железа (III) подвергается сильному гидролизу:
Равновесие можно сместить в обратную сторону сильно подкислив раствор HNO3.
— Выступает в роли окислителя с металлами, например, с медью:
Применение
- Применяется как коагулянт при очистке сточных вод.
- При окраске тканей и шерсти используют нитрат железа (III) как протраву.
- Нитрат железа(III) является катализатором для синтеза амида натрия из раствора натрия в аммиаке:
- Некоторые глины, пропитанные нитратом железа (III), являются полезными окислителями в органическом синтезе.
- Используется ювелирами и кузнецами для протравки серебра и его сплавов.
Соединения железа
- Алюминат железа II ( Fe(AlO2)2 ) Алюминат железа II
- Арсенат железа II (Fe3(AsO4)2) Железо мышьяковокислое
- Арсенат железа III (FeAsO4) Мышьяковокислое железо
- Ацетат железа II (Fe(CH3COO)2) Железо уксуснокислое
- Ацетат железа III (Fe(CH3COO)3) Уксуснокислое железо
- Берлинская лазурь () Прусская Синь
- Бромид железа II (FeBr2) Бромистое железо
- Бромид железа III (FeBr3) Трибромид железа
- Бромид железа II,III (Fe3Br8) Железо бромистое
- Ванадат железа III (FeVO4) Железо ванадиевокислое
- Вольфрамат железа II (FeWO4) Железо вольфрамовокислое
- Гексаплутонийжелезо (FePu6) Гексаплутонийжелезо
- Гексахлороплатинат IV железа (Fe[PtCl6]) Гексахлороплатеат железа
- Гексацианоферрат II железа II (Fe2[Fe(CN)6]) Гексацианоферрат железа II
- Гексацианоферрат II железа III (Fe4[Fe(CN)6]3) Гексацианоферрат железа III
- Гексацианоферрат III железа II,III (Fe III 4Fe II 3[Fe(CN)6]6) Гексацианоферрат железа II,III
- Гексацианоферрат III железа II (Fe3[Fe(CN)6]2) Турнбулева синь
- Гексацианоферрат II калия (K4[Fe(CN)6]) Желтая кровяная соль
- Гексацианоферрат III калия (K3[Fe(CN)6]) Красная кровяная соль
- Гидроксид железа II (Fe(OH)2) Гидроксид железа II
- Гидроксид железа III (Fe(OH)3) Гидроксид железа III
- Динитрозилдикарбонилжелезо (Fe(CO)2(NO)2) Динитрозилдикарбонилжелезо
- Дипразеодимгептадекажелезо (Fe17Pr2) Гептадекажелезодипразеодим
- Диренийтрижелезо (Fe3Re2) Трижелезодирений
- Дисамарийгептадекажелезо (Fe17Sm2) Гептадекажелезодисамарий
- Диселенид железа (FeSe2) Железо селенистое
- Дисилицид железа (FeSi2) Железо кремнистое
- Дистаннид железа (FeSn2) Дистаннид железа
- Дистаннид трижелеза (Fe3Sn2) Дистаннид трижелеза
- Дисульфид железа II (FeS2) Дисульфид железа
- Дителлурид железа (FeTe2) Дителлурид железа
- Дихромат железа III (Fe2(Cr2O7)3) Хромовокислое железо
- Додекакарбонилтрижелезо (Fe3(CO)12) Додекакарбонилтрижелезо
- Железо (Fe)
- Железистосинеродистая кислота (H4[Fe(CN)6]) Кислота железистосинеродистая
- Железониобий (FeNb) Железониобий
- Железосинеродистая кислота (H3[Fe(CN)6]) Кислота железосинеродистая
- Йодид железа II,III (Fe3I8) Йодистое железо
- Йодид железа II (FeI2) Железо йодистое
- Карбонат железа II (FeCO3) Железо углекислое
- Лактат железа II (Fe(C3H5O3)2) Железо молочнокислое
- Лактат железа III (Fe(C3H5O3)3) Молочнокислое железо
- Метаванадат железа III (Fe(VO3)3) Ванадиевокислое железо
- Метагидроксид железа (FeO(OH)) Железо метагидроксид
- Молибдат железа II (FeMoO4) Железо молибденовокислое
- Нитрат железа II (Fe(NO3)2) Железо азотнокислое
- Нитрат железа III (Fe(NO3)3) Азотнокислое железо
- Нитрид дижелеза (Fe2N) Железо азотистое
- Оксалат железа II (FeC2O4) Железо щавелевокислое
- Оксид железа II (FeO) Оксид железа
- Оксид железа III (Fe2O3) Окись железа ( Железный сурик )
- Оксид железа II,III (Fe3O4) Закись-окись железа
- Оксихлорид железа (FeOCl) Оксид-хлорид железа
- Пентакарбонилжелезо ([Fe(CO)5]) Пентакарбонил железа
- Перхлорат железа II (Fe(ClO4)2) Железо хлорнокислое
- Пирофосфат железа III (Fe4(P2O7)3) Железо пирофосфорнокислое
- Пирофосфат железа III-натрия (FeNaP2O7) Фосфорнокислое железо-натрий
- Платинажелезо (FePt) Железоплатина
- Плутонийдижелезо (Fe2Pu) Плутонийдижелезо
- Празеодимдижелезо (Fe2Pr) Дижелезопразеодим
- Ржавчина
- Самарийдижелезо (Fe2Sm) Дижелезосамарий
- Самарийпентажелезо (Fe5Sm) Пентажелезосамарий
- Самарийтрижелезо (Fe3Sm) Трижелезосамарий
- Селенид железа II (FeSe) Селенистое железо
- Силикат железа II (FeSiO3) Железо кремнекислое
- Силицид дижелеза (Fe2Si) Кремнистое железо
- Силицид железа (FeSi)
- Соль Мора (FeSO4·(NH4)2SO4·6H2O) Сульфат аммония-железа II
- Станнид железа (FeSn)
- Станнид трижелеза (Fe3Sn)
- Сульфат железа (FeSO4) Железо сернокислое (Железный купорос)
- Сульфат железа II-калия (K2Fe(SO4)2) Сернокислое железо-калий
- Сульфат железа III (Fe2(SO4)3) Железо сернокислое III
- Сульфат железа III-аммония (NH4Fe(SO4)2·12H2O) Сернокислое железо-аммоний
- Сульфат железа III-калия (KFe(SO4)2) Сернокислое железо-калий
- Сульфид железа II,III (Fe3S4)
- Сульфид железа II (FeS)
- Сульфид железа II-меди II (CuFeS2)
- Сульфид железа III (Fe2S3)
- Сульфид железа III-калия (KFeS2) Сернистое железо-калий
- Сульфит железа II (FeSO3) Железо сернистокислое
- Танталат железа II (Fe(TaO3)2) Железо танталовокислое
- Тартрат железа II (FeC4H4O6) Железо виннокислое
- Теллурид железа II (FeTe) Железо теллуристое
- Теллурид железа III (Fe2Te3) Теллуристое железо
- Тетракарбонилдигидриджелезо (H2Fe(CO)4)
- Тетракарбонилжелезо (Fe(CO)4) Тетракарбонил железа
- Тиосульфат железа II (FeSO3S) Тиосернокислое железо
- Тиоцианат железа II (Fe(SCN)2) Железо роданистое
- Тиоцианат железа III (Fe(SCN)3) Тиоциановокислое железо
- Титанат железа II (FeTiO3) Титановокислое железо
- Триренийдижелезо (Fe2Re3) Дижелезотрирений
- Формиат железа III (Fe(CHO2)3) Железо муравьинокислое
- Фосфат железа II (Fe3(PO4)2) Железо фосфорнокислое
- Фосфат железа III (FePO4) Фосфорнокислое железо
- Фосфинат железа III (Fe(PH2O2)3) Железо фосфорноватистокислое ( гипофосфит железа )
- Фторид железа II (FeF2) Железо фтористое
- Фторид железа III (FeF3) Фтористое железо
- Хлорид железо II (FeCl2) Железо двухлористое
- Хлорид железа III (FeCl3) Железо треххлористое
- Хлорид железа II,III (Fe3Cl8) Хлористое железо II,III
- Хлорид железа III-калия (FeCl3•2KCl•H2O) Хлористое железо-калий
- Хромат железа III (Fe2(CrO4)3) Железо хромовокислое
- Хромит железа II (Fe(СrO2)2) тетраоксид железа-дихрома
- Цианид железа II (Fe(CN)2) Железо цианистое
- Цитрат железа II (FeC6H6O7) Железо лимоннокислое
- Цитрат железа III (FeC6H5O7) Лимоннокислое железо
- Цитрат железа III-аммония (Fe(NH4)3(C6H5O7)2) Лимоннокислое железо-аммоний
Источник: chem.ru
Задание с ответами: химия. ЕГЭ — 2018
Для выполнения задания используйте следующий перечень веществ: хлорид железа (III), медь, нитрат бария, серная кислота, уксусная кислота. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Сведения для решения
Для начала запишем молекулярные формулы данных веществ: 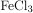 ,
,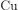 ,
, 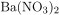 ,
, 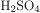 ,
, 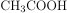 .
.
Условия реакций ионного обмена (РИО):
1) Растворимость реагирующих веществ:
Кислота + Основание. Растворим хотя бы 1 из реагентов
Кислота + Соль. Обязательно растворима должна быть кислота
Основание + Соль. Растворимы оба реагента
Соль + Соль. Должны быть обе растворимы
2) В ходе реакции должны образоваться осадок, газ или вода.
Медь — простое вещество, в реакции обмена не вступает.
Хлорид железа (III) — растворимая соль, с нитратом бария и серной кислотой образует растворимые продукты, с уксусной кислотой идет реакция совместного гидролиза.
Нитрат бария — растворимая соль, при взаимодействии с уксусной кислотой образует растворимые продукты, а с серной кислотой — осадок сульфата бария.
Серная кислота — с уксусной кислотой в РИО не вступает.
Первый вариант ответа:
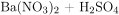 →
→ 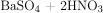
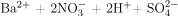 →
→ 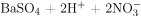
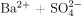 →
→ 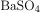
Второй вариант ответа:
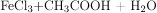 →
→ 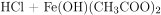 ↓
↓
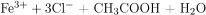 →
→ 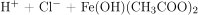 ↓
↓
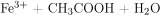 →
→ 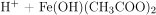 ↓
↓
Источник: vuz-24.ru