К элементам группы 1А относятся литий, натрий, калий, рубидий, цезий, франций.
Все металлы серебристого цвета, кроме цезия (желтый). Относятся к легким
металлам. Очень мягкие – режутся ножом. Все щелочные металлы сильные
восстановители. Реакционная способность возрастает в ряду литий – цезий. Самым
активным является цезий, т. к. у него самый низкий потенциал ионизации.
Щелочные металлы энергично реагируют с большинством неметаллов, разлагают воду,
бурно реагируют с растворами кислот. Комплексообразование для щелочных металлов
не характерно. В природе в свободном виде не встречаются ввиду их чрезвычайной
активности. Литий существенно отличается от остальных элементов группы: он не
имеет р-орбиталей. По ряду свойств он ближе к магнию, чем к щелочным металлам.
Наиболее промышленно важные металлы – это калий и натрий. Основные природные
соединения этих металлов – поваренная соль (NaCl), мирабилит (Na2SO
4·10H2O), сильвинит (NaCl·KCl), сильвин (KCl), ортоклаз
Химия 9 класс (Урок№23 — Щелочные металлы. Физические и химические свойства. Оксиды и гидроксиды.)
Основные способы получения – электролиз расплавов их солей в смеси с KCl, CaCl
2 (натрий) и NaCl (калий). Применяется также восстановление их оксидов,
хлоридов, карбонатов алюминием, кремнием, кальцием, магнием при нагревании в
1. С простыми веществами:
2) 2Э + Hal2 → 2ЭHal
2. Со сложными веществами:
1) 2Э + 2HCl(p) → 2ЭCl + H2
Щелочные металлы и их соединения – важнейшие компоненты различных химических
производств. Они используются в металлотермическом производстве различных
металлов, таких как Ti, Zr, Nb, Ta. Соединения натрия и калия находят
применение в мыловарении (Na2CO3), производстве стекла
4, Li2O), используются для отбелки и дезинфекции (Na2
O2), в качестве удобрений (KCl, KNO3). Из поваренной соли
получают многие важные химические соединения: Na2CO3,
Калий улучшает водный режим растений, способствует обмену веществ
и образованию углеводов, повышает морозо- и засухоустойчивость. Содержание
калия выражается в пересчете на К2О. Стандартным считается
удобрение, содержащее 41,6% К2О. Важнейшими калийными удобрениями
являются хлорид и сульфат калия. Хлорид калия содержит 50-60% К
2О и его получают из минералов, используя его особую растворимость.
Сульфат калия содержит 45-52% К2О и получается следующим образом:
Источник: studopedia.ru
К какому типу элементов относятся щелочные и щелочноземельные металлы?



- 29 May 2021
- Ответ оставил: OosvaldD
Щелочные и щелочноземельные металлы относятся к s-элементам
Нравится —> 0
Щелочные металлы. Видеоурок 14. Химия 9 класс
- НЕ НАШЛИ ОТВЕТ?
Если вас не устраивает ответ или его нет, то попробуйте воспользоваться поиском на сайте и найти похожие ответы по предмету школьной программы: химия.
На сегодняшний день (02.07.2023) наш сайт содержит 16352 вопросов, по теме: химия. Возможно среди них вы найдете подходящий ответ на свой вопрос.
Нажимая на кнопку «Ответить на вопрос», я даю согласие на обработку персональных данных
Ответить на вопрос
Последние опубликованные вопросы
Источник: edubirdie.pro
Готовимся к углубленному изучению химии
В периодической системе элементов металлы в основном располагаются в главных подгруппах I—Ill групп, а также в побочных подгруппах.
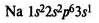
В IA группе у атомов элементов на внешнем энергетическом уровне находится 1 электрон в состоянии s 1 , во IIA группе у атомов на внешнем ЭУ 2 электрона в состоянии s 2 . Эти элементы относятся к s-элементам. В IIIA группе у всех элементов на внешнем ЭУ 3 электрона в состоянии s 2 p 1 . Они относятся к p-элементам.
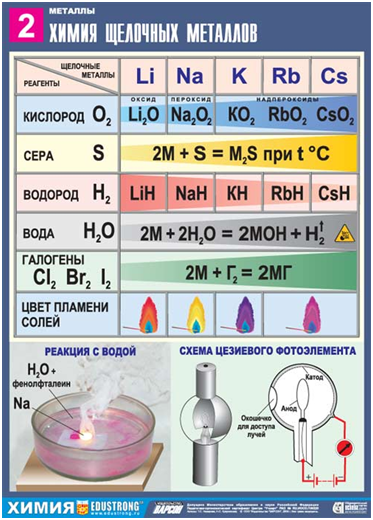
В IA группу входят щелочные металлы Li, Na, K, Rb, Cs, Fr, активность которых при движении сверху вниз увеличивается вследствие увеличения радиуса атомов, металлические свойства возрастают также, как и у щелочеземельных металлов IIA группы Be, Mg, Ca, Sr, Ba, Ra и металлов IIIA группы Al, Ga, In, Tl.
Оксиды типа R2O характерны только для Li, для всех остальных щелочных металлов характерны пероксиды R2O2, которые являются сильными окислителями.
Все металлы этих групп образуют основные оксиды и гидроксиды, кроме Be и Al, которые проявляют амфотерные свойства.
Физические свойства
В свободном состоянии все металлы – серебристо-белые вещества. Магний и щелочноземельные металлы – ковкие и пластичные, довольно мягкие, хотя тверже щелочных. Бериллий отличается значительной твердостью и хрупкостью, барий при резком ударе раскалывается.
В кристаллическом состоянии при обычных условиях бериллий и магний имеют гексагональную кристаллическую решетку, кальций, стронций – кубическую гранецентрированную кристаллическую решетку, барий – кубическую объемоцентрированную кристаллическую решетку с металлическим типом химической связи, что обуславливает их высокую тепло- и электропроводность.
Металлы имеют температуры плавления и кипения выше, чем у щелочных металлов, причем с увеличением порядкового номера элемента температура плавления металла изменяется немонотонно, что связано с изменением типа кристаллической решетки.
Бериллий и магний покрыты прочной оксидной пленкой и не изменяются на воздухе. Щелочноземельные металлы очень активны, их хранят в запаянных ампулах, под слоем вазелинового масла или керосина.
Источник: himiy88.blogspot.com