⭐⭐⭐⭐⭐ Лучший ответ на вопрос «1.Выберите группу элементов, в которой находятся только металлы: А) Al, As, P; Б) Mg, Ca, Si; В) K, Ca, Pb 2. Выберите группу, в которой находятся только простые вещества – неметаллы: А) K2O, SO2, SiO2; Б) H2, Cl2, I2 ; В)Ca, Ba, HCl; 3. Укажите общее в строении атомов K и Li: А) 2 электрона на последнем электронном слое; Б) 1 электрон на последнем электронном слое; В) одинаковое число электронных слоев. 4. Металлический кальций проявляет свойства: А) окислителя; Б) восстановителя; В) окислителя или восстановителя в зависимости от условий.
5. Металлические свойства натрия слабее, чем у – А) магния; Б) калия; В) лития. 6. К неактивным металлам относятся: А) алюминий, медь, цинк; Б) ртуть, серебро, медь; В) кальций, бериллий, серебро. 7. Какое физическое свойство не является общими для всех металлов: А) электропроводность, Б) теплопроводность, В) твердое агрегатное состояние при нормальных условиях, Г) металлический блеск» от пользователя Наталья Костюченко в разделе Химия. Задавайте вопросы и делитесь своими знаниями.
Всего одна трава выводит 80% тяжёлых металлов из организма
Открой этот вопрос на телефоне — включи камеру и наведи на QR-код!
Источник: shpora.org
Химические свойства металлов. Ряд напряжения металлов
Цели урока: расширить и углубить знания учащихся о характеристике химических элементов и образуемых ими простых веществ на примере металлов I-III групп главных подгрупп; уметь давать общую характеристику металлов I-IIIгрупп главных подгрупп в сравнении на основании положения в периодической системе и строения атомов.
1. Организационный момент урока.
2. Изучение нового материала
Общие химические свойства металлов представлены в таблице:
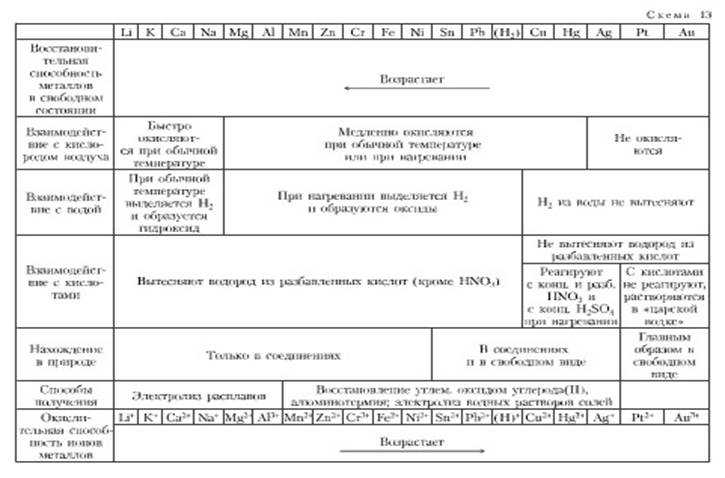
1). Металлы по-разному реагируют с водой:
Алюминий реагирует с водой подобно активным металлам, образуя основание:
2Al + 6H2O = 2Al(OH)3 + 3H2↑
2). Металлы особо реагируют с серной концентрированной и азотной кислотами:
H2SO4 (конц.) + Me = соль + H2O + Х
Металлы до водорода Сd-Pb
могут S↓ или SO2↑
1) пассивируются на холоде;
2) при нагревании → SO2↑
могут H2S илиSO2
H2SO4 (разб) + Zn = ZnSO4 + H2↑
2H2SO4 (конц.) + Cu = CuSO4 + 2H2O + SO2↑
Pt, Au + H2SO4 (конц.) → реакции нет
Al, Fe, Cr + H2SO4 (конц.) холодная→ пассивация
Al, Fe, Cr + H2SO4 (конц.) t˚C→ SO2
4HNO3 (k) + Cu = Cu(NO3)2 + 4H2O + 2NO2↑
8HNO3 (p) + 3Cu = 3Cu(NO3)2 + 4H2O + 2NO↑
Pt, Au + HNO3 → реакции нет
Al, Fe, Cr + HNO3 (конц) холодная→ пассивация
Al, Fe, Cr + HNO3 (конц) t˚C→ NO2
Al, Fe, Cr + HNO3 (разб) → NO
3). С растворами солей менее активных металлов
Ме + Соль = Новый металл + Новая соль
Золото и серебро — интересные факты о металлах
Fe + CuCl2 = FeCl2 + Cu
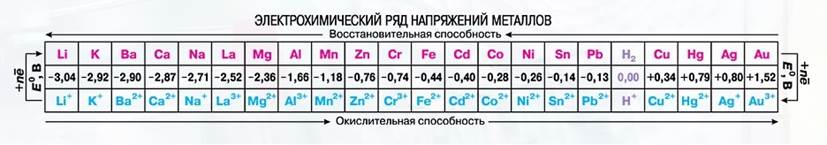
Активность металла в реакциях с кислотами, водными растворами солей и др. можно определить, используя электрохимический ряд, предложенный в 1865 г. русским учёным Н. Н. Бекетовым: от калия к золоту восстановительная способность (способность отдавать электроны) уменьшается, все металлы, стоящие в ряду левее водорода, могут вытеснять его из растворов кислот; медь, серебро, ртуть, платина, золото, расположенные правее, не вытесняют водород.
3. Закрепление изученного материала
№ 1. Закончите УХР, расставьте коэффициенты методом электронного баланса, укажите окислитель (восстановитель):
№ 2. Решите тестовые задания:
1. Выберите группу элементов, в которой находятся только металлы:
2. Выберите группу, в которой находятся только простые вещества – неметаллы:
3. Укажите общее в строении атомов K и Li:
А) 2 электрона на последнем электронном слое;
Б) 1 электрон на последнем электронном слое;
В) одинаковое число электронных слоев.
4. Металлический кальций проявляет свойства:
В) окислителя или восстановителя в зависимости от условий.
5. Металлические свойства натрия слабее, чем у
6. К неактивным металлам относятся:
А) алюминий, медь, цинк;
Б) ртуть, серебро, медь;
В) кальций, бериллий, серебро.
7. Какое физическое свойство не является общими для всех металлов:
В) твердое агрегатное состояние при нормальных условиях,
Г) металлический блеск.
Часть В. Ответом к заданиям этой части является набор букв, которые следует записать.
С увеличением порядкового номера элемента в главной подгруппе II группы Периодической системы свойства элементов и образуемых ими веществ изменяются следующим образом:
1) число электронов на внешнем уровне
4) восстановительные свойства
В) не изменяется
4. Домашнее задание
П. 37, упр. 11-12, задача 4 на стр. 112.
Библиотека образовательных материалов для студентов, учителей, учеников и их родителей.
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы из сети Интернет, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
Источник: axiomaonline.ru