Пользователь
Регистрация: 27.11.2010
Сообщений: 9
В друзьях у: 0
Голосов: 0 / 0
Добавлено: 04.10.2011 23:53:13
korobtsov-alex,
Спасибо большое за полезную информацию.
Теперь понятно, для чего нужен цинк!
Пользователь
Регистрация: 22.06.2008
Откуда: дороже Питера
Сообщений: 3795
В друзьях у: 38
Голосов: 454 / 7
Добавлено: 08.10.2011 01:21:50
Leon.joyas,
Хлорид серебра восстанавливается в металл в присутствии водорода. При травлении цинка в солянке выделяется необходимый водород. Может и в серной то самое происходит, не пробовал правда.
Пользователь
Регистрация: 29.05.2008
Откуда: РХТУ им. Менделеева, Москва
Сообщений: 853
В друзьях у: 18
Голосов: 164 / 2
Добавлено: 08.10.2011 10:29:00
Хлорид серебра восстанавливается и без водорода по электрохимическому механизму обмена электронами (цинк отдает, серебро(хлорид) забирает) — если цинк опустить в нейтральную дист.воду с хлоридом серебра, последний все равно восстановится, только медленней. Кислота резко ускоряет коррозию цинка (и, соответственно, отдачу электронов), а выделение водорода — всего лишь побочная реакция (т.к. он тоже забирает электроны у цинка, см. ряд напряжений металлов)
Оцинковка своими руками. Сравниваем три электролита
Пользователь
Регистрация: 13.10.2011
Сообщений: 2
В друзьях у: 0
Голосов: 0 / 0
Добавлено: 13.10.2011 20:26:49
всем добрый вечер, вопрос по аффинажу серебра. подскажите пожалуйста — как можно сократить потребление дистилированной воды при промывке соли серебра после осаждения в азотке. и существуют какие-то требования по чистоте азотной и соляной кислоты. дело в том, что при получении 300 гр. серебра было израсходовано почти 30 литров дистиллированной воды.
Пользователь
Регистрация: 22.06.2008
Откуда: дороже Питера
Сообщений: 3795
В друзьях у: 38
Голосов: 454 / 7
Добавлено: 13.10.2011 20:45:04
| (Кирилл Мефодьевич 08.10.2011 10:29:00) Хлорид серебра восстанавливается и без водорода по электрохимическому механизму обмена электронами (цинк отдает, серебро(хлорид) забирает) — если цинк опустить в нейтральную дист.воду с хлоридом серебра, последний все равно восстановится, только медленней. |
Вот и верь апосля этого книжкам. )))))) Я ведь это из книжицы какой-то нашей ювелирной взял. Ещё помню пытался обдумывать как цинк травить отдельно, а струю водорода под серебро подвести, чтоб бурбулил)))) Ну, теперь понятен процесс, спасибо.
Пользователь
Регистрация: 13.10.2011
Сообщений: 2
В друзьях у: 0
Голосов: 0 / 0
Добавлено: 13.10.2011 21:39:43
ремесленник,
я просто хотел применить систему фильтров (грубой очистки, угольной), вроде как на 2 -5 кубов хватит. или просто гасить щелочью до нейтральной реакции.
а по чистоте азотной и соляной кислоты (класс ч подойдет?)
Пользователь
Полезные лайфхаки, которые можно попробовать дома! Секрет цинка
Регистрация: 12.04.2011
Откуда: Днепродзержинск
Сообщений: 31
В друзьях у: 0
Голосов: 0 / 0
Добавлено: 13.10.2011 21:48:22
jukraine,
К чему такой напряг?я из крана беру лет 15 и порядок!
Слишком хорошо-ТОЖЕ ПЛОХО
Пользователь
Регистрация: 29.05.2008
Откуда: РХТУ им. Менделеева, Москва
Сообщений: 853
В друзьях у: 18
Голосов: 164 / 2
Добавлено: 14.10.2011 13:52:43
азотка техническая, дистиллировка только для разбавления азотки при растворении серебра, затем хлорид натрия из магазина (10-15 руб./кг), вода кипяченая из-под крана для промывки и хлорида серебра, и серебряного порошка — дешево и сердито
Пользователь
Регистрация: 22.06.2008
Откуда: дороже Питера
Сообщений: 3795
В друзьях у: 38
Голосов: 454 / 7
Добавлено: 14.10.2011 23:05:22
Кирилл Мефодьевич,
А вот вопрос к Вам — Соль брать можно йодированную или разницы нету.? Я для плавки опилок её использую и в отбел иногда добавлял,но старался брать не йодированную. А йод , я читал, доволно активен с металлами. Или он там в таких незначительных колличествах, что не опасен.
Изменено: Валера Сурик — 27.06.2016 01:00:35
Пользователь
Регистрация: 29.05.2008
Откуда: РХТУ им. Менделеева, Москва
Сообщений: 853
В друзьях у: 18
Голосов: 164 / 2
Добавлено: 17.10.2011 10:21:47
Лучше брать неиодированную — иод образует растворимую комплексную соль с серебром, это хоть и незначительные, но лишние потери. Да и хлорид натрия надо вводить с минимальным избытком, поскольку растворимость серебра хлористого в избытке хлоридов тоже повышается (тоже за счет комплексообразования).
Пользователь
Регистрация: 24.02.2009
Сообщений: 1854
В друзьях у: 2
Голосов: 116 / 20
Добавлено: 25.10.2011 00:57:19
Кирилл Мефодьевич,
а правильно я понимаю, что для восстановления металлического серебра из хлорида, в кислой среде можно воспользоваться любым металлом стоящим левее водорода в ряду электрохимической активности ?
и правильно ли что чем дальше от водорода металл отстоит . тем эффективнее будет происходить восстановление серебра.
т.е. алюминий эффективнее цинка, а магний эффективнее алюминия ?
хочется знать чем павильнее пользоватся, т.к. специально покупать металлический цинк. при наличии , например бухты алюминиевого провода, или магниевого электрода от водонагревателя, вроде глупо, да и как оказалось—не так просто.
моё личное мнение основано на моём личном опыте /// «Раб не хочет обрести свободу; он хочет иметь собственных рабов»
Источник: www.jportal.ru
Как цинк покрыть серебром
Камрады, кто может помочь посеребрить знак из цинкового сплава? Сам попробовал с фиксажем и фотобумагой, ничего не получилось. Основа тёмная, чтобы получить устойчивое видимое серебрение нужен плотный слой серебра
Только электрохимия спасёт, с анодом из серебра. Чисто химическое осаждение при такой разности потенциалов гарантировано даст слой шлама и хреновое покрытие.
Завтра поищу книжку «рецептурный сборник электротехника», там были рецепты электролитов и режимы осаждения.
Только электрохимия спасёт, с анодом из серебра. Чисто химическое осаждение при такой разности потенциалов гарантировано даст слой шлама и хреновое покрытие.
Завтра поищу книжку «рецептурный сборник электротехника», там были рецепты электролитов и режимы осаждения.

Кто б сделал бы такое, не химик(физик) я деньжат бы подкинул, договорились бы
да и городить гальванику ради одного знака не хочется.
ЗЫ. Знак небольшой, кокарда-череп с фуражки. Был бы оригинал, ничего бы делать не стал. Но это старая качественная копия и поэтому можно поэкспериментировать
а просто отлить копию из серебра не?
dk12k
а просто отлить копию из серебра не?
Нет, так будет совсем не аутентично. Оригинал штампованный и в покрытии, за исключением позднего в алюминии без покрытия, но он сюда не пойдёт. Пока просто хотел копии придать более приличный вид серебрением. Оригинал неподъемный по деньгам, как нибудь потом подыщу
Я бы попробовал засеребрить в два этапа: сначала в медном купоросе (подложка), потом в растворе серебряной соли. Естественно — сначала «потренироваться на кошках» ☺

Купил пасту серебритель. Где то со второго раза пошло серебрение. Так раза три четыре повторил, результатом доволен
Серебрение в домашних условиях: обзор способов покрытия серебром
Серебрение изделий из металла можно выполнить и в домашних условиях. Качественно провести такую процедуру можно различными способами, причем для практической реализации многих из них вам не потребуется искать и покупать дорогостоящие химические реактивы. Приготовить раствор для посеребрения медных изделий можно из доступных средств даже в домашних условиях.

На фото видно, как меняется внешний вид изделия после серебрения
Изделия, покрытые слоем серебра, как и позолоченный металл, смотрятся очень презентабельно, что и объясняет высокую популярность такой технологической операции.
Как выполняется серебрение меди и медных сплавов
Процесс серебрения отличается рядом особенностей, которые обязательно следует учитывать при его выполнении. Заключаются такие особенности в следующем.
- Серебрению, как правило, подвергают изделия, изготовленные из меди, латуни, алюминия, стали и ряда других сплавов. Из раствора для выполнения серебрения при соприкосновении с данными металлами и сплавами выделяется металлическое серебро, что и позволяет эффективно осуществлять такой технологический процесс.
- Качественно посеребрить легче всего светлый металл. Чтобы из-под нанесенного слоя серебра не просвечивала более темная поверхность основного металла, толщина такого слоя должна составлять не менее 10–15 микрометров.
- Серебрение в домашних условиях или на производственном участке необходимо выполнять в помещениях, которые хорошо проветриваются.
- Для того чтобы серебрение латуни, меди или любого другого металла отличалось высоким качеством, обрабатываемую поверхность необходимо предварительно обезжирить.
- Пасту, при помощи которой выполняют серебрение, наносят посредством кусочка мягкой ткани или кожи.
Химический метод
Один из способов, при помощи которого выполняется химическое серебрение, заключается в том, что поверхность металла обрабатывается антихлором (тиосульфатом натрия) – раствором для фиксирования фотографии. Суть метода серебрения с применением такого раствора состоит в следующем.
- В один литр антихлора, который уже не годится для закрепления фотопленки, добавляют шесть-десять капель формалина и 4–6 мл нашатырного спирта.
- Медное изделие, подвергаемое серебрению, тщательно готовят: поверхность зачищают до металлического блеска, затем деталь кипятят в растворе соды и тщательно промывают водой. После такой подготовки обрабатываемое изделие погружается в фотораствор на час-полтора.
- После выдержки в фоторастворе металл покрывается тонким слоем серебра. Завершающими этапами процедуры серебрения по данной технологии являются промывка изделия водой, просушка и полировка.
- Выполнить посеребрение изделий из меди можно и при помощи обычной фотобумаги.
- Фотобумагу режут на отдельные части и погружают в раствор, состав которого указан на ее упаковке.
- Изделие, на поверхность которого необходимо нанести слой серебра, тщательно подготавливают и опускают в раствор с фотобумагой.
- Обрабатываемую поверхность натирают эмульсионным слоем фотобумаги, в результате чего формируется серебряный налет.
- После окончания процедуры изделие тщательно промывают водой, просушивают, а затем натирают мягкой тканью.

Все реактивы для этого способа серебрения можно купить в свободной продаже
Посеребрить медь можно и следующим способом.
- В 300 мл антихлора добавляют 2 мл водного раствора гидроксида аммония и 2–3 капли формалина.
- Полученный раствор ставят в темное место и на 30 минут (или даже на полтора часа) погружают в него обрабатываемое изделие.
- После выдержки в растворе изделие высушивают и протирают мягкой тканью.
Использование специальных паст
Для того чтобы посеребрить металл, можно использовать специальные пасты, которые легко приготовить и в домашних условиях. Серебрение металлических изделий при помощи специальных пастообразных составов выполняется по различным методикам.
Первый из таких способов предполагает использование нитрата серебра, который часто называют ляписным карандашом. Хотя данный способ серебрения и отличается достаточно высокой сложностью, он позволяет сформировать на поверхности металла плотное серебряное покрытие.
Ляписный карандаш также используют в качестве «тестера» серебра и других металлов
Для реализации данного метода серебрения готовят водный раствор, состоящий из 300 мл воды и 2 граммов нитрата серебра. В полученный раствор постепенно добавляют хлороводородную кислоту или 10%-й водный раствор поваренной соли. Выполняют такой процесс до того момента, пока на дно емкости не перестанет выпадать осадок, представляющий собой хлорное серебро. Полученный таким образом осадок, выглядящий в виде хлопьев, необходимо собрать, отфильтровать и тщательно промыть.
Отфильтрованное и промытое хлорное серебро смешивают с раствором, состоящим из 100 мл воды и 20 граммов гипосульфита натрия. Полученную таким образом смесь профильтровывают и смешивают с зубным порошком или размолотым мелом, доводя ее консистенцию до сметанообразного состояния. Такая смесь уже готова к применению, ею и натирают поверхность медного изделия, в результате чего на нем формируется тонкая пленка серебра.
Чтобы выполнить посеребрение медных изделий по второму методу, надо смешать следующие компоненты:
- 6 граммов хлорида серебра;
- 8 граммов пищевой соли;
- такое же количество виннокислого калия.
Все вышеперечисленные компоненты смешиваются в сухом виде и тщательно перетираются в ступке. Полученная смесь может храниться в посуде из темного стекла достаточно длительное время. Непосредственно перед использованием этот порошок разводят в воде до пастообразного состояния и натирают таким средством поверхность обрабатываемого изделия.
Следующий метод серебрения предполагает использование смеси, в состав которой входят следующие компоненты:
- 4 грамма битартрата калия;
- 2 мл нашатыря;
- 1 грамм ляписного карандаша.
Полученную смесь растворяют в воде до пастообразного состояния, наносят ее на мягкую ткань, которой и натирают обрабатываемую поверхность до получения серебряного блеска.

Перед серебрением изделий, независимо от способа обработки, необходимо тщательно обезжиривать поверхности
Чтобы посеребрить металл по данному методу, готовят смесь следующего состава:
- 10 граммов нитрата серебра;
- 25 граммов цианида калия;
- 100 мл воды.
Технология приготовления пасты для серебрения по данному методу выглядит следующим образом:
- Нитрат серебра растворяют в 50 мл воды.
- В полученный раствор добавляют цианистый калий и еще 50 мл дистиллированной воды.
- Вводят в раствор 10 граммов битартрата калия и 100 граммов порошкообразного мела, доводя консистенцию смеси до пастообразного состояния.
Пастой, которая получилась в итоге смешивания всех компонентов, обрабатывают поверхность изделия, после чего его промывают водой и тщательно просушивают.
Порошки, из которых готовятся такие пасты для серебрения, могут храниться в сухом виде достаточно длительное время (год и больше), в то время как жидкость для серебрения имеет срок годности, ограниченный всего несколькими сутками.
Серебрение с нагреванием обрабатываемого изделия
Чтобы приготовить набор для серебрения, при выполнении которого обрабатываемое изделие будет нагреваться вместе с применяемым раствором, используется несколько методик.
Для реализации первого метода готовится смесь следующего состава:
- 100 граммов хлористого серебра;
- 600 граммов битартрата калия;
- такое же количество поваренной соли.

Для взвешивания нужного количества реактивов понадобятся весы, вполне подойдут простые рычажного типа
Полученную сухую смесь, которая длительное время может храниться в емкости из темного стекла, растворяют в воде (из расчета 3 столовых ложки сухой смеси на пять литров воды) и доводят полученный раствор до кипения. Металл, подвергаемый серебрению, кипятят в таком растворе на протяжении четверти часа.
В результате такой обработки металл покрывается матовым слоем серебра. Чтобы придать покрытию блеск, необходимо дополнительно обработать изделие в растворе следующего состава:
- 4,8 литров воды;
- 300 граммов серноватисто-натриевой соли;
- 100 граммов уксусно-свинцовой соли.

Раствор необходимо профильтровать перед применением
Такой раствор доводят до температуры 70–80° и выдерживают в нем изделие на протяжении 10–15 минут. В результате такой обработки поверхность металла приобретает характерный серебряный блеск.
Посеребрить металл можно и с использованием такого состава:
- хлорид серебра, полученный из 25 граммов нитрата серебра;
- 150 граммов битартрата калия;
- пищевая соль;
- вода.
2–3 столовых ложки такой смеси добавляются в пять литров воды, которая доводится до кипения. Обрабатываемые изделия погружают в такой раствор в глиняном или фарфоровом сите, при этом кипящую смесь непрерывно перемешивают палочкой из стекла или дерева.
Погружной способ серебрения
Такое гальваническое серебрение позволяет получать посеребренную проволоку или изделие любого другого типа с более плотным покрытием. Гальваническое покрытие серебром также может выполняться с помощью разных методик.
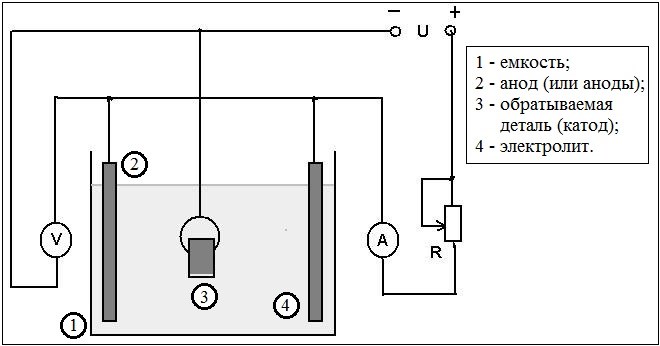
Схема гальванической ванны
Для реализации первого метода серебрения, в котором задействована гальваника, готовят раствор следующего состава:
- 70 мл водного раствора гидроксида аммония;
- 10 граммов хлорида серебра;
- 40 граммов кристаллической соды;
- такое же количество цианистого калия;
- 15 граммов пищевой соли.
Смешивая компоненты данного раствора с дистиллированной водой, доводят его объем до одного литра. Гальванизация обрабатываемого изделия происходит за счет того, что в емкость, в которой производится серебрение, добавляются куски цинка или пластина из данного металла.

Для электролита подойдет стеклянная или пластиковая посудина из химически нейтрального материала, выдерживающего нагрев до 80°С
Пастообразная смесь для серебрения по данному методу готовится из следующих компонентов
- 11 граммов ляписа;
- 60 граммов цианида калия;
- 750 граммов порошкообразного мела;
- 60 мл воды.
В пастообразную массу, полученную при смешивании такой смеси с двумя частями воды, погружают небольшие изделия, а более крупные детали просто натирают ей.
Цинк покрытый серебром. Какое это покрытие – анодное или катодное? Почему?
⚡ Условие + 37% решения:
Цинк покрытый серебром. Какое это покрытие – анодное или катодное? Почему? Какой из металлов будет корродировать во влажном воздухе в случае разрушения покрытия? Составьте электронные уравнения анодного и катодного процессов?
Каков состав продуктов коррозии?
Решение: Анодное покрытие – это покрытие из металла, имеющего меньшее значение стандартного электрохимического потенциала, чем у защищаемого металла. Катодное покрытие – это покрытие из металла, имеющего большее значение стандартного электрохимического потенциала, чем у защищаемого металла. Стандартные электродные потенциалы цинка и серебра имеют следующие значения B Zn Zn 0,763 / 2 B Ag Ag 0,799 / Так как цинк имеет меньшее значение электродного потенциала, следовательно, он является анодом, то есть покрытие анодное. В случае разрушения покрытия во влажном воздухе будет корродировать цинк. Записываем электронные уравнения анодного и катодного процессов
Готовые задачи по химии которые сегодня купили:
- Напишите электронные и электронно-графические формулы атомов фосфора, ванадия, стронция.
- Расставьте коэффициенты в окислительно-восстановительных реакциях, используя метод электронного баланса, или метод полуреакций.
- Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей MnCl2, Na2CO3, Ca(NO3)2, NH4CH3COO. Какое значение рН (>7<) имеют растворы этих солей?
- Напишите выражения для константы равновесия систем: а) СО2(г) + С(графит) 2СО(г); б) 2СО2(г) 2СО(г) + О2(г)
- Какие из солей K2CO3, FeCl3, K2SO4, NH4I подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
- Вычислите массовую долю (в процентах) сахара С12Н22О11 в водном растворе, зная температуру кристаллизации этого раствора t = -0,93°С. Криоскопическая константа воды 1,86.
- Для реакций HIO3 + H2O2 → I2+ O2+ H2O I2 + H2O2 → 2HIO3+ H2O а) составьте баланс степеней окисления и укажите, какой процесс — окисление или восстановление — происходит при следующих превращениях; б) уравняйте реакции методом электронного баланса (Для студентов химических направлений уравняйте реакции методом полуреакций); в) на основании баланса степеней окисления расставьте коэффициенты в уравнении реакции, идущим по схемам; г) укажите тип окислительно-восстановительной реакции; д) рассчитайте эквивалентые массы окислителя и восстановителя.
- Каким образом должны быть составлены гальванические элементы, чтобы в них протекали реакции: а) Mg+ CuSO4 → MgSO4 + Cu; б) 2Au3+ + 3H2 → 2Au + 6H+ ; в) Zn + 2Fe3+ → Zn2+ + 2Fe2+ .
- Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) К2S и HCl; б) FeSO4 и (NH4)2S; в) Cr(OH)3 и KOН, учитывая, что гидроксид хрома (III) проявляет амфотерные свойства.
- Составьте электронные уравнения процессов, происходящих на электродах при электролизе растворов CuSO4 и КI.





















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
Источник: lfirmal.com