Магниевая вспышка
В магниевой вспышке свет излучается вследствие интенсивного сгорания в воздухе металлического, с окисляющими добавками, магния в порошке или в виде ленты.
Зажигание смеси осуществляется при помощи специальных приспособлений с кремнием или пистоном, а при отсутствии таких приспособлений смесь, насыпанная на металлическую пластинку, поджигается при помощи целлулоидной ленточки длиной 10–15 см.
Рецепты магниевых смесей
На одну весовую часть магния:
Количество весовых частей добавки
Быстро сгорает, дает мало дыма
Хорошо сохраняется, дает мало дыма
Имеет наибольшую световую отдачу, плохо сохраняется
Имеет хорошую световую отдачу
Добавляется 0,01 весовой части сернистой сурьмы
Дает наибольшее количество дыма
Примечание: смешивать инградиенты, в особенности содержащие бертолетову соль и сернистую сурьму, необходимо крайне осторожно, т.к. возможно воспламенение смеси порошков от трения!
Световая энергия, излучаемая порошковой магниевой вспышкой, зависит от количества смеси и может быть очень велика, достигая нескольких сот тысяч люмен-секунд. Полная продолжительность горения вспышки составляет обычно 1/5–1/10 секунды, однако эффективная продолжительность магниевой вспышки составляет не более половины от полной продолжительности горения и равна приблизительно 1/15–1/20 секунды.
Горение магния — химическая реакция.
Практическая невозможность синхронизации магниевой вспышки с работой затвора фотоаппарата заставляет производить съемку с установкой затвора на длительную выдержку, открывая последний непосредственно перед моментом вспышки и закрывая после ее прекращения.
Гнездо синхронизации M, имеющееся на некоторых старых фотоаппаратах, было предназначено для подключения ламп-вспышек — прозрачных колб, наполненных кислородом и содержащих алюминиевую фольгу (иногда в сплаве с магнием, а первоначально — и непосредственно магниевую стружку). Внутрь колбы пропущена токопроводящая нить, концы которой присоединены к электродам цоколя лампы. При подаче на лампу напряжения 4–8 В нить перегорает, поджигая фольгу, которая сгорая в кислороде, дает мощную световую вспышку.
Современные фотовспышки используют импульсные газоразрядные лампы.
При использовании магниевых вспышек открытого типа необходимо строго соблюдать меры пожарной безопасности, а также учитывать, что при сгорании магниевой смеси образуется много дыма, мелкие пылевые частицы которого после осаждения могут испортить окружающие предметы.
Вспышка магниевой смеси обладает огромной эффективностью. Вследствие очень высокой температуры сгорания, свет магниевой смеси обладает весьма большой фотографической актиничностью.
При съемке со вспышкой магния выдержка (в зависимости от состава и количества смеси) колеблется от 1/10 до 1/30 секунд., т.е. съемка фактически производится моментально. Необходимая экспозиция (количество освещения) регулируется только количеством смеси, поэтому целью расчетов является определение количества магниевой смеси, необходимое для данных условий съемки.
Магний — самый горячий металл на Земле!
Магниевая смесь представляет собой смесь мелкого порошка металлического магния с различными окислителями, в качестве которых применяются нитраты бария, тория, аммония, калия а также перманганат и хлорат калия.
Также, можно применять магний в виде опилок различной крупности или лент. Сгорание чистого магния (без каких – либо окислителей) на воздухе происходит гораздо медленнее, что иногда более приемлемо. Нет магния? Замените его алюминиевой пудрой (предварительно пересчитав количество окислителя в смеси).Если вы предпочитаете иметь дело только с пудрой, то на воздухе её нужно сжигать небольшими порциями, т.к. при её горении в большом количестве часть алюминия под действием высокой температуры сплавляется в королёк металла и не сгорает. Если выражаться более простым языком – это половина чайной ложки алюминиевой пудры.
Техника безопасности:
Все составы, содержащие порошкообразный металл (в данном случае Mgи/или Al) и окислитель взрывоопасны и при взрыве могут (и вызывают!) серьёзные ожоги; поэтому их приготовление и сжигание требует большой осторожности и соблюдения ряда правил:
1. Составные части этих смесей следует измельчать в порошок по отдельности с помощью фарфоровой ступки.
2. Смешивание составных частей следует производить в небольших количествах (2-3 г. на первых порах) с помощью птичьего перышка или длинной деревянной/пластиковой палочки. Оденьте защитную маску с прозрачным плексигласовым экраном.
3. Во избежание возникновения искр смесь должна быть однородной.
4. Смеси сжигать на металлической пластинке с помощью полоски пропитанной селитрой (желательно калийной) бумаги или целлулоида, при этом один конец длиной в 8-10 см. выводится наружу и поджигается. Очень хороши (для помещения в них смеси) крышки от пивных бутылок.
5. Нельзя (читай – не рекомендуется) сжигать смеси на вате и подносить горящую спичку непосредственно к смеси. Спичку надо вставить в длинную пластиковую/металлическую трубочку или же схватить пинцетом. Желательно надеть кожаные перчатки и заправить в них рукава.
Помните о том, что вследствие высокой температуры сгорания, в излучаемом спектре значительная доля приходится на вредное для глаз ультрафиолетовое излучение. Защита – увиолевые светофильтры С-4 или С-5 (сварочные).Ультрафиолетовое излучение ослабляется также с увеличением расстояния до его источника: с 10 – 15 м. за вспышкой 2-3 г. смеси можно наблюдать без светофильтров.
6. В случае невоспламенения смеси следует подождать не менее 1-1,5 минут и только после этого приблизиться к смеси, т.к. возможно «позднее зажигание» (или “подлое зажигание”).
7. Не следует сжигать смеси на расстоянии менее 1,5-2 м. от людей (обосрутся).
Не следует также самому находиться ближе 1 м.
8. Смеси чувствительны к удару! Особенно смесь MgcNH4NO3 (или КClO3).Не бейте по ним молотком и не мешайте их металлическим (стальными, железными, алюминиевыми) предметами в металлических (стальных, железных, алюминиевых или стеклянных) емкостях. Засыпьте компоненты в пластиковый стаканчик, слегка наклоните его и вращайте до тех пор, пока смесь не станет однородной.
Если будете обращаться с ней деликатно – всё у вас будет ОК.
Если нет – вас ждут серьёзные ожоги (в лучшем случае).
9. По возможности ограничьтесь небольшими дозами смеси (не более 2-3 г.)
поберегите магний – он вам ещё пригодится…
Рецепты магниевых смесей.
Вещества
Количество весовых частей
Характеристика
Источник: camera-history.ru
Чем можно, а чем нельзя тушить магний
Большинство людей думает, что металлы (Me) не горят. Но это не так. Причем воспламенения некоторых Me ликвидировать очень сложно. Ошибка способна привести к взрыву и другим неприятным последствиям. В статье пойдет речь о том, чем тушить магний.
Классы пожаров
Процесс неконтролируемого горения, способного нанести существенный ущерб, принято делить на категории:
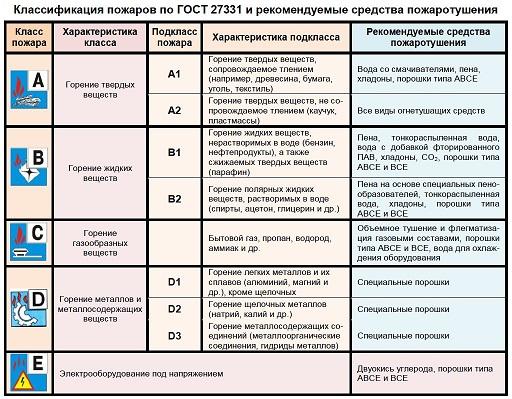
- А – воспламенение твердого вещества (уголь, бумага, пластмасса). Может сопровождаться тлением.
- В – горение жидкости.
- С – пожар с участием газообразного вещества.
- Д – воспламенение металла.
- Е – возгорание электроустановки.
- F – горение радиоактивного соединения.
Пожары класса D – что это
К этой категории относят все случаи горения металлов. Пожары класса D делятся на 3 вида:
- Д1 – воспламенение легких металлов (магний, алюминий), условно тяжелых (уран, цирконий);
- Д2 – пожар с участием щелочных Me (калий, натрий);
- Д3 – горение металлоорганических соединений.
Как горят металлы
Исходя из характера горения, Me бывают:
- Летучие (магний, калий, натрий, кальций, литий). Для них характерна низкая температура фазового перехода. При 1000 К они начинают плавиться, а при 1500 К – кипеть.
- Нелетучие. Температура фазового перехода плавления у них составляет более 1000 К, а кипения – выше 2500 К. При горении таких металлов формируется оксидная пленка, сцепляющаяся с поверхностью вещества. Из-за этого диффузия паров затрудняется, потому крупные частички бериллия, алюминия и других нелетучих металлов гореть не могут. Воспламенению подвержены стружка и аэрозоли этих Me.
При поднесении к металлу открытого огня на поверхности вещества начинается испарение и окисление. Когда концентрация паров достигает предела, происходит воспламенение Me, возникает цветной огонь. По оттенку можно понять, какой это металл:
- стронций горит бордовым;
- литий – малиновым;
- натрий – ярко-желтым;
- кальций – кирпичным;
- железо – бледно-желтым;
- барий и молибден – зелено-желтым;
- медь – сине-зеленым;
- бор – светло-зеленым;
- селен – голубым;
- мышьяк – светло-синим;
- калий – насыщенным фиолетовым;
- свинец – голубым.
На заметку. Щелочные металлы в виде пудры или порошка, находясь на открытом воздухе, способны к самовоспламенению. Это происходит из-за их окисления, что приводит к повышению температуры.
Характеристика и свойства магния
Mg – двухвалентный, пластичный, щелочно-земельный, активный металл серебристого оттенка. Если магний находится на открытом воздухе, на его поверхности появляется пленка окиси. Этот металл довольно активный и растворяется в воде при нагревании. Реагирует со всеми кислотами, за исключением плавиковой.

Магний устойчив к действию минеральных масел, бензина, едкой щелочи, керосина, соды. Благодаря способности соединяться с хлором и кислородом металл применяют для выделения чистых веществ (титана, брома). Чтобы синтезировать органические соединения, используют возможность взаимодействия Mg с галогенами (йод, хлор).
Чем его можно тушить
Главным средством, используемым для ликвидации воспламенения магния, является порошковый огнетушитель. Оптимальный вариант устройства – тот, в состав которого входят хлориды. Это связано с их доступностью и нетоксичностью.
Механизм действия огнетушителя основан на создании препятствия доступа воздуха к месту горения. К другим свойствам работы усройства относят охлаждение поверхности, ингибирование реакции.

Небольшой очаг можно потушить:
- Чугунной стружкой. При этом нужно проследить, чтобы на поверхности стружки отсутствовала ржавчина, способная вступать в химическую реакцию с магнием, усиливая пожар.
- Воздушно-механической пеной.
- Густым минеральным маслом.
Чем нельзя и что будет
Справиться с возгоранием Mg непросто. Почему нельзя потушить горящий магний углекислотным огнетушителем? Потому что такой пожар происходит при участии СО2, а использование углекислотного огнетушителя только усилит горение. Для ликвидации пламени также недопустимо применять воду, так как может произойти взрыв.
Если начала гореть значительная площадь, то засыпание территории песком приведет к выделению большого количества тепла. Не подойдет и такое популярное средство, как фтористая присадка. Это связано с тем, что в результате ее реакции с магнием формируется аммиак, способный вызвать отравление.

Основные правила тушения пожаров класса D
Горящие металлы затушить практически невозможно. Обычно стратегия борьбы с огнем состоит в том, чтобы дать веществу догореть до конца, сдерживая распространение пожара на большую площадь. Для этого окружающие поверхности заливаются водой или подходящим средством тушения огня.
Новости
Время работы: с 10:00 до 21:00,
Выходной день: вторник
«Ретро-кафе»: в дни работы Планетария с 10:00 до 20:00.
> Элементы: магний – металл, способный гореть в воде
Элементы: магний – металл, способный гореть в воде
Дата: 25.09.2019
Город Эпсом в Великобритании стал знаменит после того, как в1695 году английский врач Неемия Грю (Nehemiah Grew) выделил из вод минерального источника, расположенного в этом городе, горькую соль (представляющую собой порошок белого цвета), обладающую слабительным действием. Аптекари быстро нашли ей применение, назвав эпсомской солью. Позже, когда это сильное слабительное стало распространяться по аптекам многих стран, его стали называть английской солью. Производство английской соли положило начало открытию элемента магния, растянувшемуся на более чем столетний период, так как в основе этого лекарства лежит минерал эпсомит, содержащий магний с формулой MgSO4 · 7H2O.

Кристаллы эпсомита MgSO4 · 7H2O, 7х4х3 см. Месторождение Тibi-Mina, Испания.
Похожий (только внешне!) светлый порошок получался и при прокаливании минерала, найденного в окрестностях греческого города Магнезия. Позже выяснится, что это оксид магния, минерал периклаз с формулой MgO.

Периклаз MgO, 6х5х3 см, карьер Crestmore, Калифорния (США).
Этот порошок стали называть «белая магнезия». За внешнее сходство эпсомскую (английскую) соль также нарекли «белая магнезия», что приводило к некоторой путанице, так как исходные вещества, хоть и содержат магний, но разные по составу.
В 1808 году английский химик Гемфри Дэви с помощью электролиза увлажнённой смеси белой магнезии и оксида ртути получил сплав ртути и тогда ещё неизвестного металла, которому дал латинское название magnesium. Этот термин позже и стал международным символом элемента №12. В России с тех пор утвердилось название «магний». И только в 1829 году французский химик Антуан Бюсси получил чистый магний.
Итак, магний (символ Mg) – легкий металл (в 5 раз легче меди) серебристо-серого цвета. Плавится при температуре 651°C, но в обычных условиях расплавить его трудно, так как нагретый на воздухе до 550°C он вспыхивает и мгновенно сгорает ослепительно ярким пламенем. Способность магния гореть как в воде, так и в атмосфере углекислого газа существенно усложняет тушение пожаров, при которых горят конструкции из магния или его сплавов.

Кристаллы чистого магния
Россия и Китай — две страны с самыми большими запасами магниевых руд. По состоянию на 2015 год Россия обладала запасами в размере 650 млн. тонн, а Китай — 500 млн. тонн. Более половины производимого в мире магния используется в сплавах с алюминием, которые ценятся за их прочность и легкость и широко используются в автомобильных деталях. По некоторым оценкам в ближайшие десять лет спрос на магний будет устойчиво расти.
Источник: planetarium-moscow.ru