В пробирку вносят 2 капли раствора нитрата серебра и прибавляют 1 каплю раствора аммиака – образуется осадок гидроксида серебра. При добавлении 1-2 капель раствора аммиака осадок AgOH легко растворяется с образованием аммиачного раствора оксида серебра ([Ag(NH3)2]OH).
Через аммиачный раствор оксида серебра пропускают ацетилен (см. опыт 1). В пробирке образуется светло-желтый осадок ацетиленида серебра, который затем становится серым.
Опыт 5. Образование ацетиленида меди.
Реактивы и материалы: карбид кальция; хлорид меди CuCl2, аммиачный раствор. Оборудование: фильтровальная бумага (полоски размером 5*40 мм).
В сухую пробирку помещают 1-2 кусочка карбида кальция и добавляют 2 капли воды. В отверстие пробирки вводят полоску фильтровальной бумаги, смоченной аммиачным раствором хлорида меди CuCl2, содержащим комплексный аммиакат состава [Cu(NH3)2]C12. Появляется красно-бурое окрашивание вследствие образования ацетиленида меди.
В водных растворах ацетилениды серебра и меди устойчивы. В сухом состоянии при нагревании или при ударе они взрываются с большой силой.
Получение ацетилена
1. Аверина А.В., Снегирева А.Я. Лабораторный практикум по органической химии. М.: Высшая школа, 1980. – С. 31-33.
Лабораторная работа №5
Ароматические углеводороды.
Цель: экспериментальное получение и изучение свойств ароматических углеводородов.
Образование ацетиленида серебра опыт
Многие знают про ацетиленид серебра Ag2C2, который выпадает в осадок при пропускании ацетилена через аммиачный раствор оксида серебра [1]. Образование малорастворимых ацетиленидов серебра и меди (I) является характерной реакцией на ацетилен (а также на его гомологи, которые содержат водород при тройной связи).
Однако ацетиленид серебра может образовываться не только из аммиачного раствора серебра, но и из раствора нитрата серебра в разбавленной азотной кислоте. Если быть более точным, выпадает смешанная соль: ацетиленид-нитрат серебра.
Согласно Хмельницкому [2] уравнение реакции имеет вид:
Продукт реакции имеет строение: AgC≡CAg·AgNO3 или С2О3NAg3
Техника синтеза проста: через раствор нитрата серебра, подкисленный азотной кислотой, пропускают ацетилен. Однако, свойства осадка сильно зависят от условий получения.
Например, если брать 25% раствор нитрата серебра в 10% азотной кислоте и вести реакцию при 80-90°С, то Ag2C2·AgNO3 получается в виде кристаллов преимущественно удельного веса 5.39; Qвзр=451 ккал/кг; объем газов взрыва 136.7 л/кг; температура вспышки 215-220°С.
Если взять 5% раствор нитрата серебра в воде или очень разбавленной азотной кислоте и вести реакцию при комнатной температуре, то Ag2C2·AgNO3 получается в виде хлопьев удельного веса 5.36; Qвзр =400 ккал/кг; объем газов взрыва 136.7 л/кг; температура вспышки 205-210°С.
В отличие от ацетиленида серебра, осажденного из аммиачного раствора, ацетиленид серебра, полученный из азотнокислого раствора, может быть использован как инициирующее взрывчатое вещество (ИВВ).
Получение хлората калия, бертолетовой соли из отбеливателя (химия)
Инициирующая способность ацетиленида-нитрата серебра сильно зависит от способа получения.
В справочнике Хмельницкого приведена величина предельного заряда Ag2C2·AgNO3 (в гр), необходимого для инициации 0.5 гр различных ВВ:
| Инициирующее вещество | Для тетрила | Для ТНФ | Для ТНТ |
| Ag2C2·AgNO3 (из 5% холодного нейтрального раствора) | 0.05 | 0.10 | >0.15 |
| Ag2C2·AgNO3 (из 5% горячего нейтрального раствора) | 0.03-0.05 | 0.05 | 0.10 |
| Ag2C2·AgNO3 (из 13% горячего раствора в 15% азотной кислоте) | 0.02 | 0.03 | 0.05-0.075 |
| Азид свинца | 5 гр/см 3 (при этой плотности расчетная скорость детонации >4000 м/с). |
Детонатор был взорван над жестяной банкой в которой пробил отверстие
20 мм при начальном диаметре коктейльной трубочки 5мм. Для большинства ВВ такого количества ацетиленида-нитрата серебра должно хватить. Несмотря на ничтожное количество, взрыв даже 0.1 гр вещества при непосредственном контакте может привести к тяжелому увечью вплоть до потери пальца.
По результатам многочисленных испытаний ацетиленид-нитрат серебра показал себя хорошим ИВВ, способным заменить гремучую ртуть и токсичный азид свинца, не говоря уже о чувствительных пероксидах. При этом ацетиленид-нитрат серебра обладает следующими преимуществами:
Ацетиленид серебра

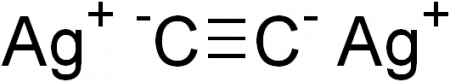 |
|
| Ag2C2 | |
| 239.76 г/моль | |
| 7659-31-6 | |
Внешний вид
Получение
Получают пропусканием ацетилена через аммиачный раствор оксида серебра. Ацетилен получают действием воды на карбид кальция. Атомы водорода в молекуле ацетилена обладают большой подвижностью, поэтому они легко могут быть замещены металлами. Через аммиачный раствор оксида серебра пропускается ацетилен. Выпадает осадок белого цвета — ацетиленид серебра.
Высушенный ацетиленид серебра — очень опасное взрывчатое вещество. Его уничтожают обработкой концентрированной соляной кислотой, реже сульфидом аммония: AgC ≡ CAg + 2 HCl ⟶ HC ≡ CH↑ + 2 AgCl↓ AgC ≡ CAg + (NH4)2S ⟶ HC ≡ CH↑ + Ag2S↓ + 2 NH3↑
Безопасность
Очень опасен. Взрывается при нагревании и механических воздействиях, даже от тлеющей лучины. Необходимо получать только небольшие количества ацетиленида серебра.
Применение
Применяется во взрывчатых веществах, в детонаторах. Источник
Синтез хлорида меди (I). Получение ацетиленида серебра и ацетиленида меди (I).
МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА с. ОКТЯБРЬСКОЕ СТЕРЛИТАМАКСКОГО РАЙОНА РЕСПУБЛИКИ БАШКОРТОСТАН Номинация: Учёные будущего Получение ацетиленида серебра и ацетиленида меди Выполнила: Лукманова Ангелина, ученица 11 класса МОБУ СОШ Научный руководитель: Исхакова Р.У., учитель химии МОБУ СОШ Получение ацетиленида серебра и ацетиленида меди получение ацетиленида серебра; получение ацетиленида меди; доказать свойства веществ. Оборудование: колба, делительная воронка, воронка Бюхнера, газоотводная трубка, стакан, штатив, фильтровальная бумага, штатив с пробирками, ложечка.
Химикаты: гидрат аммиака ( NH 4 OH ), нитрат серебра ( AgNO 3 ), карбид кальция ( CaC 2 ), вода, хлорид меди ( CuCl ). Получение ацетиленида серебра Подготовка оборудования и химикатов. Получение аммиачного раствора оксида серебра. Наполнили на четверть пробирку гидратом аммиака. Добавили столько же оксида серебра. Перемешали.
Получили аммиачный раствор оксида серебра. Закрепили колбу в штативе. Газоотводную трубку опустили в пробирку с аммиачным раствором оксидом серебра. В колбу насыпали 15 грамм карбида кальция. Плотно закрыли. В делительную воронку приливали воду до образования ацетилена. Получение ацетиленида серебра.
Пройдя через газоотводную трубку, ацетилен провзаимодействовал с аммиачным раствором оксида серебра. В результате чего образовался чёрный осадок-ацетиленид серебра. 
Провели проверку : поднесли горящую спичку к 2 граммам ацетиленида серебра. Произошёл взрыв. Получение ацетиленида меди Подготовка оборудования и химикатов. Получение аммиачного раствора хлорида меди. Наполнили на четверть пробирку гидратом аммиака. Добавили 10 грамм хлорида меди ( I ). Перемешали до растворения. Получили аммиачный раствор хлорида меди.
Закрепили колбу в штативе. Газоотводную трубку опустили в пробирку с аммиачным раствором хлорида меди ( I ). Получение ацетиленида меди. В колбу насыпали 15 грамм карбида кальция. Плотно закрыли. В делительную воронку приливали воду до образования ацетилена.
Пройдя через газоотводную трубку, ацетилен провзаимодействовал с аммиачным раствором хлорида меди ( I ). В результате чего образовался красный осадок-ацетиленид меди.  Осадок отфильтровали. Затем высушили. Ацетиленид меди — очень неустойчивое взрывчатое вещество.
Осадок отфильтровали. Затем высушили. Ацетиленид меди — очень неустойчивое взрывчатое вещество.
Провели проверку: поднесли горящую спичку к 2 граммам ацетиленида меди. Произошёл взрыв. Может возникнуть проблема с хлоридом меди ( I ): если он получен не в чистом виде, тогда при его добавлении в гидрат аммиака он растворится не полностью. Чтобы решить эту проблему, нужно отфильтровать раствор. Был получен ацетиленид серебра-очень неустойчивое взрывчатое вещество.
Был получен ацетиленид меди-очень неустойчивое взрывчатое вещество. Репетитор по химии/ под ред. А.С. Егорова. – Изд. 41-е – Ростов н/Д: Феникс,2014. – 762, [1] с. : ил. – (Абитуриент). Вам будут интересны эти курсы:
Оставьте свой комментарий
Детей-инвалидов будут обслуживать вне очереди Искусственный интеллект предупредит студентов о грозящем отчислении Кузнецова предложила оплачивать нянь для детей-инвалидов из семей в трудной ситуации Большинство российских учителей занимаются репетиторством Россиянам разрешили не ставить в паспорт отметки о браке и детях Переболевшие коронавирусом наблюдают у себя ухудшение когнитивных функций
Подарочные сертификаты
Источник: ollimpia.ru
Получение ацетиленида меди (I)
В отличие от многих других углеводородов ацетилен проявляет слабые
кислотные свойства (рКа = 25). Атомы водорода в молекуле ацетилена
способны замещаться на металл. Например, ацетилен взаимодействует со
щелочными и щелочноземельными металлами, а также металлоорганическими
соединениями. При реакции ацетилена с аммиачными растворами солей
серебра и меди (I) образуются малорастворимые ацетилениды этих металлов.
В сухом состоянии ацетилениды серебра и меди неустойчивы и взрываются
при нагревании. Ацетиленид серебра также чувствителен к механическим
воздействиям.
Ниже описан эксперимент по получению ацетиленида меди (I).
Растворите в воде 0.5-1.0 г сульфата меди, добавляйте при
перемешивании раствор аммиака. Сначала выпадет голубой осадок гидроксида
меди, который растворится в избытке аммиака с образованием синего
раствора аммиаката меди (II).
К синему раствору добавьте 1.5-3.0 г
солянокислого гидроксиламина. Выделится азот, раствор обесцветится в
результате восстановления двухвалентной меди до одновалентной.
2[Cu(NH3)4](OH)2 +2NH2OH = 2[Cu(NH3)2](OH) + N2 + 4NH3 + 4H2O
При легком встряхивании этот раствор приобретает
синеватую окраску, поскольку аммиакат одновалентной меди легко
окисляется кислородом воздуха, однако избыток гидроксиламина
восстанавливает медь (II) до меди (I), и раствор снова обесцвечивается.
Теперь пропустите через полученный раствор ацетилен. Жидкость
сразу же окрасится в красно-коричневый цвет в результате образования
осадка ацетиленида меди Cu2C2 . Когда поток газа
прекратится, осадок соберется на дне сосуда, над ним будет прозрачный и
бесцветный раствор. В нашем эксперименте ацетилен был получен реакцией
кусочка карбида кальция (размером с половину ореха) с водой. Этого
вполне хватило.
Отфильтруйте и хорошо промойте осадок, после чего оставьте его
сушиться на фильтровальной бумаге. Для ускорения сушки полезно несколько
раз аккуратно отжать осадок между листами фильтровальной бумаги. Когда
осадок почти высохнет, аккуратно измельчите его в порошок (пластмассовым
шпателем на мягкой бумаге) и разместите тонким слоем на листе белой
бумаги.
Осаждение ацетиленида меди
Смотреть (8.0 Мб, .avi )
Фильтрование, промывка и сушка ацетиленида меди
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
Для восстановления аммиачного комплекса меди (II) до комплекса меди (I)
кроме гидроксиламина подходит также аскорбиновая кислота и гидразин,
однако, использовать эти вещества при синтезе ацетиленида меди (I) автор
не пробовал. Восстановить комплекс [Cu(NH3)4](OH)2 до [Cu(NH3)2](OH)
можно также пр и длительном контакте его раствора с металлической медью
( стружка или проволока) в закрытом сосуде. Об окончании реакции можно
судить по обесцвечиванию раствора. Однако при контакте с воздухом такой
раствор начинает быстро окисляться, поэтому после открытия сосуда
необходимо сразу же начать пропускание ацетилена.
Оттенок ацетиленида меди (I), полученного в разных опытах,
немного отличался. Возможно, это объясняется различием в размере частиц
или некоторой разницей химического состава.
Источник: how-make.ru
Опыты по химии. Непредельные углеводороды

Постановка опытов и текст – к.п.н. Павел Беспалов.
Взаимодействие ацетилена с хлором
В цилиндр насыпаем небольшое количество кристаллов перманганата калия и бросаем кусочек карбида кальция. Затем приливаем в цилиндр соляную кислоту. В сосуде наблюдаются вспышки, стенки цилиндра покрываются сажей. При взаимодействии соляной кислоты с перманганатом калия выделяется газ хлор
16 HCI + 2KMnO4 = 5CI2 + 2 KCI + 2 MnCI2 + 8H2O
С соляной кислотой карбид кальция дает ацетилен
СаС2 + 2 HCI = С2Н2 + СаCI2
Хлор с ацетиленом взаимодействуют, образуя хлороводород и уголь
С2Н2 + CI2 = 2С + 2 НCI
Оборудование: цилиндр, шпатель.
Техника безопасности. Соблюдать правила работы с горючими газами. Опыт проводить только под тягой. После проведения опыта цилиндр залить водой.
Взаимодействие этилена с бромной водой
Получаем этилен нагреванием смеси этилового спирта с концентрированной серной кислотой. Выделяющийся этилен пропустим через раствор брома в воде, который называют бромной водой. Бромная вода очень быстро обесцвечивается. Бром присоединяется к этилену по месту двойной связи. При этом образуется 1,2-дибромэтан.
СН2=СН2 + Br2 = CH2Br — CH2Br
Реакция обесцвечивания водного раствора брома служит качественной реакцией на непредельность органических соединений.
Оборудование: колба Вюрца, капельная воронка, промывалка, газоотводная трубка, стакан или пробирка, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами, концентрированными кислотами и огнеопасными жидкостями.
Взаимодействие ацетилена с бромной водой
Ацетилен получаем действием воды на карбид кальция. Пропустим выделяющийся ацетилен через бромную воду. Наблюдаем обесцвечивание бромной воды. Бром присоединяется к ацетилену по месту тройной связи. При этом образуется соединение с четырьмя атомами брома в молекуле — 1,1,2,2-тетрабромэтан.
СН ≡ СН + 2Br2 = CHBr2 — CHBr2
Обесцвечивание бромной воды доказывает непредельность ацетилена.
Оборудование: колба Вюрца, делительная воронка, газоотводная трубка, стакан или пробирка, штатив.
Техника безопасности. Опыт следует проводить под тягой. Соблюдать правила работы с горючими газами.
Взаимодействие ацетилена с раствором перманганата калия
Ацетилен получаем действием воды на карбид кальция. При пропускании ацетилена через подкисленный раствор перманганата калия наблюдаем быстрое обесцвечивание раствора. Происходит окисление ацетилена по месту разрыва тройной связи с образованием продукта окисления – щавелевой кислоты. В избытке перманганата калия щавелевая кислота окисляется до углекислого газа и воды.
Обесцвечивание раствора перманганата калия служит доказательством непредельности ацетилена.
Оборудование: колба Вюрца, делительная воронка, газоотводная трубка, стакан, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами.
Взаимодействие этилена с раствором перманганата калия.
Получаем этилен нагреванием смеси этилового спирта с концентрированной серной кислотой. Опустим газоотводную трубку с выделяющимся этиленом в подкисленный раствор перманганата калия. Раствор быстро обесцвечивается. При этом этилен окисляется в двухатомный спирт этиленгликоль.
СН2=СН2 + [О] + Н-ОН = CH2ОН — CH2ОН
Эта реакция является качественной реакцией на двойную связь.
Оборудование: колба Вюрца, капельная воронка, промывалка, газоотводная трубка, стакан или пробирка, штатив.
Техника безопасности.
Соблюдать правила работы с горючими газами, концентрированными кислотами и огнеопасными жидкостями.
Взрыв смеси ацетилена с кислородом
Смесь ацетилена с кислородом при поджигании взрывается с большой силой. Поэтому безопасно экспериментировать только небольшими объемами смеси — в этом нам поможет раствор мыла. В фарфоровую ступку с водой и раствором мыла добавим немного пероксида водорода. К полученному раствору прибавим катализатор — диоксид марганца. Сразу же начинается выделение кислорода.
В эту смесь опустим небольшой кусочек карбида кальция. При взаимодействии с водой он дает ацетилен.
На поверхности раствора, благодаря присутствию мыла, образуются пузыри, заполненные смесью ацетилена с кислородом. При поджигании пузырей происходят сильные взрывы смеси ацетилена с кислородом.
Оборудование: фарфоровая ступка, лучина.
Техника безопасности. Соблюдать правила работы с горючими газами. Поджигать можно только небольшой объем смеси.
Горение ацетилена
Получим ацетилен из карбида кальция и воды. Закроем колбу пробкой с газоотводной трубкой. В конец газоотводной трубки вставлена игла для инъекций. Через некоторое время, когда ацетилен полностью вытеснит воздух из колбы, подожжем выделяющейся газ. Ацетилен горит белым ярким пламенем.
При горении ацетилена образуется углекислый газ и вода.
Оборудование: круглодонная колба, пробка с иглой от медицинского шприца, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами. Поджигать ацетилен можно только после отбора пробы на чистоту.
Горение этилена
Получаем этилен нагреванием смеси этилового спирта с концентрированной серной кислотой. Смесь готовят из одной части спирта и трех частей серной кислоты. Серная кислота играет роль водоотнимающего средства. При нагревании смеси выделяется этилен.
Собираем этилен в цилиндр способом вытеснения воды. Этилен – бесцветный газ, малорастворимый в воде. Этилен сгорает на воздухе с образованием углекислого газа и воды.
Оборудование: колба Вюрца, делительная воронка, промывалка, газоотводная трубка, штатив, цилиндр.
Техника безопасности. Соблюдать правила работы с горючими газами, концентрированными кислотами и огнеопасными жидкостями.
Получение ацетиленида меди
Ацетилен получаем действием воды на карбид кальция. Атомы водорода в молекуле ацетилена обладают большой подвижностью. Поэтому они легко могут быть замещены металлами. Пропустим через аммиачный раствор хлорида меди (I) ацетилен. Выпадает красный осадок ацетиленида меди (I) .
СН ≡ СН + 2CuCI → CuC ≡ CCu ↓ + 2HCI
Оборудование: колба Вюрца, делительная воронка, газоотводная трубка, стакан или пробирка, полипропиленовая воронка, фильтровальная бумага, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами. Получать только небольшие количества ацетиленида меди. Высушеный ацетиленид меди — очень опасное взрывчатое вещество. Его уничтожают обработкой концентрированной соляной кислотой.
Получение ацетиленида серебра
Ацетилен получаем действием воды на карбид кальция. Атомы водорода в молекуле ацетилена обладают большой подвижностью. Поэтому они легко могут быть замещены металлами. Пропустим через аммиачный раствор оксида серебра ацетилен. Выпадает осадок ацетиленида серебра.
СН ≡ СН + Аg2O → AgC ≡ CAg ↓ + H2O
Оборудование: колба Вюрца, делительная воронка, газоотводная трубка, стакан или пробирка, полипропиленовая воронка, фильтровальная бумага, штатив.
Техника безопасности. Соблюдать правила работы с горючими газами. Получать только небольшие количества ацетиленида серебра. Высушенный ацетиленид серебра — очень опасное взрывчатое вещество. Его уничтожают обработкой концентрированной соляной кислотой.
Непрочность ацетиленидов металлов
Ацетилениды металлов — неустойчивые соединения. Во влажном состоянии ацетиленид серебра устойчив, высушенный он легко взрывается. Поднесем к сухому ацетилениду серебра тлеющую лучинку — он взрывается. Проведем аналогичный эксперимент с ацетиленидом меди (I).
Так же как и ацетиленид серебра, ацетиленид меди (I) во влажном состоянии устойчив, но легко разлагается, если его высушить. Горящая лучинка, поднесенная к сухому ацетилениду меди (I), приводит к взрыву. При этом появляется пламя, окрашенное в зеленый цвет.
Оборудование: огнезащитная прокладка, лучина.
Техника безопасности. Получать и разлагать можно только небольшие количества ацетиленида серебра и меди. Высушеные ацетилениды серебра и меди — опасные взрывчатые вещества. Ацетилениды уничтожают обработкой концентрированной соляной кислотой.
Источник: www.yoursystemeducation.com