mэ(KOH) = М(KOH)/кислотность = 56/1 = 56 г/моль.
Эквивалентную массы кислоты определим исходя из закона эквивалентов: m(KOH)/m(кислоты) =mэ(KOH)/mэ(кислоты)
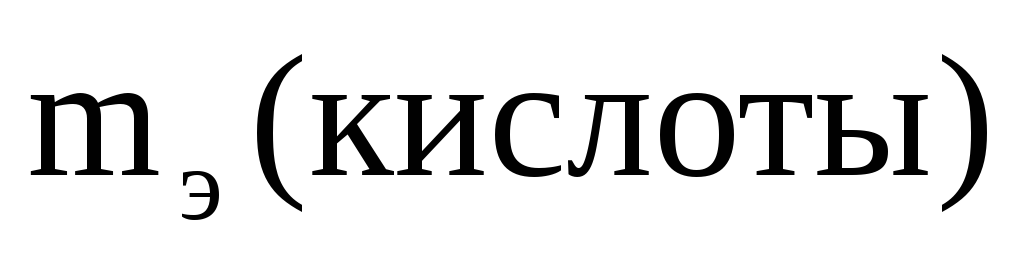 =
= 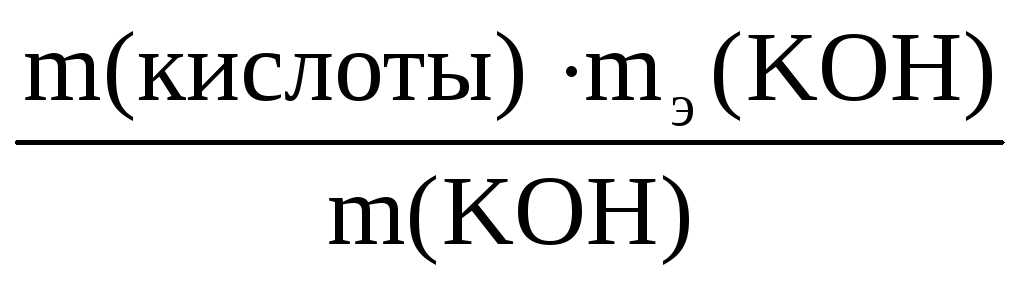
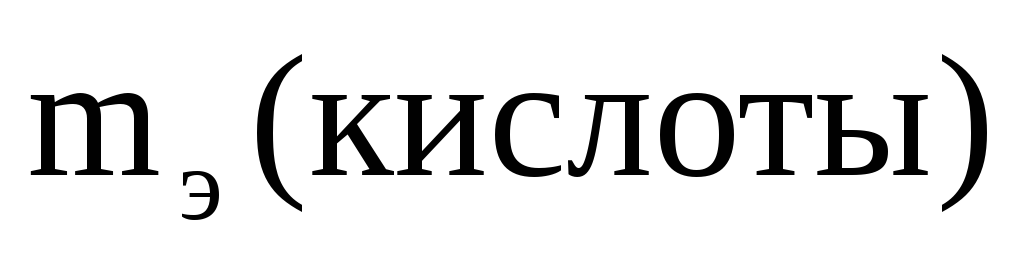 =
= 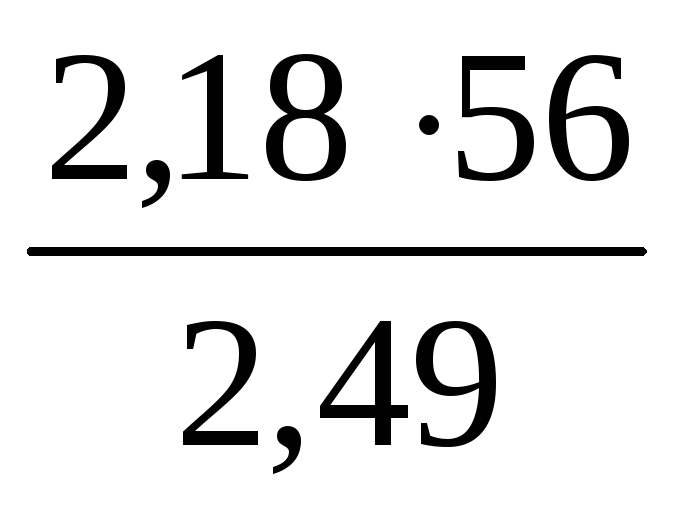 = 49 г/моль
= 49 г/моль
Пример 4. Определите массу металла, вступившего в реакцию с кислотой, если при этом выделился водород объёмом 260 мл при нормальных условиях. Эквивалентная масса металла mэ(Ме) = 9 г/моль.
Решение. Согласно закону эквивалентов массы (объёмы) реагирующих друг с другом веществ пропорциональны их эквивалентным массам (объёмам).
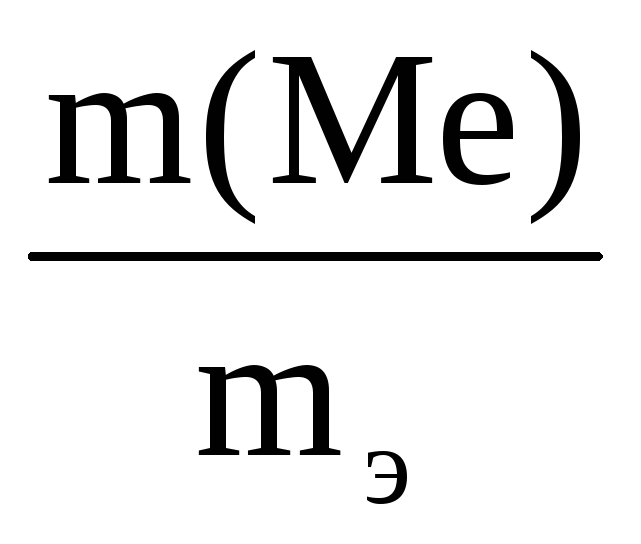 =
=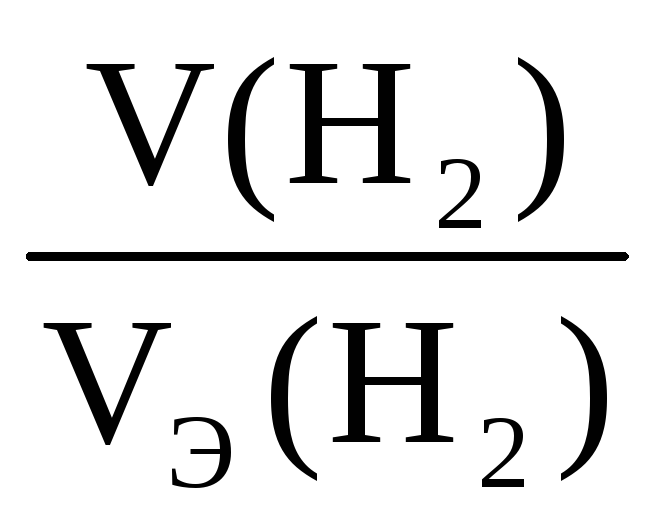 ,
,
133. Эквивалент. Молярная масса эквивалента.
где VЭ(H2) – эквивалентный объём водорода равный 11,2 л.
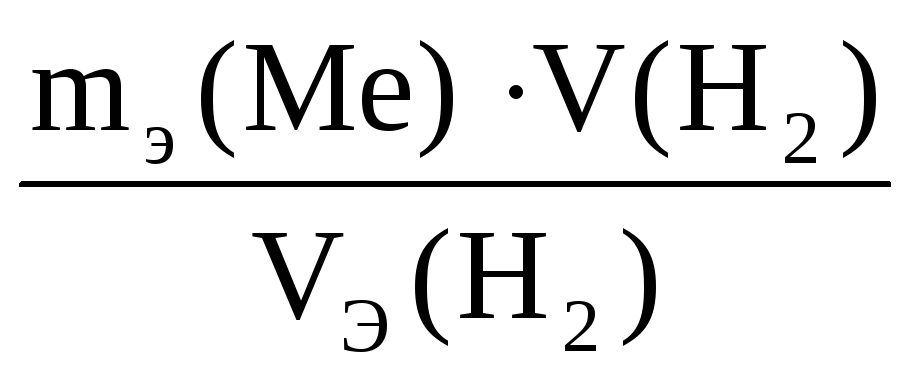
m(Me) = = 90,26/11,2 = 0,2 г.
Пример 5. Эквивалентная масса металла составляет 63,5 г/моль. Вычислите массовую долю металла (Ме) в его оксиде.
Решение. Массовая доля кислорода в оксиде металла будет равна
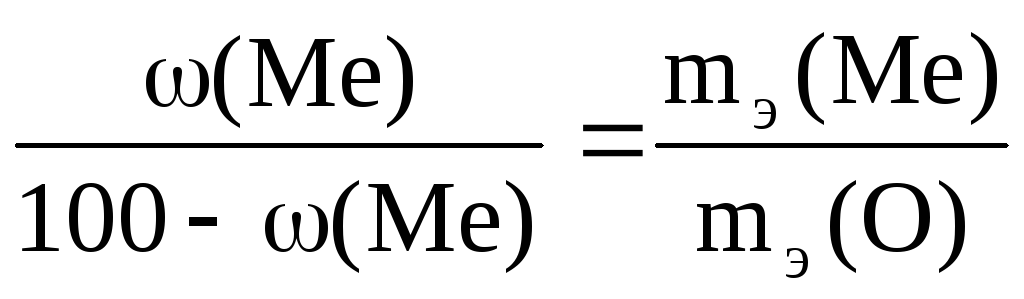
100 − (Ме). Согласно закону эквивалентов: .
Эквивалентная масса кислорода mэ(О) = 16/2 = 8 г/моль.
Из уравнения выразим массовую долю металла
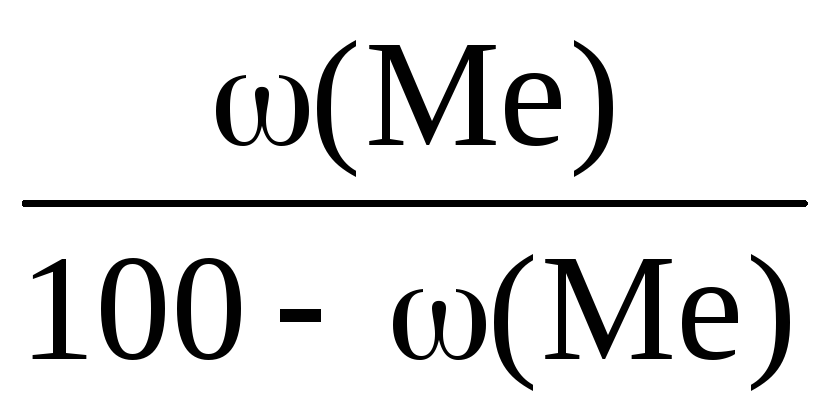 =
= 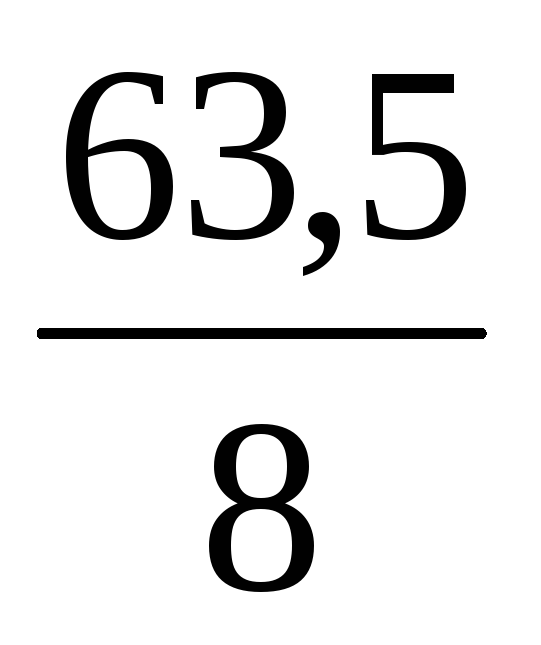
8(Ме) = 6350 – 63,5 (Ме)
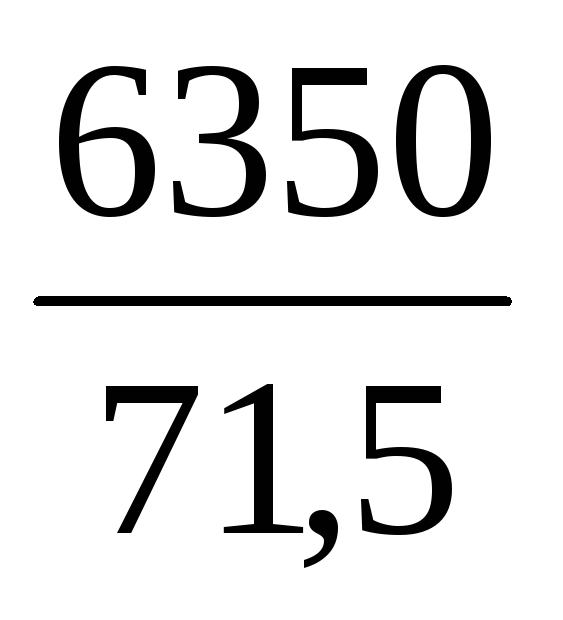
(Ме) = = 88,8 %
Пример 6. Из 3,85 г нитрата металла получено 1,60 г его гидроксида. Вычислите эквивалентную массу металла.
Решение. Эквивалент (эквивалентная масса) химического соединения равен сумме эквивалентов (эквивалентных масс) составляющих его частей.
Эквивалент (эквивалентная масса) гидроксида равен сумме эквивалентов (эквивалентных масс) металла и гидроксильной группы.
Эквивалент (эквивалентная масса) соли равен сумме эквивалентов (эквивалентных масс) металла и кислотного остатка.
Согласно закону эквивалентов:
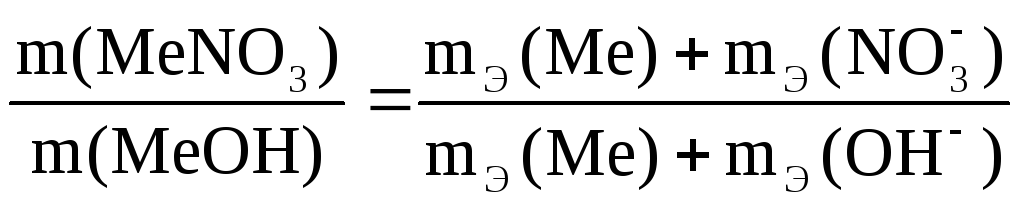
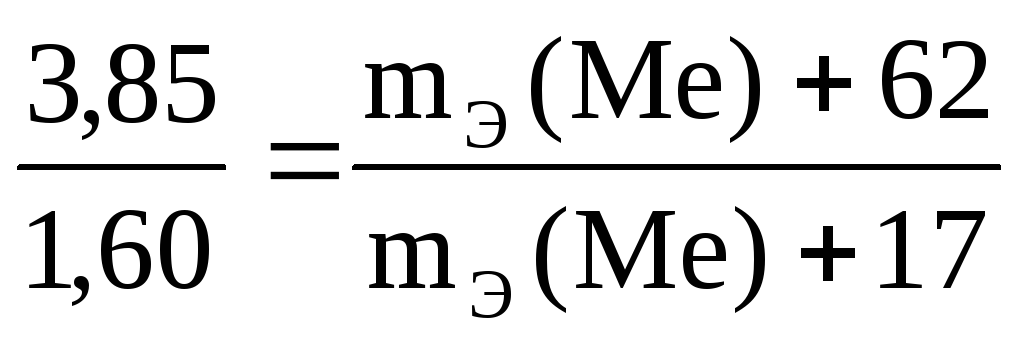
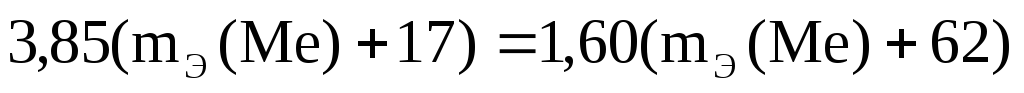
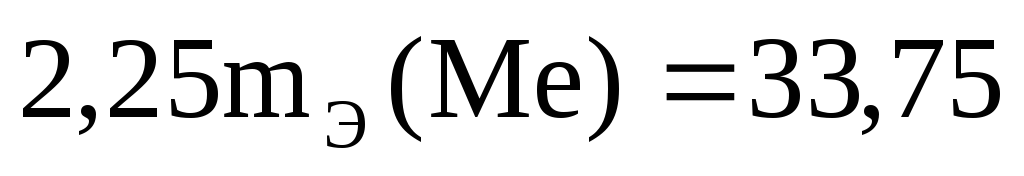
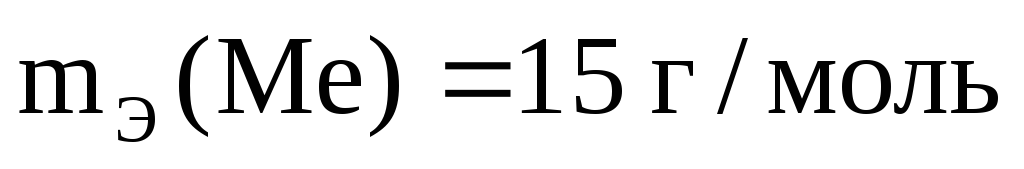
Эквивалент. Часть 1. Эквивалент элемента. Задачи.
Источник: studfile.net
Вычислить эквивалентную массу металла, если из 4,93 г хлорида металла по реакции с нитратом серебра получилось 8,61 г хлорида серебра.


⚡ Условие + 37% решения:
Вычислить эквивалентную массу металла, если из 4,93 г хлорида металла по реакции с нитратом серебра получилось 8,61 г хлорида серебра.
Решение: Эквивалентная масса хлорида серебра равна Согласно закону эквивалентов массы реагирующих друг с другом веществ пропорциональны их эквивалентным массам Кроме того, согласно закону эквивалентов эквивалентная масса хлорида металла равна сумме эквивалентных масс металла и кислотного остатка (хлорида). Записываем пропорцию
Готовые задачи по химии которые сегодня купили:
- Сколько миллилитров раствора А с заданной массовой долей ω (%) и плотностью ρ (г/мл) потребуется для нейтрализации раствора В, содержащего определенную массу m растворенного вещества (см. табл. 6).
- Дана схема реакции: HNO3 CaI2 Ca(NO3 ) 2 I 2 NO H2O 1) определите степень окисления атомов элементов, меняющих ее в процессе реакции; 2) составьте электронный баланс с учетом принципа равенства числа отдаваемых и принимаемых электронов, укажите процессы окисления и восстановления; 3) запишите множители в уравнение окислительно-восстановительной реакции как основные стехиометрические коэффициенты; 4) подберите стехиометрические коэффициенты остальных участников реакции; 5) выпишите формулы вещества – окислителя и восстановителя, рассчитайте их молярные массы эквивалентов.
- В 1 дм3 водного раствора содержится 0,4 г NaOH.
- Даны масса двухвалентного металла (mMe) и объем кислорода (VO2), затраченного на его окисление при н.у. (см. вариант в табл.1).
- Ряд судовых конструкций включает пары разнородных в электрохимическом отношении материалов
- Гидроксид Ме(ОН)3 имеет растворимость 1,1 ·10–3 г/дм3 , его молярная масса – 110 г/моль.
- Рассчитайте степень окисления Mo в соединениях: Ag2MoO4, (NH4)2MoO4, K5[Mo(CN)7], K4Mo2(SO4)4, MoO(SO4)2 и укажите правильный ответ.
- Напишите молекулярное и ионно-молекулярное уравнения реакции гидролиза соли Al(NO3)3.
- Впервые широкое применение для защиты от коррозии подводной части кораблей военно-морского флота получили цинковые протекторы в Канаде в 1945 году
- Больному ввели 10 мл 10 %-го раствора хлорида кальция (ρ = 1,2 г/мл) внутривенно.





















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
Источник: lfirmal.com
Закон эквивалентов. Понятие эквивалент. Молярная масса эквивалента
Одним из основных законов химии является закон эквивалентов, открытый в конце 18 века: массы элементов, соединяющихся друг с другом, пропорциональны их эквивалентам:
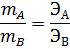
где mA, mВ – массы взаимодействующих веществ А и В;
ЭА и ЭВ – эквиваленты этих веществ.
Эквивалент – это реальная или условная частица, которая в кислотно-основных реакциях ионного обмена равноценна одному атому или одному иону водорода, а в окислительно-восстановительных реакциях одному электрону.
Массу одного моля эквивалента элемента называют молярной массой эквивалента MЭ(X). Значение эквивалента веществ зависит от того, в какой конкретной реакции участвует это вещество.
Молярная масса эквивалента химического элемента (MЭ(X)), а также простых или сложных веществ рассчитывается по формуле
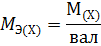
где M(X) – молярная масса; вал – суммарная валентность.
Для простых веществ суммарная валентность определяется произведением валентности атома химического элемента и числа атомов. Так, молярная масса эквивалента алюминия составляет MЭ(AI) = 27/3 = 9г моль -1 . Молярные массы эквивалента кислорода и водорода следует запомнить, они равны соответственно MЭ(О) = 16/2=8г моль -1 , МЭ(Н) = 1/1 = 1 г моль -1 .
Молярные массы эквивалента сложных веществ вычисляются по их химическим формулам с учетом происходящих химических реакций.
К сложным веществам относятся оксиды, гидроксиды, соли.
Суммарная валентность оксидов равна произведению валентности кислорода (2) на количество атомов кислорода в молекуле. Суммарная валентность гидроксидов определяется их кислотностью, которая равняется числу замещенных гидроксильных групп. Суммарная валентность кислот равняется основности данных соединений, которая определятся числом замещенных атомов водорода. Суммарная валентность соли равняется произведению валентности катиона и количества катионов в молекуле, или валентности аниона и количества анионов в молекуле.
Молярная масса эквивалентов сложных веществ может быть определена как сумма молярных масс эквивалентов элементов или условных частиц, образующих данное вещество.
Мэ (оксиды) = Мэ (О) + Мэ (элемента) = 8 + Мэ (элемента), т.к. Мэ кислорода величина постоянная, равна 8г моль -1 .
Мэ (кислота) = Мэ (Н) + Мэ (кислотного остатка) = 1 + Мэ (кислотного остатка), т.к. Мэ водорода величина постоянная, 1г моль -1
Мэ (гидроксиды) = Мэ (OH — ) + Мэ (металла) = 17 + Мэ (металла), т.к. Мэ “OH” групп величина постоянная, равна 17г моль -1 .
Мэ (соли) = Мэ (катиона) + Мэ (кислотного остатка).
Пример 1. Выразите в молях: а) 6,0210 21 молекул CO2; б) 1,2010 24 атомов кислорода; в) 2,0010 23 молекул воды. Чему равна мольная (молярная) масса указанных веществ?
Решение. Моль – это количество вещества, в котором содержится число частиц любого определенного сорта, равное постоянной Авогадро (6,02 10 23 ). Отсюда:
а) 6,0210 21 , т.е. 0,01 моль; б) 1,20 10 24 , т.е. 2 моль; в) 2,00 10 23 м, т.е. 1/3 моль.
Так как молекулярные массы СО2 и H2O и атомная масса кислорода соответственно равны 44; 18 и 16 а.е.м., то их мольные (молярные) массы равны: а) 44 г/моль; б) 18 г/моль; в) 16 г/моль.
Пример 2. Определите эквивалент (Э) и эквивалентную массу МЭ (Х) азота, серы и хлора в соединениях NHз,H2S и HCl.
Решение. Масса вещества и количество вещества – понятия неидентичные. Масса выражается в килограммах (граммах), а количество вещества – в молях.
В данных соединениях с 1 моль атомов водорода соединяется 1/3 моль азота,1/2 моль серы и 1 моль хлора. Отсюда Э(N) = 1/3 моль, Э(S) = 1/2 моль, Э(Cl) = 1 моль. Исходя из мольных масс этих элементов определяем их эквивалентные массы:
Пример 3. На восстановление 7,09 г оксида двухвалентного металла требуется 2,24 л водорода (н.у.). Вычислите эквивалентную массу оксида и эквивалентную массу металла. Чему равна атомная масса металла? Нормальные условия по Международной системе единиц (СИ): давление 1,013 10 5 Па (760 мм рт. ст. = 1 атм), температура 273 К или 0 0 С.
Решение. Согласно закону эквивалентов массы (объемы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объемам):
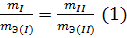
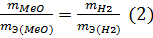
Если одно из веществ находится в газообразном состоянии, то, как правило, его количество измеряется в объемных единицах (см 3 , л, м 3 ).
Объем, занимаемый при данных условиях мольной или эквивалентной массой газообразного вещества, называется мольным или, соответственно, эквивалентным объёмом этого вещества. Мольный объём любого газа при н.у. равен 22,4 л. Отсюда эквивалентный объём водорода VmЭ (Н2) = 22,4/2 = 11,2 л, а эквивалентный объём кислорода равен 5,6 л.
В формуле (2) отношение mН2/mЭ(Н2) заменяем равным ему отношением VН2/VmЭ(Н2), где VН2 — объём водорода, VmЭ(MeO) — эквивалентный объём водорода:
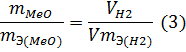
Из уравнения (3) находим эквивалентную массу оксида металла mЭ (МеО):
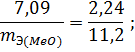
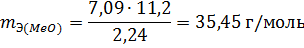
Согласно закону эквивалентов mЭ (МеО) = mЭ (Ме) + mЭ (О2), отсюда
Мольная масса металла определяется из соотношения mЭ = А/В,
где mЭ — эквивалентная масса, А — мольная масса металла, В- стехиометрическая валентность элемента; А = mЭ В = 27,452 = 54,9 г/моль. Так как атомная масса в а.е.м. численно равна мольной (молярной) массе, выражаемой в г/моль, то искомая атомная масса металла 54,9 а.е.м.
Пример 4. Вычислите эквиваленты и эквивалентные массы H2SО4 и Аl(OH)3 в реакциях, выраженных уравнениями:
Решение. Эквивалент (эквивалентная масса) сложного вещества, как и эквивалент (эквивалентная масса) элемента, может иметь различные значения и зависит от того, в какую реакцию обмена вступает это вещество. Эквивалентная масса кислоты (основность) равна мольной массе (М), деленной на число атомов водорода, замещенных в данной реакции на металл (на число вступающих в реакцию гидроксильных групп).
Пример 5. Сколько металла, эквивалентная масса которого 12,16 г/моль, взаимодействует с 310 см 3 кислорода (н.у.)?
Решение. Так как молярная масса О2 (32 г/моль) при н.у. занимает объем 22,4 м, то объем молярной массы эквивалента кислорода (8 г/моль) будет равен 22,4/4 = 5,6 = 5600 см 3 . По закон эквивалентов
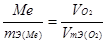 или
или 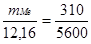 ,
,
откуда тМе = 12,16? 310/5600 = 0,673 г.
Пример 6. Из 3,85 г нитрата металла получено 1,60 г его гидроксида. Вычислите молярную массу эквивалента металла (тЭ(Ме) ).
Решение. При решении задачи следует иметь в виду:
а) молярная масса эквивалента гидроксида равна сумме молярных масс эквивалентов металла и гидроксильной группы;
б) молярная масса эквивалента соли равна сумме молярных масс эквивалентов металла и кислотного остатка. Вообще молярная масса эквивалента химического соединения равна сумме молярных масс эквивалентов составляющих его частей.
Учитывая сказанное, подставляем соответствующие данные в уравнение (1) примера 3:
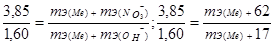
Пример 7. В какой массе Са(ОН)2 содержится столько же эквивалентных масс, сколько в 312 г А1(ОН)3?
Решение. Молярная масса эквивалента А1(ОН)3 равна 1/3 его молярной массы, т.е. 78/3 = 26 г/моль. Следовательно в 312 г А1(ОН)3 содержится 312/26 =12 эквивалентов. Молярная масса эквивалента Са(ОН)2 равна ½ его молярной массы, т.е.
37 г/моль. Отсюда 12 эквивалентов составляют 37 г/моль? 12 моль = 444 г.
Пример 8. Вычислите абсолютную массу молекулы серной кислоты в граммах.
Решение. Моль любого вещества содержит постоянную Авогадро NA структурных единиц (в нашем примере молекул). Молярная масса H2SO4 равна 98,0 г/моль. Следовательно, масса одной молекулы 98/(6,0210 23 ) = 1,6310 -22 г.
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Источник: studopedia.ru