Хлори́д на́трия(хлористый натрий, поваренная соль, столовая соль, пищевая соль, каменная соль, галит), натриевая соль соляной кислоты , NaCl (в природе – минерал галит ), бесцветные кристаллы ; tпл801 °С, плотность 2161 кг/м 3 . Хлорид натрия хорошо растворяется в воде (35,8 г на 100 г H2O при 20 °C); растворимость в воде мало зависит от температуры; в присутствии других солей растворимость в воде сильно снижается. В интервале от –21,2 до 0,15 °C из водного раствора кристаллизуется дигидрат NaCl·2H2O (плотность 1600 кг/м 3 ). Насыщенный водный раствор NaCl кипит при 108,7 °C. Растворяется в жидком NH3, спиртах , этиленгликоле , муравьиной кислоте . Чистый хлорид натрия мало гигроскопичен , в присутствии примесей (например, солей магния) гигроскопичность сильно повышается.

Хлорид натрия, содержащийся в плазме крови и тканевых жидкостях организма (концентрация 0,9 % по массе), является важнейшим компонентом, поддерживающим осмотическое давление плазмы крови и внеклеточной жидкости. Сростки кристаллов галита. Фото: Anna Suslina / Shutterstock Сростки кристаллов галита. Фото: Anna Suslina / Shutterstock При дефиците NaCl в организме наблюдается сгущение крови, могут развиться спазмы гладкой мускулатуры, судорожные сокращения скелетных мышц, нарушения функций нервной системы и кровообращения. При некоторых заболеваниях (почек, гипертонической болезни ) ограничивают поступление NaCl в организм.
СОЛИ ХИМИЯ 8 КЛАСС // Урок Химии 8 класс: Классификация солей, Формулы Солей, Кислотный Остаток
Хлорид натрия получают из природного сырья ( каменная соль ) закрытым способом (реже открытым) с применением подземного выщелачивания . Самосадочная соль добывается из соляных озёр механическим путём, осадочную соль получают естественным испарением морских и озёрных соляных рассолов, выварочную соль (наиболее чистую) – упариванием соляных рассолов в выпарных аппаратах. Применяют как пищевой продукт, консервант мяса , рыбы и др., химическое сырьё в производстве различных веществ и материалов (Na2CO3, Cl2, NaOH и др.). Водные растворы хлорида натрия ( изотонический и гипертонический) используются в медицинской практике.
Аликберова Людмила Юрьевна . Первая публикация: Большая российская энциклопедия, 2013.
в 11:59 (GMT+3) Обратная связь
Информация
Области знаний: Неорганическая химия, Неорганические соединения Другие наименования: Хлористый натрий, Поваренная соль, Столовая соль, Пищевая соль, Каменная соль, Галит Брутто-формула: NaCl Молярная масса: 58,44277 г/моль Температура плавления: 801 °C Температура кипения: 1465 °C Агрегатное состояние: Твёрдое Плотность при н. у.: 2,161 г/см³
Источник: bigenc.ru
Урок 25. Соли
В уроке 25 «Соли» из курса «Химия для чайников» узнаем, как правильно называть соли, их состав и научимся составлять химические формулы солей.
Чем морская соль отличается от поваренной соли?

Как отмечалось в предыдущем уроке, в реакциях кислот с металлами выделяется простое вещество водород Н2. Кроме водорода, образуются и сложные вещества: ZnCl2, MgSO4и др. Это представители класса широко распространенных в химии соединений — солей(рис. 102).

Здесь же мы рассмотрим состав солей, научимся составлять их формулы, узнаем, как называть соли.
Cостав солей
Сравним формулы кислот HCl и H2SO4c формулами солей ZnCl2и FeSO4. Мы видим, что в этих формулах одинаковые кислотные остатки Cl(I) и SO4(II). Но в молекулах кислот они соединены с атомами водорода Н, а в формульных единицах солей — с атомами цинка Zn и железа Fe. Значит, эти и другие соли можно рассматривать как продукты замещения атомов водорода в молекулах кислот на атомы металлов. Вещества, подобные ZnCl2и FeSO4, относят к классу солей.
Соли— это сложные вещества, состоящие из атомов металлов и кислотных остатков.
В солях кислотные остатки соединяются с атомами металлов в соответствии с их валентностью. Для составления химической формулы соли необходимо знать валентность атома металла и валентность кислотного остатка. При этом пользуются тем же правилом, что и при составлении формул бинарных соединений. Для солей это правило следующее: сумма единиц валентности всех атомов металла должна быть равна сумме единиц валентности всех кислотных остатков.
Для примера составим формулу соли, в которую входят атомы кальция и кислотный остаток фосфорной кислоты PO4(III). Кальций проявляет постоянную валентность II, а валентность кислотного остатка PO4равна III.

Названия солей
Соли образованы атомами разных металлов и различными кислотными остатками. Поэтому состав солей самый разнообразный. Давайте научимся давать им правильные названия.
Название соли состоит из названия кислотного остатка и названия металла в родительном падеже. Например, соль состава NaCl называют «хлорид натрия».
Если входящий в формульную единицу соли атом металла имеет переменную валентность, то она указывается римской цифрой в круглых скобках после его названия. Так, соль FeCl3 называют «хлорид железа(III)», а cоль FeCl2 — «хлорид железа(II)».
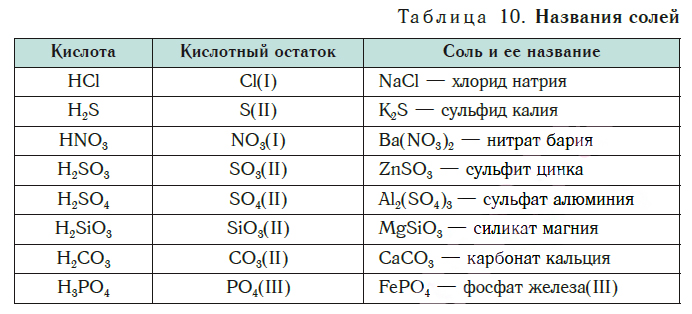
В таблице 10 приведены названия некоторых солей.
Соли — это вещества немолекулярного строения. Поэтому их состав выражают с помощью формульных единиц. В них отражено соотношение атомов металлов и кислотных остатков. Например, в формульной единице NaCl на один атом Na приходится один кислотный остаток Cl.
По химической формуле соли можно вычислить ее относительную формульную массу Mr, а также молярную массу M, например:
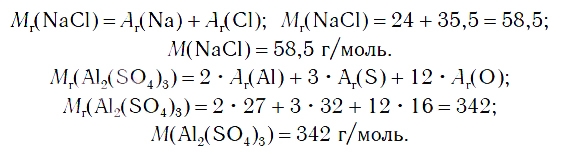
К солям относится не только поваренная соль (NaCl), но и мел, мрамор (СаСО3), сода (Na2CO3), марганцовка (KMnO4) и др.
Краткие выводы урока:
- Соли — сложные вещества, которые состоят из атомов металлов и кислотных остатков.
- Соли образуются при замещении атомов водорода в молекулах кислот на атомы металлов.
- Соли — вещества немолекулярногостроения.
Надеюсь урок 25 «Соли» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Источник: himi4ka.ru
Какая формула поваренной соли? Какая химическая формула поваренной соли?
Кто хоть немного знает химию, просто непременно должен знать химическую формулу самого употребляемого продукта и одного из самого важного для поддержания нашей жизни. Без него могут нарушится обмен веществ, водяной баланс и многое другое. Формула соли такая — NaCl или хлористый натрий.

автор вопроса выбрал этот ответ лучшим
комментировать
в избранное ссылка отблагодарить
Чёрна я Луна [267K]
10 месяцев назад
В нашем мире существует множество солей. Солями в химии называют вещества, которые сочетают в себе атомы металла и кислотные остатки. Например, СаCl2, Na2SO4, H3PO4, HBr.
Поваренная соль — это самая распространенная соль на нашей планете, как и другие соли она состоит из атомов металла и кислотного остатка. Поваренную соль добывают путем добычи полезных ископаемых или методом испарения растворов с солью.
Так же это вещество можно получить из натрия и хлороводородной кислоты. 2Na + 2HCl = 2NaCl + H2↑. В результате реакция получается две молекулы NaCl. Это и есть формула поваренной соли, состоящее из металла (Na) и Кислотного остатка (Cl).
комментировать
в избранное ссылка отблагодарить
З В Ё Н К А [827K]
9 лет назад
Химическое вещество, которое в народе прозвали «поваренной солью», имеет и другое, более научное название (химическое название): хлорид натрия (или — хлористый натрий). Формула этого вещества очень проста: NaCl.

в избранное ссылка отблагодарить
Михаиллл [9.1K]
Поваренная соль НЕ разлагается в организме человека на Na и Cl. По отдельности эти элементы ядовиты. А Натрий необходим, но в других сочетаниях и количествах. Так, что я не согласен с картинкой! А с ответом солидарен 🙂 — 9 лет назад
Rafail [136K]
Михаиллу.
А никто и не утверждает, что она разлагается на атомы Na и Cl. Она изначально состоит из ионов Na(+) и Cl(-), и именно на них она распадается в водных растворах (правда не «голые», а гидратированные), и именно в виде ионов она присутствует в нашем организме. В тексте на картинке (и вообще во всех медицинских, и биологических текстах) под термином натрий понимают именно ион натрия. Все об этом знают, к этому привыкли, и специально не указывают, что речь идет именно об ионах. Вы один оказывается этого не знали, и решили оспаривать текст на картинке.
Кстати, когда во всяких рекламах, говорят о кальции, магнии, калии. то речь идет тоже именно об ионах, а никак не о металлах, как таковых. — 9 лет назад
Источник: www.bolshoyvopros.ru