Кремний- элемент 4-й группы, имеет кубическую кристаллическую решетку с ковалентными связями. Устойчив при нагреве на воздухе до 900 0 С, затем активно окисляется.
1. оптимальная температура плавления 1420 0 С. При более низкой температуре не возможно было бы проводить диффузию, протекающую при 1220 0 С, а при более высокой создало бы проблемы для материалов петлей и реакторов.
2.достаточная ширина запрещенной зоны обеспечивает хороший температурный диапазон -60-+130 0 С
3. возможность получения на поверхности Si собственного окисла SiO2, обладающего хорошими защитными свойствами.
1. не обладает излучательной способностью (не пригоден для ОКГ и светодиодов)
2. невысокая подвижность носителей, что препятствует созданию на нем сверхвысокочастотных приборов.
3. высокая химическая активность в расплавленном состоянии
4. наличие трудноудаляемых примесей (бор), температура плавления которого значительно выше (2300 0 С)
5. невысокая радиационная стойкость.
Как производят Процессоры: Кремниевые Пластины
Получение поликристаллического чистого кремния:
. водородным восстановлением из хлорсиланов (тетрахлорида кремния SiCl4 или трихлорсилана)
2. термическим разложением (получение поликристаллических пленок) моносилана Si H4 SiH4→Si+2H2
1. метод Чохральского (диаметр слитков до 100,150мм)
2. метод бестигельной зонной плавки, диаметр до 60 мм.
Наибольшее распространение для получения монокристаллов полупроводниковых материалов получил метод Чохральского.
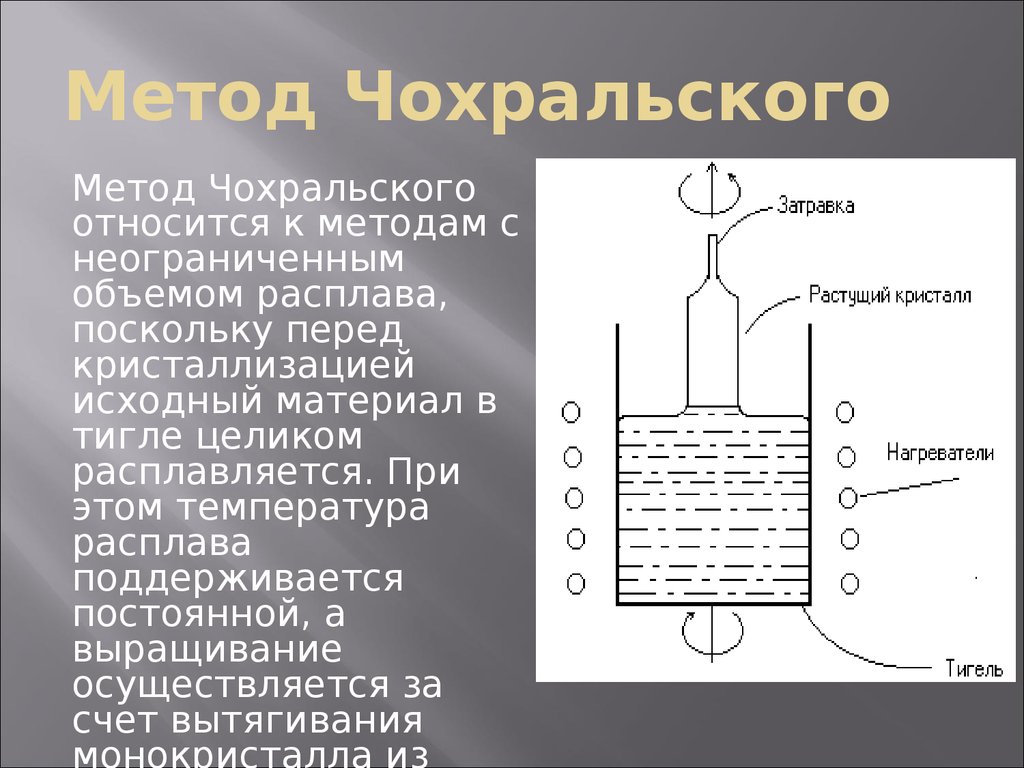
Сущность метода: на монокристаллическую затравку нарастает кристалл в точности повторяющий кристаллографическую ориентацию в самой затравке.
Основные стадии процесса:
- плавление поликристаллической загрузки
- оплавление монокристаллической затравки и кристаллизация на ней первых порций расплава
- подъем затравки и вытягивание щетки
- разращивание монокристалла до номинального диаметра
- рост монокристалла постоянного диаметра
- оттяжка на конус, обрыв кристалла
- охлаждение выращенного монокристалла
Бестигельная зонная плавка.
Метод Чохральского применяют, в основном, для получения крупных монокристаллов с относительно небольшим удельным сопротивлением (ρ
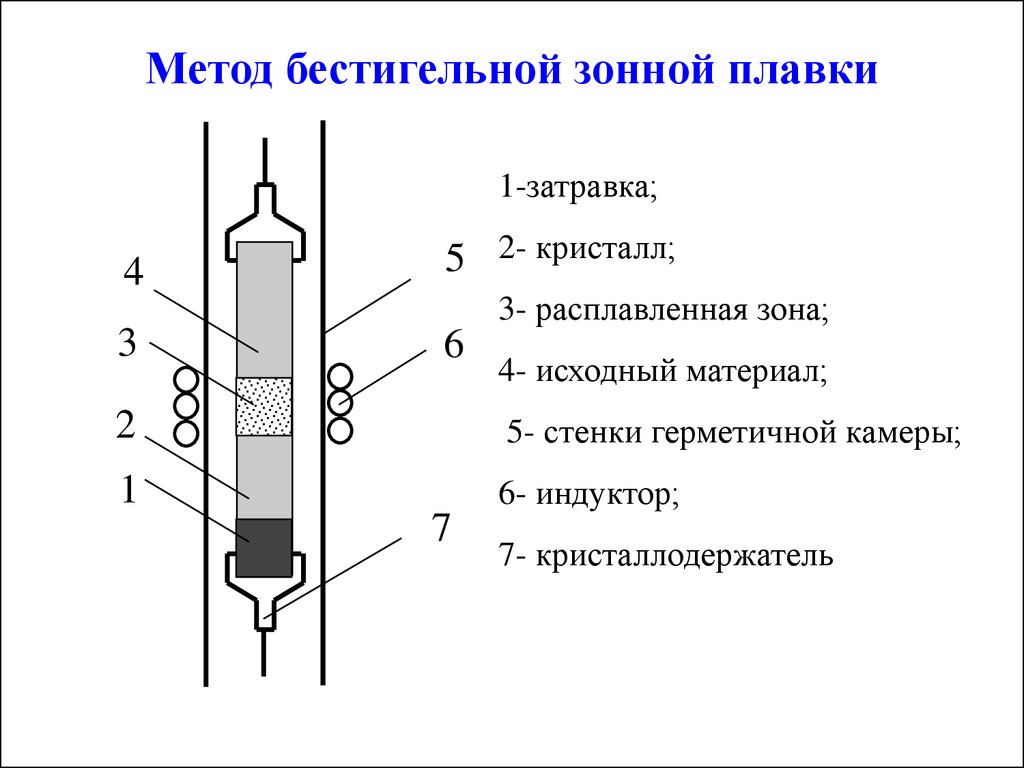
При этом методе узкая зона расплава удерживается между твердыми частями слитка за счет сил поверхностного натяжения.
Использование метода возможно при малой плотности и большом коэффициенте поверхностного натяжения в жидком материале.
Эти условия имеют место в жидком Si.
Для получения монокристаллов в Ge этот метод нельзя использовать из-за большой плотности и малого поверхностного натяжения. Диаметр получаемого слитка
Можно выращивать этим методом однородные монокристаллы диаметром до 60-76 мм, а при использовании индуктора, диаметр которого меньше диаметра проплавляемого стержня- до 100 мм.
🔥 КРЕМНИЙ из ПЕСКА. Эксперименты с песком.
Процесс плавки можно проводить в вакууме и в атмосфере инертных газов. Плавка в водороде используется тогда, когда проводится одновременное легирование из газовой фазы. В этом случае водород служит газом-носителем.
Этапы процесса бестигельной зонной плавки:
- разогрев торца кремниевого стержня
- образование висячей капли расплава кремния
- оплавление затравки
- выращивание щетки (начальная стадия роста монокристалла)
- проведение процесса в установившемся режиме
К недостаткам метода следует отнести:
1. сложная дорогостоящая аппаратура.
2. меньшая производительность, чем при методе Чохральского.
3. более высокая стоимость.
Толщина пластин кремния составляет 400 мкм при диаметре до 76 мм. В США 625 мм при диаметре 100-150 мм.
Источник: studfile.net
Как получить чистый кремний
![]()
Цинкотермическое восстановление тетрахлорида кремния
Получение мелкокристаллического кремния этим способом основано на реакции, впервые предложенной знаменитым физико-химиком Н.Н. Бекетовым. Способ заключается в восстановлении парообразных галогенидов кремния парами активных металлов, например цинка, магния, алюминия и др.
Преимущества цинка как восстановителя следующие:
1) цинк не образует соединений с кремнием и почти нерастворим в нем;
2) высокая упругость паров цинка облегчает проведение реакции восстановления;
3) хлорид цинка — продукт реакции восстановления — в условиях процесса также находится в парообразном состоянии (температура кипения ZnCl2~732°C) и поэтому легко удаляется из зоны реакции;
4) при восстановлении SiCl4 цинком реакция протекает при наличии трех газообразных продуктов:
SiCl4 (газ) + 2Zn (газ) → Si (тв) + 2ZnCl2 (газ),
что обусловливает более легкое отделение от них восстановленного кремния.
Восстановление тетрахлорида кремния цинком осуществляют в кварцевом реакторе (рис. 130), в который с одной стороны введены трубки от испарителя цинка и испарителя SiCl4, а с другой — присоединен конденсатор-сборник хлорида цинка и непрореагировавших продуктов реакции.
Реактор нагревается до 1000—1100°C, испаритель цинка и транспортирующая его трубка — до 950—1000°C, испаритель тетрахлорида — до 30—60°С, а транспортирующий змеевик — до 650—1000°C.
Кварцевый реактор, соединенный с конденсатором и испарителями, устанавливают в печь с селитовыми нагревателями на подставки из пеношамота с наклоном в сторону конденсатора ZnCl2.

На рис. 131 показано влияние скорости подачи цинка на степень использования SiCl4 и цинка.
Кремний образуется в виде игольчатых кристаллов различной крупности, спеков, мелких кристаллов и пленок. Характер и вид получаемого кремния зависят от скорости подачи цинка и SiCl4 в реакционное пространство.

SiCl4 + 2H2 → Si + 4HCl.
Этот метод широко используется в производстве полупроводникового кремния. Перед цинкотермическим метод водородного восстановления обладает рядом преимуществ;
1) восстановитель (водород) может быть более глубоко очищен от примесей, чем цинк;
2) кремний в процессе восстановления не соприкасается с кварцем, что исключает дополнительные загрязнения кремния примесями, содержащимися в кварцевой аппаратуре;
3) при водородном восстановлении получается компактный кремний более высокой степени чистоты, чем при цинкотермическом восстановлении.
При водородном восстановлении кремния особенно большое внимание уделяют очистке водорода. С целью очистки водород пропускают через платинированный асбест, силикагель и активированный уголь, охлаждаемый жидким азотом. Исходный тетрахлорид кремния очищают ректификацией.

Установка, применяемая для получения кремния водородным восстановлением SiCl4, показана на рис. 132. Она состоит из системы очистки водорода, испарителя тетрахлорида кремния, реактора и откачивающей системы.
Реактор представляет собой кварцевый охлаждаемый водой колпак, в который через нижнюю крышку введены электроды, соединенные с танталовой или молибденовой проволокой. В реактор введены также трубки для ввода смеси тетрахлорида кремния и водорода и для отвода избытка водорода и продуктов реакции.
Водород вводят в реактор с большим избытком, так как при стехиометрическом соотношении выход кремния очень низок. Это объясняется тем, что образующийся при восстановлении кремния хлороводород снижает парциальное давление водорода и реакция затухает. Поэтому восстановление ведут при 50—60-кратном избытке водорода сверх стехиометрического количества.
Восстановление тетрахлорида кремния водородом осуществляется непосредственно на нагретой до 1050—1100°C танталовой или молибденовой проволоке, на которой кремний осаждается в виде плотного поликристаллического слоя, диаметр которого постепенно увеличивается и к концу процесса достигает 35—40 мм.
Снятый с тантала или молибдена кремний подлежит травлению перед плавкой. В качестве травителя применяют смесь кислот HF + HNO3 + Hg(NO3)2. Травление осуществляют на глубину 0,1 мм для удаления с поверхности кремния, которая соприкасается с проволокой, примесей тантала или молибдена, а также следов магния, железа и меди.
Вместо танталовой или молибденовой проволоки можно применять стержни из чистого кремния и на них вести осаждение кремния. В этом случае кремний после восстановления можно направлять на вытягивание без предварительного травления. Кремний, полученный этим методом, имеет удельное электросопротивление около 1000 ом*см.
Восстановление трихлорсилана водородом
Восстановление трихлорсилана водородом осуществляется по реакции
SiHCl3 + H2 ⇔ Si + 3НСl,
которая протекает при 1000—1100°C. Восстановление трихлорсилана водородом может осуществляться на установке, аналогичной для восстановления тетрахлорида кремния (рис. 132). Вначале из реактора тщательно откачивают воздух и всю систему промывают водородом. Характер протекания реакции взаимодействия трихлорсилана с водородом зависит от соотношения количеств водорода и трихлорсилана, вводимых в реактор.
При стехиометрическом соотношении или малом избытке водорода реакция разложения силана протекает с незначительным выходом аморфного кремния. С увеличением отношения подаваемого водорода к трихлорсилану выход кремния возрастает, при 45—50-кратном избытке водорода достигается максимальное извлечение кремния, который осаждается на нагретой поверхности в кристаллическом виде. Кремний в этом процессе, как и при восстановлении тетрахлорида кремния, осаждается на нагретых танталовой или молибденовой проволоке или на кремниевых стержнях.
Этим способом, особенно при осаждении на кремнии, получается очень чистый поликристаллический кремний с удельным электросопротивлением около 2500—3000 ом*см, более чистый, чем при водородном восстановлении тетрахлорида кремния. Это объясняется главным образом более высокой чистотой трихлорсилана, который поддается более глубокой очистке от примесей методом ректификации, чем SiCl4. При этом исходный технический трихлорсилан при получении его методом гидрохлорирования содержит примесей меньше, чем технический тетрахлорид кремния, так как гидрохлорирование кремния протекает при значительно более низкой температуре, чем хлорирование кварца или технического кремния, с получением SiCl4, одновременно с которым хлорируются почти все примеси, содержащиеся в исходных продуктах.
Кроме того, на трихлорсилановый метод расходуется меньше водорода и достигается больший коэффициент использования газовой смеси, что объясняется величинами констант равновесия реакций восстановления трихлорсилана водородом.
Силановый метод получения кремния
Весьма перспективным методом получения кремния высокой степени чистоты является термическое разложение моносилана, которое протекает по реакции
SiH4 → Si + 2Н2.
Достаточно быстрое и полное разложение SiH4 происходит при 600—700° С.
Для получения моносилана применяют несколько методов. Один из них основан на реакции взаимодействия литий-алюминийгидрида с тетрахлоридом кремния:
LiAlH4 + SiCl4 → SiH4 + LiCl + AlCl3.
Для реакции используются предварительно глубокоочищенные LiAlH4 и SiCl4. Реакцию проводят в эфире, в котором литий-алюминийгидрид хорошо растворяется. Это обеспечивает больший выход и более спокойное течение реакции.
Моносилан, получаемый этим способом, сразу очищается от бора, так как треххлористый бор, который может присутствовать в тетрахлориде кремния, хорошо реагирует с литий-алюминийгидридом с образованием литий-боргидрида — соединения, характеризующегося низкой упругостью пара:
LiAlH4 + BCl3 → LiBH4 + AlCl3.
При отгонке моносилана LiBH4 остается в растворе.
Другой метод получения моносилана — разложение триэтоксисилана в присутствии натрия:
4SiH(OC2H5) → SiH4 + 3Si(OC2H5)4.
Эта реакция протекает при небольшом нагревании до 80°С.
Триэтоксисилан получают при взаимодействии трихлорсилана со спиртом:
SiHCl3 + 3С2Н5ОН → SiH (OC2H5)3 + 3НСl
с последующей отгонкой фракций, кипящих при 130— 140°С.
Очистку моносилана осуществляют вымораживанием примесей при температуре (-100)/(-110°C). Дополнительную очистку силана осуществляют путем предварительного разложения. С этой целью моносилан пропускают через дополнительный реактор, нагреваемый до более низкой температуры, чем основной. В дополнительном реакторе разлагаются менее устойчивые гидриды.
На рис. 133 показана схема установки для разложения моносилана, в которой совмещены получение, очистка и разложение SiH4. Моносилан здесь получают разложением триэтоксисилана в присутствии натрия. Образующийся моносилан проходит через ловушки, охлаждаемые жидким азотом, и реактор предварительного разложения, после чего попадает в основной реактор для разложения.

Основной реактор представляет собой кварцевый охлаждаемый водой колпак, в который через нижнюю крышку введены электроды для нагрева танталовой ленты, а также трубки для подачи силана и отвода газообразных продуктов реакции.
Разложение силана происходит на танталовой ленте, нагретой до 900—800° С, на которую силан подается из щели, прорезанной в кварцевой трубке для подачи силана.
Кремний выделяется в виде мелких кристалликов, образующих компактный стержень, легко отделяющийся от тантала. Газообразные продукты, выходящие из реактора, дополнительно подогреваются до 1100°C с целью доразложения неразложившегося моносилана.
Установка должна быть герметичной. Перед началом реакции из нее откачивают воздух и затем промывают водородом. Кремний, полученный этим способом, характеризуется высоким удельным электросопротивлением, которое составляет несколько сот тысяч ом-сантиметров.
Однако большим препятствием для применения этого способа в крупных масштабах является взрывоопасность.
Йодидный метод получения кремния
В основе этого метода лежит обратимая химическая транспортная реакция синтеза и термического разложения SiI4:
Si + 2I2 ⇔ SiI4,
позволяющая осуществлять процесс получения кремния в замкнутом цикле и разомкнуто. При 700—800° С реакция идет в сторону образования тетрайодида кремния из элементов. При переходе к более высоким температурам (1100—1200° С) равновесие реакции смещается в сторону выделения чистого кремния.
В связи с обратимостью приведенной реакции йодид-ный метод имеет два варианта. По первому — синтез и разложение тетраиодида совмещены в одном аппарате, и процесс является замкнутым. По второму, разомкнутому, процессу синтез и разложение тетрайодида кремния происходят в различных аппаратах; при этом синтезированный тетрайодид кремния подвергают очистке от примесей.


Si + 2I2 ⇔ SiI4
вправо, и увеличивалось бы время контакта йода с кремнием.
Тетрайодид кремния имеет вид прозрачных бесцветных или слегка окрашенных кристаллов.
Очищать SiI4 можно ректификацией, зонной плавкой или перекристаллизацией в органических растворителях. Коэффициент распределения бора в SiI4 равен 0,16. Это позволяет при зонной плавке тетрайодида кремния очистить его от бора.
Очищенный SiI4 затем разлагают в аппарате, показанном на рис. 136.

Аппарат состоит из кварцевого реактора, соединенного с испарителем SiI4 вакуумной системой и конденсатором для сбора выделяющегося йода и остатков непрореагировавшего SiI4. Разложение тетрайодида осуществляется в глубоком вакууме 1*10-5 мм рт. ст. на танталовой нити, нагретой до 1100—1200°С. Осажденный кремний после отделения от танталовой спирали представляет собой куски неправильной формы.
При разложении предварительно полученного и очищенного SiI4 кремний может быть также в виде стержней на установке, приведенной на рис. 137. Реактор представляет собой кварцевую трубу, в которую вставлена другая кварцевая труба меньшего диаметра, внутри покрытая танталовой фольгой.
Вначале в системе создают вакуум 1*10в-5 мм рт. ст., затем, после нагрева реактора до рабочей температуры 1100°C, нагревают испаритель SiI4 до температуры, немного превышающей температуру плавления тетрайодида (—122° С).

Разложение SiI4 происходит во внутренней трубе. Кремний осаждается на танталовой фольге и в зависимости от продолжительности процесса формируется или в виде трубок с различной толщиной стенок, или в виде стержней. Последние после окончания реакции и охлаждения печи извлекают и отделяют от тантала путем травления плавиковой кислотой или смесью плавиковой и азотной кислот. Этот способ позволяет получать кремний высокой чистоты. Монокристаллы, полученные из этого кремния вытягиванием, обладают сопротивлением до несколько сот ом-сантиметров,
- Получение и очистка соединений кремния
- Некоторые физико-химические свойства кремния и его соединений. Области применения чистого кремния
- Получение монокристаллов германия с равномерными свойствами методом горизонтального зонного выравнивания
- Получение монокристаллов германия с равномерными электрофизическими свойствами вытягиванием из расплава
- Получение монокристаллов германия
- Получение поликристаллического германия высокой чистоты
- Получение чистого поликристаллического германия
- Получение чистейшей двуокиси германия
- Применение германия
- Некоторые физико-химические свойства германия и его соединений
Источник: metal-archive.ru
Кремний
В промышленности кремний получают, восстанавливая расплав SiO2 водородом. Возможна также очистка кремния за счет предварительного получения силицида магния Mg2Si. Далее из силицида магния с помощью [1] — кремний производится на заводах в г. Физические свойства [ ]
Кристаллическая структура кремния.
Кристаллическая решетка кремния кубическая гранецентрированная типа Файл:Зонная структура Si.png
Схематическое изображение зонной структуры кремния [1]
Электрофизические свойства [ ]
Элементарный кремний — типичный непрямозонный полупроводник. Ширина запрещенной зоны при комнатной температуре 1,12 эВ, а при Т = 0 К составляет 1,21 эВ [2] . Концентрация носителей заряда в кремнии с собственной проводимостью при комнатной температуре 1,5·10 16 м -3 . На электрофизические свойства кристаллического кремния большое влияние оказывают содержащиеся в нем микропримеси. Для получения монокристаллов кремния с дырочной проводимостью в кремний вводят добавки элементов III-й группы — бора, алюминия, галлия и индия, с электронной проводимостью — добавки элементов V-й группы — фосфора, мышьяка или сурьмы. Электрические свойства кремния можно варьировать, изменяя условия обработки монокристаллов, в частности, обрабатывая поверхность кремния различными химическими агентами.
Подвижность электронов 1400 см^2/(в*c).
Химические свойства [ ]
В соединениях кремний склонен проявлять фтором, при этом образуется летучий тетрафторид кремния SiF4. При нагревании до температуры 400—500°C кремний реагирует с кислородом с образованием хлором, бромом и иодом — с образованием соответствующих легко летучих тетрагалогенидов SiHal4.
Образующийся в этой реакции силан SiH4 содержит примесь и других силанов, в частности, азотом кремний при температуре около 1000 °C образует нитрид Si3N4, с бором — термически и химически стойкие углерода — магния типа Ca2Si, Mg2Si и др.) и металлоподобные (силициды переходных металлов). Силициды активных металлов разлагаются под действием кислот, силициды переходных металлов химически стойки и под действием кислот не разлагаются. Металлоподобные силициды имеют высокие температуры плавления (до 2000 °C). Наиболее часто образуются металлоподобные силициды составов MeSi, Me3Si2, Me2Si3, Me5Si3 и MeSi2. Металлоподобные силициды химически инертны, устойчивы к действию кислорода даже при высоких температурах.
При восстановлении SiO2 кремнием при высоких температурах образуется оксид кремния (II) SiO.
Для кремния характерно образование кремнийорганических соединений, в которых атомы кремния соединены в длинные цепочки за счет мостиковых атомов кислорода —О—, а к каждому атому кремния, кроме двух атомов О, присоединены еще два органических радикала R1 и R2 = CH3, C2H5, C6H5, CH2CH2CF3 и др.
Применение [ ]
Для некоторых организмов кремний является важным биогеным элементом. Он входит в состав опорных образований у растений и скелетных — у животных. В больших количествах кремний концентрируют морские организмы — диатомовые водоросли, радиолярии, губки.
Большие количества кремния концентрируют хвощи и злаки, в первую очередь — подсемейства Бамбуков и Рисовидных, в том числе — рис посевной. Мышечная ткань человека содержит (1-2)·10 -2 % кремния, костная ткань — 17·10 -4 %, кровь — 3,9 мг/л. С пищей в организм человека ежедневно поступает до 1 г кремния.
Соединения кремния относительно нетоксичны. Но очень опасно вдыхание См. также [ ]
- Категория:Соединения кремния
- Ссылки [ ]
Литература [ ]
- Самсонов. Г. В. Силициды и их использование в технике. Киев, Изд-во АН УССР, 1959. 204 стр. с илл.
- Алёшин Е.П., Алёшин Н.Е. Рис. Москва, 1993. 504 стр. 100 рис.
Примечания [ ]
- ↑ Р Смит., Полупроводники: Пер. с англ. — М.: Мир, 1982. — 560 с, ил.
- ↑ Зи С., Физика полупроводниковых приборов: В 2-х книгах. Кн. 1. Пер. с англ. — М.: Мир, 1984. — 456 с, ил.

| H | He | ||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | Xe | |
| Cs | Ba | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Uub | Uut | Uuq | Uup | Uuh | Uus | Uuo | |
| Uue | Ubn | ||||||||||||||||
| La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | |||
| Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr |
Эта страница использует содержимое раздела Википедии на русском языке. Оригинальная статья находится по адресу: Кремний. Список первоначальных авторов статьи можно посмотреть в истории правок. Эта статья так же, как и статья, размещённая в Википедии, доступна на условиях CC-BY-SA .
Источник: vlab.fandom.com