Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
- Обратная связь
- Правила сайта
Источник: www.soloby.ru
2.8 Алюминий и его сплавы
Алюминий – легкий металл с плотностью 2,7 г/см 3 и температурой плавления 660ºС. Имеет гранецентрированную кубическую решетку. Обладает высокой тепло- и электропроводностью. Химически активен, но образующаяся плотная пленка оксида алюминия Al2O3, предохраняет его от коррозии.
Алюминий. Учебный фильм — 1976
Технический алюминий хорошо сваривается, имеет высокую пластичность. Из него изготавливают строительные конструкции, малонагруженные детали машин, используют в качестве электротехнического материала для кабелей, проводов.
Принцип маркировки алюминиевых сплавов. В начале указывается тип сплава: Д – сплавы типа дюралюминов; А – технический алюминий; АК – ковкие алюминиевые сплавы; В – высокопрочные сплавы; АЛ – литейные сплавы.
Далее указывается условный номер сплава. За условным номером следует обозначение, характеризующее состояние сплава: М – мягкий (отожженный); Т – термически обработанный (закалка плюс старение); Н – нагартованный; П – полунагартованный.
3. Кристаллическое строение металлов
Все металлы в твердом состоянии имеют кристаллическое строение. Атомы в твердом металле расположены упорядочено и образуют кристаллические решетки (рис. 1).

Рис. 1. Схемы кристаллических решеток: а – объемно-центрированная кубическая; б – гранецентрированная; в – гексагональная плотноупакованная
Кристаллическая решетка представляет собой наименьший объем кристалла, дающий полное представление об атомной структуре металла, и носит название элементарной ячейки.
Для металлов характерны кристаллические решетки трех видов: кубическая объемно-центрированная (ОЦК), в которой атомы расположены по вершинам элементарной ячейки и один в ее центре (вольфрам W, молибден Mo, ванадий V, ниобий Nb, хром Cr и др., рис. 1а); кубическая гранецентрированная (ГЦК), в которой атомы расположены по вершинам элементарной ячейки и в центрах ее граней (медь Cu, никель Ni, серебро Ag, алюминий Al, платина Pt и др., рис.1б); гексагональная плотноупакованная (ГПУ), представляющая собой шестигранную призму, в которой атомы расположены в три слоя (магний Mg, лантан La, титан Ti, кадмий Cd и др., рис.1в).
Цинковые и алюминиевые сплавы Как отличить цинк силумин дюраль
Элементарные частицы в кристаллической решетке находятся во взаимодействии, определяемом их электронным строением. От характера этого взаимодействия зависят электрические, магнитные, тепловые и оптические свойства материала, его температура плавления и испарения, модуль упругости и другие свойства.
Существование одного и того же металла в нескольких кристаллических формах носит название полиморфизма или аллотропии. Перестройка кристаллических решеток при критических температурах называется полиморфными превращениями. Полиморфные модификации обозначают греческими буквами α, β, γ и другими, которые в виде индекса добавляют к символу элемента (например, Feα, Feβ). Полиморфную модификацию при самой низкой температуре обозначают буквой α, при более высокой β и т.д.
Всем кристаллам присуща анизотропия, т.е. неравномерность свойств по направлениям, определяемая различными расстояниями между атомами в кристаллической решетке. Наиболее сильно анизотропия выражена у металлов, имеющих ассиметричное кристаллическое строение. В таких кристаллах в зависимости от направление существенно изменяются показатели физических свойств, прочностные характеристики, коэффициент теплопроводности и электропроводимости.
Аморфные тела обладают свойством изотропии, т.е. имеют одинаковые свойства во всех направлениях.
Источник: studfile.net
Тип кристаллической решетки алюминия
Для решения задачи, мне нужно указать тип кристаллической решетки алюминия. Буду очень признателен тому, кто поможет мне в этом деле. А еще, нужны способы получения алюминия.
Xumuk Админ. ответил 6 лет назад
Отображением пространственной структуры монокристалла служит его кристаллическая решетка. Таким образом, различие геометрических форм кристаллов тех или иных веществ связано с особенностями симметрии их кристаллических решеток. Обычно оценивают следующие элементы симметрии в монокристалле: оси симметрии, плоскости симметрии и центры симметрии.
Если при повороте на определенный угол вокруг воображаемой оси кристаллическая решетка совмещается сама с собой, то это свидетельствует о наличии в кристалле оси симметрии. Если в кристалле можно провести одну или несколько плоскостей таким образом, что одна часть кристаллической решетки будет зеркальным отображением другой, значит в кристалле имеются плоскости симметрии. Наконец, когда отражение всех узлов решетки в какой-либо точке кристалла приводит к их совмещению, говорят о существовании центра симметрии.
Кристаллическая решетка представляет собой своего рода пространственный каркас, образованный пересекающимися прямыми линиями. В точках пересечения линий – узлах решетки – лежат центры частиц.
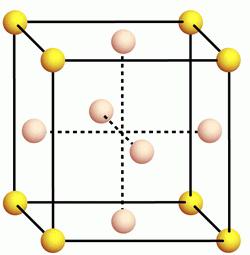
Тип кристаллической решетки алюминия — молекулярная гранецентрированная кубическая. Это означает, что в её узлах находятся молекулы. Они связаны друг с другом межмолекулярными силами.
Алюминий – металл, относится к элементам p-семейства. Электронная конфигурация алюминия выглядит следующим образом:
.
На внешнем энергетическом уровне алюминия находится 3 электрона, из которых один неспаренный. Два из вышеуказанных валентных электронов находятся на s-орбитали, а один – на p-орбитали. s- и p-уровни в изолированных атомах близки. Это означает, что соответствующие зоны в кристаллах алюминия перекрываются. Следовательно, число валентных электронов недостаточно для заполнения энергетических уровней перекрывающихся зон.
Таким образом, металлические кристаллы образуются элементами, в атомах которых число валентных электронов мало по сравнению, с числом энергетически близких валентных орбиталей. Вследствие этого химическая связь в металлических кристаллах сильно делокализована.
Источник: ru.solverbook.com