Вопрос по химии:
Какая валентность у серебра?
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
- bookmark_border
- 20.10.2017 17:22
- Химия
- remove_red_eye 14711
- thumb_up 36
Ответы и объяснения 1
fitheferes
У серебра валентность 1. По таблице Менделеева смотри. Поскольку этот элемент с постоянной валентностью,то смотри по номеру группы. Серебро в первой группе,значит и валентность 1
- 21.10.2017 19:44
- thumb_up 20
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
Как БЫСТРО определить ВАЛЕНТНОСТЬ #shorts #youtubeshorts
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Источник: online-otvet.ru
Валентность серебра

Валентность (от лат. valēns – «имеющий силу») – способность атомов химических элементов образовывать определённое число химических связей.
Валентность – это мера (численная характеристика) способности химических элементов образовывать определённое число химических связей.
Значения валентности записывают римскими цифрами I, II, III, IV, V, VI, VII, VIII.
Валентность определяют по числу химических связей, которые один атом образует с другими.
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода – двум, азота – трём, углерода – четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента. Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода – двум, азота – трём, кремния – четырём, серы – шести.
С точки зрения электронной теории валентность определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии.
Известны элементы, которые проявляют постоянную валентность. У большинства химических элементов валентность переменная.
Валентность серебра равна I, II, III. Серебро проявляет переменную валентность.
| Валентность серебра в соединениях | |
| I | Ag2O, Ag2O2, Ag2SO4, Ag2S, AgBr, AgBrO3 |
| II | AgS, AgO, AgF2 |
| III | Ag3P, Ag2O2 |
Источник: xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai
Валентность серебра
Серебро расположено в пятом периоде I группе побочной (В) подгруппе Периодической таблицы. Металл. Обозначение – Ag. Порядковый номер – 47.
Серебро представляет собой металл белого цвета с гранецентрированной кубической решеткой. Серебро характеризуется исключительной пластичностью и превосходит другие металлы по теплопроводности и электрической проводимости. Плотность 10,5 г/см 3 . Температура плавления 961,2 o С, кипения 2170 o С.
Валентность серебра в соединениях
Серебро – сорок седьмой по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в пятом периоде в IВ группе. В ядре атома серебра содержится 47 протонов и 61 нейтрон (массовое число равно 108). В атоме серебра есть пять энергетических уровней, на которых находятся 47 электронов (рис.
1).
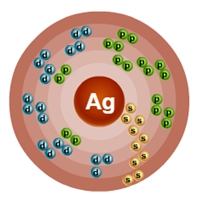
Рис. 1. Строение атома серебра.
Электронная формула атома серебра в основном состоянии имеет следующий вид:
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
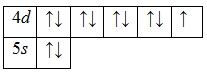
Наличие одного неспаренного электрона свидетельствует о том, что серебро проявляет валентность I в своих соединениях (Ag2O, AgNO3, AgCl, Ag2S и т.д.).
Известно, что для серебра также характерна валентность II (AgO, AgF2).
Примеры решения задач
| Задание | Вычислите массовую долю нитрата серебра в растворе, полученном при растворении соли массой 40 г в воде количеством 20 моль. |
| Решение | Найдем массу воды (молярная масса 18г/моль): |
m (H2O)= 20 × 18 = 360 г.
Рассчитаем массу раствора нитрата серебра:
msolution(AgNO3) = 40 + 360 = 400 г.
Вычислим массовую долю нитрата серебра в растворе:
ω (AgNO3)=40 / 400 × 100% = 10%.
| Задание | При растворении 3 г сплава меди и серебра в концентрированной азотной кислоте получили 7,34 г смеси нитратов. Определите массовые доли металлов в сплаве. |
| Решение | Запишем уравнения реакций взаимодействия металлов, представляющих собой сплав (медь и серебро), в концентрированной азотной кислоте: |
В результате реакции образуется смесь, состоящая из нитрата серебра и нитрата меди (II). Пусть количество вещества меди в сплаве составляет х моль, а количество вещества серебра – у моль. Тогда массы этих металлов будут равны (молярная масса меди 64 г/моль, серебра – 108 г/моль):
m (Cu) = n (Cu) × M (Cu);
m (Cu)= x × 64 = 64x.
m (Ag) = n (Ag) × M (Ag);
m (Ag)= x × 108 = 108y.
Согласно условию задачи, масса сплава равна 3 г, т.е.:
По уравнению (1) n(Cu) : n(Cu(NO3)2) = 1:1, значит n(Cu(NO3)2) = n(Cu) =х. Тогда масса нитрата меди (II) составляет (молярная масса равна 188 г/моль) 188х.
Согласно уравнению (2), n(Ag) : n(AgNO3) = 1:1, значит n(AgNO3) = n(Ag) =y. Тогда масса нитрата серебра составляет (молярная масса равна 170 г/моль) 170y.
По условию задачи масса смеси нитратов равна 7,34 г:
188х + 170у = 7,34.
Получили систему уравнений с двумя неизвестными:
![[ begin{cases} 4х + 108у = 3 \ 188х + 170у = 7,34 end{cases} ]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-bbdc4ee63a39a240d9293928a8772950_l3.png)
Выразим из первого уравнения х и подставим это значение во второе уравнение, т.е. решим систему методом подстановки.
Значит количество вещества серебра равно 0,01 моль. Тогда, масса серебра в сплаве равна:
m (Ag) = n (Ag) × M (Ag) = 0,01 × 108 = 1,08г.
Не вычисляя x можно найти массу меди в сплаве:
m (Cu) = malloy– m (Ag) = 3 – 1,08 = 1,92 г.
Определим массовые доли металлов в смеси:
ω (Cu)= 1,92 / 3 × 100% = 64%;
ω (Ag)= 1,08 / 2 × 100% = 36%.
Источник: ru.solverbook.com