К металлам относят простые вещества, обладающие в обычных условиях высокими значениями электрической проводимости и теплопроводности, металлическим блеском и пластичностью. В настоящее время определяющим физическим свойством, которое позволяет отнести данное вещество к металлам, является понижение электропроводности при повышении температуры (отрицательный температурный коэффициент электрической проводимости). С химической точки зрения металлы обладают низкими значениями электроотрицательности и сродства к электрону, вследствие чего они выступают в химических процессах только как доноры электронов (восстановители), а в соединениях имеют положительные значения степени окисления. Важнейшая химическая характеристика металлов – образование основных оксидов и соответствующих гидроксидов. Металлы IV–VIII групп периодической системы имеют, как правило, соединения с несколькими степенями окисления, при этом высшие оксиды проявляют кислотный характер.
Все металлы в зависимости от строения атома делятся на s-металлы (щелочные металлы, щелочноземельные металлы), p-металлы (алюминий, галлий, индий, таллий, олово, свинец, висмут и полоний), d-металлы (все элементы побочных подгрупп) и f-металлы (лантаноиды и актиноиды). По технической классификации металлы делят на черные (железо и его сплавы), цветные (медь, свинец, никель, кобальт, олово, ртуть и др.), легкие металлы с плотностью менее 5000 кг/м 3 (щелочные металлы, алюминий, магний, кальций и др.), драгоценные, или благородные металлы (серебро, золото, платиновые металлы).
Простые вещества — металлы | Химия 8 класс #14 | Инфоурок
Обычно к металлам относят и их сплавы. Сплавы – это однородные системы, состоящие из двух или более металлов (иногда компонентами сплава могут быть и неметаллы), обладающие характерными металлическими свойствами. В промышленности, медицине, быту и т.д. чаще всего используют не чистые металлы, а их сплавы. Многие металлы образуют полиморфные модификации, отличающиеся кристаллической структурой.
Около 20 химических элементов образуют простые вещества, являющиеся неметаллами, обладающие свойствами, противоположными свойствам металлов: отсутствие металлического блеска, ковкости (пластичности), электрической проводимости, с низкой теплопроводностью. В периодической таблице химических элементов (в ее длиннопериодном варианте) граница между металлами и неметаллами проходит по диагонали от бора до астата, при этом германий все же часто относят к неметаллам. Как уже указывалось, деление простых веществ на металлы и неметаллы по приведенным признакам достаточно условно, так как и некоторые неметаллы обладают металлическим блеском, например, иод; известны хрупкие металлы; некоторые химические элементы образуют как металлические, так и неметаллические аллотропные модификации.
С химической точки зрения неметаллы при взаимодействии с другими веществами могут выступать и в роли доноров, и в роли акцепторов электронов, то есть могут проявлять в соединениях как положительные, так и отрицательные значения степени окисления.
13. Простые вещества (металлы и неметаллы)
Исходя из вышеуказанного, к неметаллам относят простые вещества, образованные химическими элементами главных подгрупп VIII группы (гелий, неон, аргон, криптон, ксенон, радон); VII группы (водород, фтор, хлор, бром, иод, астат); VI группы (кислород, сера, селен, теллур); V группы (азот, фосфор, мышьяк); IV группы (углерод, кремний, германий); III группы (бор).
Простые вещества называют, как правило, по названиям химических элементов. Исключения составляют: алмаз, графит, озон и некоторые другие названия простых веществ. Двойственность названий химического элемента и простого вещества вызывает определенные затруднения в их различении.
Обычно, о чем речь – об элементе или о простом веществе, становится ясным из контекста высказываний. Например, в предложениях: «Вода содержит почти 90% кислорода». «Содержание кислорода в воде падает с повышением температуры», – в первом случае говорится о кислороде как элементе, во втором предложении – как о простом веществе. Для различения простых веществ и элементов можно уточнять их названия прилагательными «атомный» (атомарный) или «молекулярный», например, молекулярный хлор – Cl2, атомарный азот – N. Возможно также в названиях веществ указывать число атомов в молекуле, например, дииод – I2, трикислород – O3, октасера – S8.
Названия полиморфных модификаций металлов состоят из соответствующей греческой буквы (α, β, γ, δ, ε) и обычного названия вещества, например, альфа-железо – α-Fe, гамма-олово – γ-Sn и т.д.
Источник: studfile.net
Простые и сложные вещества
Из этой статьи вы узнаете, какие вещества называются простыми, а какие сложными, в чем их различия и особенности строения.
· Обновлено 23 июня 2023
Прежде чем переходить к понятиям простых и сложных веществ и к их строению, давайте вспомним, что такое химический элемент.
Химический элемент — это группа атомов с одинаковым зарядом ядра, который обусловливает его (элемента) химические свойства.
В зависимости от того, как соединяются друг с другом химические элементы, выделяют два типа веществ: простые и сложные.
Что такое простые вещества
Простые вещества — это вещества, образованные атомами только одного типа химического элемента. Например: H2, Na, P, Al.
Простые вещества делятся на два типа: металлы и неметаллы.
Металлы
Имеют общие между собой физические свойства. Обладают металлическим блеском, высокой тепло- и электропроводностью, твердые (за исключением ртути), пластичные и ковкие.
К простым веществам — металлам относятся: Na, Ca, Fe и т. д.
Почти все металлы имеют немолекулярное строение, т. е. состоят из атомов или ионов.
Неметаллы
Среди неметаллов выделить общие физические свойства практически невозможно. Они могут находиться в разных агрегатных состояниях, обладать различным цветом и т. д.
К простым веществам — неметаллам относятся: P, C, F2 и т. д.
Большинство неметаллов имеют молекулярное строение, т. е. состоят из молекул. При этом молекулы могут быть:
- одноатомные: He, Si, Ar и другие;
- двухатомные: F2, O2, H2, N2, Cl2, Br2, I2. Эти простые вещества всегда пишутся с индексом 2, их необходимо запомнить;
- трехатомные — например, молекула озона O3;
- и другие многоатомные.
Запоминаем
Некоторые неметаллы имеют немолекулярное (атомное) строение: красный фосфор, кремний, алмаз и графит.
Металлы и неметаллы сильно отличаются друг от друга физическими и химическими свойствами.
При этом запоминать, к какому типу относится то или иное вещество, не нужно, достаточно посмотреть в таблицу Менделеева:
- Проведите диагональ от 5-го до 85-го номера химических элементов.
- Все химические элементы, находящиеся ниже и левее проведенной диагонали, образуют простые вещества — металлы (кроме водорода).
- Выше диагонали химические элементы, находящиеся в главных подгруппах, образуют простые вещества — неметаллы, а в побочных — металлы.
Например, фосфор (порядковый номер — 15) расположен в таблице Менделеева выше диагонали и в главной подгруппе V группы. Значит, простое вещество фосфор — неметалл.
В большинстве случаев названия химического элемента и простого вещества совпадают. Поэтому необходимо научиться различать характеристики простого вещества и химического элемента.
Характеристика химического элемента
Характеристика простого вещества
- Расположение в периодической системе (атомный номер, номер группы или периода)
- Относительная атомная масса
- Строение атома (число электронов, протонов или нейтронов, количество заполненных энергетических уровней)
- Изотопный состав
- Возможные степени окисления
- Валентность
- Распространенность в природе
- Содержание в соединении (например, в растительных белках или аминокислотах)
- Значения электроотрицательности, сродства к электрону, энергии ионизации
Как правило, когда мы характеризуем простое вещество, то говорим о его физических или химических свойствах:
Аллотропия
- углерод (алмаз, графит, графен, углеродные нанотрубки, фуллерен и другие);
- фосфор (красный, белый и черный);
- кислород (кислород и озон);
- кремний (аморфный и кристаллический);
- Рассмотрим две аллотропные модификации углерода:


The image 1 is a derivative of «Crystal» by manfredxy on Envato Elements.
The image 2 is a derivative of «Rough Graphite rock» by vvoennyy on Envato Elements.
Алмаз — бесцветное прозрачное вещество. Является одним из самых твердых веществ. Не проводит электрический ток.
Графит представляет собой вещество серо-черного цвета, обладает металлическим блеском. Имеет высокую тепло- и электропроводность.
Графит представляет собой вещество серо-черного цвета, обладает металлическим блеском. Имеет высокую тепло- и электропроводность.
Получай лайфхаки, статьи, видео и чек-листы по обучению на почту
![]()
Полезные подарки для родителей
В колесе фортуны — гарантированные призы, которые помогут наладить учебный процесс и выстроить отношения с ребёнком!
Получить подарок!
Что такое сложные вещества
Сложные вещества — это вещества, образованные атомами нескольких химических элементов.
Например, молекула HNO3 состоит из одного атома водорода, одного атома азота и трех атомов кислорода.
К сложным веществам в химии относятся две большие группы веществ: неорганические и органические.
Неорганические вещества
Неорганические вещества делятся на 4 вида:
- Оксиды — вещества, молекулы которых состоят из двух химических элементов, один из которых — кислород в степени окисления −2. Например: Na2O, CaO, P2O5.
- Основания — вещества, молекулы которых состоят из катиона металла и гидроксильной группы (—OH). Например: KOH, Fe(OH)3, Ni(OH)2.
- Кислоты — вещества, молекулы которых состоят из катиона водорода (H+), способного замещаться атомом металла, и кислотного остатка. Например: HNO3, HCl, H3PO4.
- Соли — вещества, состоящие из катиона металла и кислотного остатка. Например: NaCl, CaCO3, K2SO4.
Кратко о классификации веществ можно узнать из схемы:
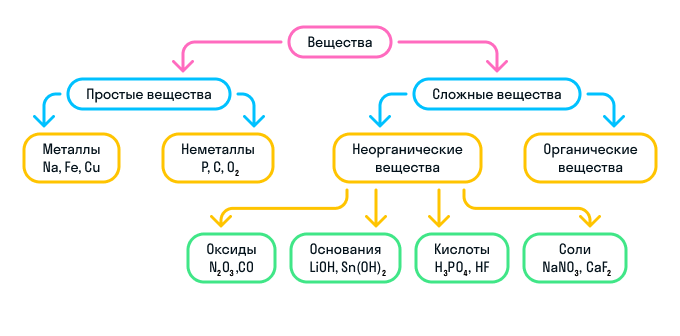
Номенклатура неорганических веществ
Названия простых веществ чаще всего совпадают с названием химического элемента, а для сложных веществ существует два вида номенклатуры: тривиальная и систематическая.
В тривиальной номенклатуре вещества названы в соответствии с их особенностями, например специфическим запахом или окраской.
В систематической номенклатуре название зависит от вида неорганического вещества.
Оксиды
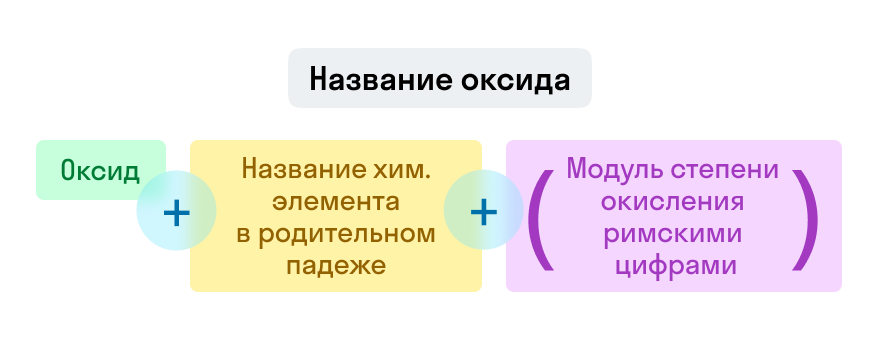
Напоминаем
Если степень окисления у элемента постоянная, то она в конце названия не указывается.
Примеры названий оксидов:
- Fe2O3 — оксид железа (III). Читается: феррум два о три;
- Na2O — оксид натрия. Читается: натрий два о.
Основания
Примеры названий гидроксидов:
- Fe(OH)3 — гидроксид железа (III). Читается: феррум о аш трижды;
- NaOH — гидроксид натрия. Читается: натрий о аш.
Соли
Примеры названий солей:
- KNO3 — нитрат калия. Читается: калий эн о три;
- AlCl3 — хлорид алюминия. Читается: алюминий хлор три.
Кислоты
Названия кислот, кислотных остатков и их формулы необходимо выучить, они приведены в таблице ниже.
Формула кислотного остатка
Название кислотного остатка
Источник: skysmart.ru
2. Металлы и неметаллы
Металлы имеют немолекулярное строение и сходные физические свойства. Все металлы (кроме ртути) при обычных условиях представляют собой твёрдые вещества. Их легко узнать по характерному металлическому блеску. Металлы хорошо проводят тепло и электрический ток.

Рис. (1). Ртуть

Рис. (2). Железо
При ударе металлы не разрушаются, а меняют свою форму, т. е. им характерна пластичность. Металлы можно ковать, прокатывать в листы, вытягивать в проволоку.
Неметаллы не имеют общих физических свойств и не похожи на металлы. У них отсутствует металлический блеск. У большинства неметаллов низкие электропроводность и теплопроводность.
Большинство неметаллов имеет молекулярное строение . Такие вещества при обычных условиях являются газами (водород, кислород, азот, озон, фтор, хлор, инертные газы), жидкостями (бром) или хрупкими легкоплавкими твёрдыми веществами (сера, иод, белый фосфор).

Рис. (3). Хлор

Рис. (4). Бром

Рис. (5). Сера
Некоторые неметаллы имеют немолекулярное строение , например, красный фосфор, кремний, алмаз и графит. Такие вещества твёрдые, тугоплавкие, нелетучие.

Рис. (6). Уголь
Определить, является простое вещество металлом или неметаллом, можно с помощью периодической таблицы. Химические элементы металлы, образующие простые вещества с металлическими свойствами, располагаются в периодической таблице слева ниже диагонали «водород — бор — кремний — мышьяк — теллур — астат — № (118)». Вверху справа располагаются химические элементы неметаллы, которые образуют простые вещества с неметаллическими свойствами.
Рис. (7). Периодическая таблица
Элементов металлов больше, чем элементов неметаллов. Значит, и простых веществ с металлическими свойствами существует больше, чем с неметаллическими.
Источник: www.yaklass.ru