2) Кристаллический кремний – серое кристаллическое вещество с металлическим блеском. По структуре напоминает алмаз.
tпл = 1410 °С, tкип = 2620 °С.
Весьма твердый, очень хрупкий. Плавится с уменьшением объема. Полупроводник при обычной температуре.
Химические свойства кремния
При обычных условиях кремний химически инертен из-за тончайшей пленки SiO2, образующегося на воздухе. Все реакции с ним протекают при повышенных температурах: 600–1200°С.
1) При обычных условиях реагирует только со фтором
Si + F2 Combin SiF4 горит в атмосфере фтора
2) Взаимодействует с кислородом
Si + О2 Combin SiО2 измельченный кремний воспламеняется
3) С водородом НЕ реагирует
Соединения кремния с водородом – силаны – можно получить косвенным путем
Силаны обычно получают, разлагая кислотами силициды активных металлов:
4) Взаимодействует с галогенами
Si + Сl2 Combin SiCl4 реагирует в токе аргона
5) Взаимодействует с серой
Кремний и его соединения. Видеоурок 35. Химия 9 класс
Si + S Combin SiS2
6) Взаимодействует с азотом
Si + N2 Combin Si3N4 нитрид кремния
7) Взаимодействует с углеродом
Si + С Combin SiС карборунд (по твердости близок к алмазу, широко применяется как абразивный материал)
8) Взаимодействует с металлами с образованием силицидов
Mg + Si Combin Mg2Si силицид магния
9) Восстанавливает металлы из их оксидов
MgO + Si Combin SiO2 + Mg
10) Растворяется в горячих концентрированных щелочах
11) Аморфный кремний растворяется в плавиковой кислоте (другие кислоты на кремний не действуют)
ПОЛУЧЕНИЕ КРЕМНИЯ
1) Восстановлением SiO2
SiО2 + C Combin Si + CО кристаллический кремний
SiO2 + Mg Combin MgO + Si аморфный кремний
2) Особо чистый кремний получают восстановлением хлорида кремния
SiCl4 + Zn Combin Si + ZnCl2
3) Термическим разложением силана
ДИОКСИД КРЕМНИЯ SiО2
(кремнезём, кварц)
ФИЗИЧЕСКИЕ СВОЙСТВА SiO2
SiO2 – бесцветное твердое кристаллическое вещество, tпл = 1713 °С. Нерастворим в воде, кислотах. Один из лучших диэлектриков (не проводит электрический ток).
В природе образует минералы – горный хрусталь, аметист, агат, яшма, песок, кремень, опал и др.
ХИМИЧЕСКИЕ СВОЙСТВА SiO2
SiO2 – кислотный оксид, нерастворимый в воде
1) Растворяется в плавиковой кислоте. Другие кислоты на него не действуют
SiO2 + HF Combin SiF4 + H2O эта реакция широко применяется для травления стекла
2)Разрушается под действием фтора
3) Сплавление с основными оксидами и щелочами
4) Сплавление с карбонатами
При сплавлении соды, известняка и песка при 1400 °С получается смесь оксидов, из которой делают оконное стекло
Если заменить Na2O → K2O, получается тугоплавкое стекло; CaO → PbO, получается хрусталь
Na2O → K2O, CaO → PbO, получаются стразы
Введение в сплав небольшого количества оксидов придает стеклу различную окраску:
Cr2O3 – зеленая, CoO – синяя, MnO2 – лиловая, Au – красная, UO3 – желто-зеленая с зеленой флуоресценцией и др.
Химические свойства кремния и его соединений.
Кварцевое стекло – чистый SiO2 – выдерживает нагревание до белого каления, пропускает УФ лучи.
Цемент, получаемый обжигом глины Al2O3·2SiO2·2H2O и известняка CaCO3 при 1400–1500 °С, состоит из оксидов Al2O3, SiO2, CaO, Fe2O3.
Керамику получают обжигом каолина Al2O3·2SiO2·2H2O, кварца SiO2, полевого шпата и пластичной глины при 1000‑1500 °С (кирпич, черепица, фаянс, фарфор).
КРЕМНИЕВАЯ КИСЛОТА H2SiО3
Существует только в растворе. Является очень слабой кислотой. Обладает полимерной структурой и в воде образует коллоидный раствор.
Разлагается при нагревании:
При ее высушивании образуется силикагель – хороший осушитель газов и жидкостей.
ПОЛУЧЕНИЕ H2SiО3
Действием кислот на силикаты
Na2SiО3 + HCl→ NaCl + H2SiO3↓ выпадает в осадок в виде геля
Соли H2SiО3 – СИЛИКАТЫ
Это белые кристаллические вещества. Растворимы только Na2SiО3 и K2SiО3 – «жидкое стекло». Остальные силикаты не растворяются в воде.
Их можно представить как смесь оксидов металла и кремния:
Все силикаты подвергаются гидролизу по аниону, создавая в своих растворах щелочную среду:
ПРИМЕНЕНИЕ КРЕМНИЯ и его СОЕДИНЕНИЙ
1. Si – как полупроводник (в солнечных батареях, выпрямителях тока, фотоэлементах);
– получение кремнистых сталей и ферросилиция;
2. SiO2 – кварц – в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др.;
– кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках;
– главный компонент почти всех земных горных пород, в частности, кизельгура;
– аморфный непористый SiO2 применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слеживанию и комкованию, парафармацевтике (зубные пасты), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента;
– искусственно полученные пленки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов;
– для производства волоконно-оптических кабелей;
– кремнезёмная нить также используется в нагревательных элементах электронных сигарет, так как хорошо впитывает жидкость и не разрушается под нагревом спирали;
– в ювелирном деле;
3. H2SiO3 – высушенный гель кремниевой кислоты – силикагель. Применяется как влагопоглотитель.
4. Na2SiO3 – раствор в воде – силикатный клей.
Источник: studfile.net
Вопрос № 2 Каковы физические и химические свойства кремния? Приведите уравнения соответствующих химических реакций. Поясните, какие свойства кремния используют в технике.
Ответ: 1. Физические свойства: кристаллический кремний обладает металлическим блеском, тугоплавкий, очень твердый, полупроводник. 2. Химические свойства: кремний малоактивен: а) при повышенных температурах (400-600 
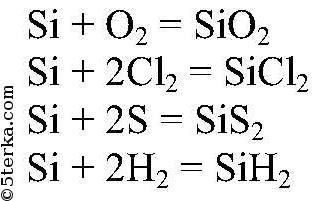 б) из сложных веществ кремний реагирует со щелочами
б) из сложных веществ кремний реагирует со щелочами 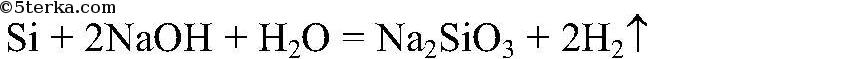 в) реагирует с металлами с образованием силицидов
в) реагирует с металлами с образованием силицидов 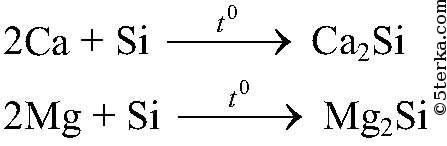 3. В технике используют полупроводниковые свойства кремния, его жаропрочность и кислотоупорность (производство кремнистых сталей).
3. В технике используют полупроводниковые свойства кремния, его жаропрочность и кислотоупорность (производство кремнистых сталей).
Источник:

Решебник по химии за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
задача №2
к главе «Глава V §§ 35 — 39 стр. 101».
Источник: 5terka.com
Каковы физические и химические свойства кремния ? Приведите уравнения соответствующих химических реакций. Поясните, какие свойства кремния используют в технике.
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
- Обратная связь
- Правила сайта
Источник: www.soloby.ru