Серебро принадлежит к первой группе периодической системы элементов Д.И. Менделеева и располагается в пятом периоде между палладием и кадмием. Порядковый номер серебра 47. По своим химическим свойствам и условиям нахождения в природе серебро является благородным металлом. Распределение электронов по уровням в атомах серебра следующее:
1s2s2р3s3p3d4s4p 4d5s
2 2 6 2 6 10 2 6 10 1
Атомная масса серебра по углеродной шкале равна 107,868. Элемент представляет естественную смесь двух устойчивых изотопов с массовыми числами 107 и 109. Искусст-венно получены многие радиоактивные изотопы серебра.
5. Кристаллическая структура серебра
Серебро имеет гранецентрированную кубическую кристаллическую решетку с пара-метром а = 4,0772 Å (при 20 °С). Энергия кристаллической решетки 290 мкДж/кмоль. Радиус междоузлий октаэдрических 0,106 нм, тетраэдрических 0,032 нм. По внешнему виду серебро – красивый металл белого цвета, очень пластичный и легко полируется. Из всех металлов серебро имеет наивысшую отражательную способность, равную в оранжево-красной части спектра 95%, наивысшую электропроводность и теплопро-водность.
ПОЛУЧЕНИЕ ЧИСТОГО СЕРЕБРА ПЛАВКОЙ! САМЫЙ ДЕШЕВЫЙ И ПРОСТОЙ СПОСОБ…
Ионный радиус серебра (Ag+) составляет, по Гольдшмидту и Полингу, 1,13 и 1,26 Å соответственно.
6. Важнейшие физические свойства серебра
Плотность. Плотность ρ чистого серебра, деформированного и подвергнутого полному отжигу, равна 10,49 Мг/м 3 . В результате холодной обработки давлением плотность уменьшается и составляет для холоднотянутой проволоки 10,434 Мг/м 3 . При нагревании до 973, 1073 и 1173 К плотность соответственно составляет 9,98; 9,8 и 9,72 Мг/м 3 .
Плотность жидкого серебра при различных температурах:
Т, К 1273 1323 1373 1423 1473 1523
ρ, Мг/м 3 9,25 9,2 9,17 9,15 9,1 9,0
Плотность серебра при температуре плавления составляет 9,346 Мг/м 3 , при температу-ре кипения 8,244 Мг/м 3 .
Электрические и магнитные характеристики.Удельная электрическая проводи-мость σ серебра в зависимости от температуры:
Т, К . 53 273 473 773
σ, МСм/м . 200 62,0 35,1 21,1
Удельное электрическое сопротивление ρ серебра в зависимости от температуры:
Т.К. …53 273 473 773
ρ, мкОм∙м…..0,005 0,0162 0,0285 0,0475
Температурный коэффициент электрического сопротивления серебра при 273 К равен 4,10∙10 –3 К –1 . При переходе из твердого состояния в жидкое удельное электросопротивление увеличивается почти в два раза и продолжает возрастать при дальнейшем повышении температуры:
Г, К ……. 1233,5 (тв) 1233,5 (ж) 1273 1373 1473 1573
ρ, мкОм∙м……. 0,084 0,166 0,170 0,182 0,194 0,205
Твердость,кг/мм 2 :
Потенциалы ионизации,эв:
Серебро – диамагнитный металл. Его удельная магнитная восприимчивость отрица-тельна и составляет при комнатной температуре % = – 0,181∙10 –9 . С изменением темпе-ратуры магнитная восприимчивость практически не изменяется. В жидком состоянии магнитная восприимчивость серебра ничтожно мала; при холодной обработке давлением снижается. Работа выхода электронов φ = 4,3 эВ. Коэффициент вторичной электронной эмиссии σ =1,5 при ускоряющем напряжении первичных электронов 0,800 кэВ.
Серебро — САМЫЙ БЛЕСТЯЩИЙ МЕТАЛЛ НА ЗЕМЛЕ!
Тепловые характеристики.Температура плавленияtПЛ= 961,9 °С, температура кипенияtКИП= 2170 °С; характеристическая температура θD= 225,3 К, удельная теплота плавления ΔНПЛ= 104,6 кДж/кг, удельная теплота сублимации, отнесенная к 298 К, ΔНСУБ= 2640 кДж/кг. При плавлении происходит увеличение объема на ΔV = 5,33∙10 –6 м 3 /кг, илиV/V0= 0,052. С увеличением давления температура плавления серебра возрастает и при 6 ГПа достигает 1588 К;dT/dP= 60 К/ГПа.
Теплопроводность λ серебра высокой чистоты в зависимости от температуры:
Т, К………….…3 15 42 273 300 600 900
λ, Вт/(мК)……501,5 3330,5 1052,0 453,0 432,5 410,7 388,8
Оптические характеристики.Отражательная способность серебра в области види-мых длин волн 95 %, в области инфракрасных 98 %, а в ультрафиолетовой области 10 % при длине волны 0,31 мкм. При выдержке на воздухе отражательная способность серебра падает. Наибольшей отражательной способностью обладает серебро, нанесенное в вакууме на стекло.
Источник: studfile.net
Какую кристаллическую решетку имеет серебро
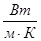
410,5
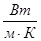
111[10]
Из рисунка 5, видно, что увеличение размера частиц серебра, приводит к существенному изменению температуры плавления. С другой стороны, существуют и другие факторы, приводящие к изменениям температуры кипения. Например, как было показано, одним из факторов может случить количество частиц углерода. Также можно отметить изменение механических свойств материала, проиллюстрированных в таблице 1.
Ключевую роль в изменении поведения наносеребра при переходе от макроструктуры к нано играют классические размерные эффекты. Данное предположение было основано на сравнении размеров наноструктуры серебра с длиной волны де-Бройля. Для металлов длина волны де Бройля находится в интервале 0.1 нм − 1 нм. Основываясь на данном факте може прийти к выводу о несущественном влиянии квантовых размерных эффектов. Однако, поскольку консистенция серебра — порошок, то внутри могут быть структуры с квантовую точку или порядка 1-10 нм, что говорит о том, что частично могут наблюдаться квантовые размерные эффекты.
Так как размер нано-порошка Ag сравним с длиной свободного пробега в кристалле и составляет 50-100 нм, то к классическим размерным эффектам можно отнести понижение температуры плавления, повышение теплоёмкости, увеличение коэффициента термического расширения и уменьшение теплопроводности, а также возрастание удельного сопротивления, увеличение механических характеристик, например, твёрдость, что согласуется с вышеприведенной таблицей 1.
С начала развития использования материалов с наноструктурой, наносеребро обрело одно из наиболее широких применений в различных сферах деятельности человека.
Методы получения наносеребра различны и могут осуществляться как на основе физических воздействий, так и при помощи химических реакций. В основу физического получения используются установки по механическому измельчению серебра вплоть до нано- размеров частиц. К химическим методам наиболее широкий способ получения наносеребра основан на химическом восстановлении. В частности можно выделить методы фоторедукции, как метода физического восстановления либо фотовосстановление, придерживающееся восстановления ионов серебра до размера частиц серебра в нано диапазоне с использованием катализаторов и образованием радикалов, под воздействием ультрафиолетового излучения.
Материалы на основе серебра имеют широкое применение в промышленности и медицине. Например, специально приготовленные наночастицы серебра используются в качестве сенсоров для определения болезнетворных бактерий. Серебро наноситься тонкой плёнкой на хирургические инструменты для обеспечения антибактериального эффекта. С другой стороны, можно выделить следующее применение материалов на основе серебра:
- Для контактов электротехнических изделий, например, контакты реле, ламели, а также многослойных керамических конденсаторов.
- Изготовление батареек.
- Ювелирная сфера применения.
- Из-за высочайшей электропроводности и стойкости к окислению применяется:
- в электротехнике и электронике как покрытие ответственных контактов
- в СВЧ технике как покрытие внутренней поверхности волноводов
- В качестве отражающей поверхности.
- Используется в качестве катализаторов в химических реакциях.
Можно также выделить тенденцию развития использования наносеребра. Важно отметить широту использования данного материала в медицине, где он нашел применение в качестве покрытия инструментов, так и подложка в из наносеребра может служить хорошей основой для имплантации неорганических приборов в человеческий организм.
Источник: eduherald.ru
Серебро
Этот красивый металл известен людям с древности. В Передней Азии были найдены серебряные изделия, изготовленные более 6000 лет назад. Первые в мире монеты делали из сплава золота и серебра. В течение нескольких тысячелетий серебро наряду с золотом и медью было одним из основных монетных металлов.

Серебряные монеты наряду с золотыми использовались в разных странах мира
Чистое серебро — сравнительно мягкий и пластичный металл: из 1 г серебра можно вытянуть тончайшую проволочку длиной почти 2 км! Кроме того, это довольно тяжелый металл: по плотности (10,5 г/см 3 ) он лишь немного уступает свинцу. По электропроводности же и теплопроводности серебру нет равных (поэтому серебряная ложка в стакане горячего чая быстро нагревается). Плавится оно при относительно низкой температуре (962°С), что значительно облегчает его обработку. Серебро легко сплавляется со многими металлами; небольшие добавки меди делают его более твердым, годным для изготовления различных изделий.
Латинское название серебра Argentum связано с его цветом. Оно происходит от греческого слова argos — «белый, блестящий».

Серебро люди добывают уже несколько тысячелетий

Серебряный рудник в Боливии
Серебро — относительно редкий элемент: в земной коре его почти в 1000 раз меньше, чем меди, — всего лишь около стотысячной доли процента. Известно же оно стало так давно потому, что встречается в природе в виде самородков, иногда очень больших. Особенно были богаты серебром горы, расположенные в Центральной Европе: Рудные, Гарц, горы Богемии и Саксонии. Из серебра, добытого близ города Иоахимсталя (ныне Яхимов в Чехии), отчеканены миллионы монет, получивших название «талеры». Немецкие серебряные рудники были настолько богаты, что из получаемого оттуда металла делали огромные вазы, столовые сервизы на сотни персон, на каждый из которых расходовали тонны серебра.

Украшения из серебра всегда были популярны
После открытия и завоевания Америки множество самородков серебра было найдено на территории современных Перу, Чили, Мексики, Боливии. Так, в Чили был обнаружен самородок в виде пластины массой 1420 кг. Многие химические элементы имеют «географические» названия, Аргентина же — единственная страна, названная в честь уже известного элемента.
Изготовление зеркал — одно из самых древних применений серебра в промышленности. Также из него делают электроды для мощных серебряно-цинковых аккумуляторов. Высокую теплопроводность и химическую инертность этого металла используют в электротехнике: из серебра и его сплавов делают электрические контакты, серебром покрывают провода в особо важных приборах. Из серебрянопалладиевого сплава (75% Ад) делают зубные протезы. Серебро применяется также для производства украшений и посуды.

Одно из применений серебра — изготовление зеркал
Физические свойства
Серебро — химический элемент 11-й группы пятого периода периодической системы химических элементов с атомным номером 47. Обозначается символом Ад (лат. Argentum).
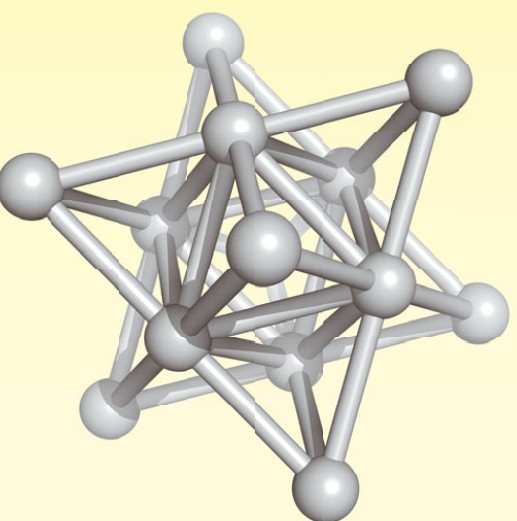
Кристаллическая структура серебра
Чистое серебро — ковкий, пластичный благородный металл серебристо-белого цвета. Кристаллическая решетка — гранецентрированная кубическая. Температура плавления — 962°С, плотность —10,5 г/см 3 .
Почему платина сначала была дешевле серебра, а теперь гораздо дороже?

Платина прочнее золота и серебра. Она используется в медицине, технике и ювелирном деле
Слово «платина» в переводе с испанского буквально означает «серебришко». Объясняется такое пренебрежительное название, данное этому металлу конкистадорами, исключительной тугоплавкостью платины, которая из-за этого долгое время не находила применения и ценилась вдвое ниже, чем серебро. Сейчас на мировых биржах платина дороже серебра примерно в 100 раз. Этот чрезвычайно плотный металл используется и как добавка к легированным сталям, и как катализатор в химической промышленности, и даже при лечении онкологических заболеваний.
Как в древнем Египте использовали серебро в медицинских целях?
Древние египтяне использовали серебро как антисептик. Во время многочисленных войн солдаты накладывали на раны серебро, которое помогало остановить кровотечение и позволяло избежать заражения крови.
Источник: sitekid.ru