Гидроксиды – это неорганические соединения, образованные тем или иным элементом, кислородом и водородом. В гидроксидах обязательно имеется водород, связанный с кислородом (связь О–Н). В некоторых гидроксидах водород может непосредственно соединяться с атомами элемента. Например, в H3РO3 два атома водорода связаны с атомами кислорода, а один – с атомом фосфора.
В ряде случаев гидроксиды являются продуктами гидратации (соединения с водой) соответствующих оксидов, хотя многие оксиды непосредственно с водой не взаимодействуют. В результате дегидратации гидроксидов образуются соответствующие оксиды.
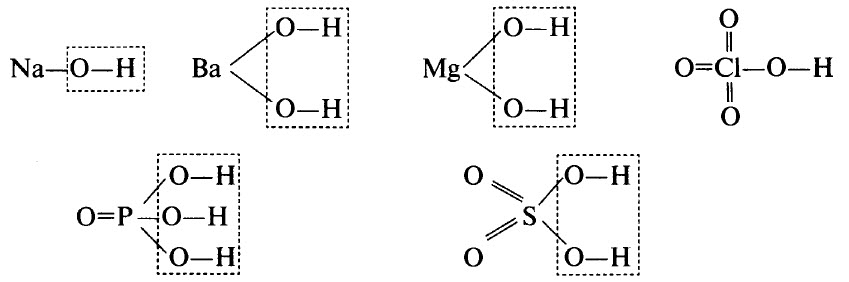
Гидроксиды могут быть основными (основания), кислотными (кислородсодержащие кислоты) и амфотерными. Примерами основных гидроксидов являются NaOH, Ва(ОН)2, Mg(OH)2. Примерами кислотных гидроксидов являются НСlO4 (хлорная кислота, высший гидроксид хлора), H3РO4 (ортофосфорная кислота, высший гидроксид фосфора), H2SO4 (серная кислота, высший гидроксид серы).
Графические формулы перечисленных гидроксидов приведены ниже. Во всех гидроксидах имеется связь О–Н:
оксиды и гидроксиды.avi
ПОНЯТИЕ ОБ АМФОТЕРНЫХ ОКСИДАХ И ГИДРОКСИДАХ
Амфотерность (от греч. amphoteros – и тот, и другой) – способность химических соединений проявлять и кислотные, и основные свойства в зависимости от природы реагента, с которым амфотерное вещество вступает в кислотно-основное взаимодействие.
Амфотерные оксиды и гидроксиды – оксиды и гидроксиды, проявляющие как основные, так и кислотные свойства. Они реагируют как с кислотами, так и с основаниями. Амфотерным оксидам соответствуют амфотерные гидроксиды, например: ВeО – Вe(ОН)2, Сr2O3 – Сr(ОН)3.
Амфотерные гидроксиды практически нерастворимы в воде. Их основные и кислотные свойства выражены слабо, они являются слабыми кислотами и слабыми основаниями.
Амфотерными оксидами и гидроксидами являются, как правило, оксиды и гидроксиды металлов, в которых степень окисления металла +3, +4, иногда +2.
Среди оксидов элементов главных подгрупп амфотерными являются: BeO, Al2O3, SnO, SnO2, PbO, Sb2O3.
Амфотерными гидроксидами являются следующие гидроксиды элементов главных подгрупп: Ве(ОН)2, Al(ОН)3, Рb(ОН)2 и некоторые другие.
Оксиды и гидроксиды элементов побочных подгрупп, соответствующие высоким степеням окисления, как правило, являются кислотными, например: СrO3 (ему соответствует H2СrO4), Мn2O7 (ему соответствует НМnO4).
Для низших оксидов и гидроксидов характерно преобладание основных свойств, например: СrO и Сr(ОН)2, МnО и Мn(ОН)2.
Оксиды и гидроксиды, в которых степени окисления элементов +3 и +4, являются, как правило, амфотерными: Сг2O3 и Cr(OH)3, Fe2O3 и Fe(OH)3. Однако последние элементы в декадах d–элементов (например, Zn) образуют амфотерные оксиды и гидроксиды даже в низких степенях окисления, например ZnO и Zn(OH)2.
ХИМИЧЕСКИЕ СВОЙСТВА АМФОТЕРНЫХ ОКСИДОВ И ГИДРОКСИДОВ
Рассмотрим амфотерные свойства оксида и гидроксида цинка – ZnO и Zn(OH)2. Оба вещества реагируют с кислотами:
Химия ОГЭ Выпуск 6 Кислотно основные свойства оксидов и гидроксидов Амфотерность
ZnO + 2HNO3 = Zn(NO3)2 + H2O
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O

Оксид и гидроксид цинка реагируют также и со щелочами:
В результате реакций со щелочами в растворах образуются комплексные ионы – тетрагидроксоцинкаты (например, Na2[Zn(OH)4]), а при сплавлении – цинкаты (например, Na2ZnO2). Чтобы составить формулы цинкатов, запишите формулу гидроксида цинка Zn(OH)2 как формулу кислоты – H2ZnO2. Кислотным остатком такой кислоты является ион ZnO2 2– .
При диссоциации этих солей в растворах образуются ионы, в которых цинк входит в состав анионов, поэтому говорят, что в этих соединениях «цинк в анионной форме».
Докажем амфотерность оксида и гидроксида алюминия Al(ОН)3. Он растворяется в кислотах с образованием солей, где алюминий находится в катионной форме:
Al(ОН)3 + 3Н + = Al 3+ + 3H2O
Но гидроксид алюминия взаимодействует и со щелочами. При сплавлении со щелочами образуются алюминаты (метаалюминаты):
Al(ОН)3 + NaOH = NaAlO2 + 2H2O
Чтобы составить формулы алюминатов, запишите формулу гидроксида алюминия Al(ОН)3 как H3AlO3. Теперь представьте, что от 1 моль этого соединения отщепляется 1 моль воды. Образуется соединение НАlO2, в котором кислотным остатком будет ион AlO2 – .
В образовавшейся соли алюминий образует анион AlO2 – (алюминий в анионной форме). В растворах в результате реакции со щёлочью образуется комплексный тетрагидроксоалюминат-ион [Al(ОН)4] – :
Al(ОН)3 + NaOH = Na[Al(OH)4] (тетрагидроксоалюминат натрия)
Некоторые амфотерные оксиды и гидроксиды не проявляют амфотерность в обычных условиях и в растворах ведут себя как основные. Амфотерность таких соединений проявляется в более жёстких условиях. Например, гидроксид железа (III) Fe(OH)3 легко реагирует с кислотами:
Fe(OH)3 + 3НCl = FeCl3 + 3H2O
Fe(OH)3 + NaOH = NaFeO2 + 2H2O
Признаком этой реакции будет растворение бурого осадка. А вот при добавлении раствора щёлочи гидроксид железа (III) не растворяется. Тогда, может быть, считать его основанием, не растворимым в воде? Дело в том, что в данном случае соль образуется при плавлении со щёлочью.
Естественно, что в ходе плавления происходит разложение гидроксида на оксид и воду, и в действительности реакция идёт между оксидом и щёлочью:
Fe2O3 + 2NaOH = 2NaFeO2 + H2O
Таким образом, гидроксид железа (III) можно отнести к амфотерным гидроксидам, хотя основные свойства у него преобладают.
Конспект урока по химии для 8 класса «Амфотерные оксиды и гидроксиды». Выберите дальнейшее действие:
- Вернуться к Списку конспектов по химии
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии
Источник: uchitel.pro
Кислотно – основные свойства гидроксидов.
Цель практической работы: изучить кислотно – основные свойства основных, кислотных и амфотерных гидроксидов, способы их получения и химическое взаимодействие; составление уравнений химических реакций, демонстрирующих эти свойства.
Теоретическая часть
Гидроксиды — тип сложных веществ, в состав которых входят атомы некоторого элемента Е (кроме фтора и кислорода) и гидроксогруппы ОН; общая формула гидроксидов Е(ОН)n, где n = 1÷6. Форма гидроксидов Е(ОН)n называется орто-формой; при n > 2 гидроксид может находиться также в мета-форме, включающей кроме атомов Е и групп ОН еще атомы кислорода О, например Е(ОН)3 и ЕО(ОН), Е(ОН)4 и Е(ОН)6 и ЕО2(ОН)2. Гидроксиды делят на две противоположные по химическим свойствам группы: кислотные и основные гидроксиды.
Кислотные гидроксиды содержат атомы водорода, которые могут замещаться на атомы металла при соблюдении правила стехиометрической валентности. Большинство кислотных гидроксидов находится в мета-форме, причем атомы водорода в формулах кислотных гидроксидов ставят на первое место, например H2SO4, HNO3 и H2CO3, а не SO2(OH)2, NO2(OH) и CO(OH)2. Общая формула кислотных гидроксидов НхЕОу, где электроотрицательную составляющую ЕОух называют кислотным остатком. Если не все атомы водорода замещены на металл, то они остаются в составе кислотного остатка. Названия распространенных кислотных гидроксидов состоят из двух слов: собственного названия с окончанием “ая” и группового слова “кислота”.
Получение кислотных гидроксидов
1. Взаимодействие кислотного оксида с водой (для кислородсодержащих кислот): SO3 + H2O = H2SO4 P2O5 + 3H2O = 2H3PO4
2. Взаимодействие водорода с неметаллом и последующим растворением полученного продукта в воде (для бескислородных кислот):
H2 + Cl2 = 2HCl H2 + S = H2S
3. Реакциями обмена соли с кислотой
Ba(NO3)2 + H2SO4 = BaSO4↓+ 2HNO3
в том числе, вытеснение слабых, летучих или малорастворимых кислот из солей более сильными кислотами:
Na2SiO3 + 2HCl = H2SiO3↓+ 2NaCl
2NaCl(тв.) + H2SO4(конц.) = Na2SO4 + 2HCl↑
Химические свойства кислотных гидроксидов
1. Действие на индикаторы: лакмус – красный; метилоранж — розовый
2. Взаимодействие с основаниями (реакция нейтрализации):
H2SO4 + 2KOH = K2SO4 + 2H2O
2HNO3 + Ca(OH)2 = Ca(NO3)2 + 2H2O
3. Взаимодействие с основными оксидами: CuO + 2HNO3 = Cu(NO3)2 + H2O
4. Взаимодействие с металлами(металлы, стоящие в ряду напряжений до водорода, кислоты-неокислители):
Zn + 2HCl = ZnCl2 + H2 2Al + 6HCl = 2AlCl3 + 3H2
Основные гидроксиды
Основаные гидроксиды состоят из иона металла и гидроксогрупп (OH-). Например, NaOH, Mg(OH)2, La (OH)3, Ca (OH)2.
ОН- — это гидроксид — ион, заряд его равен — 1. Число гидроксид — ионов в основании определяется степенью окисления металла.
Название основания составляется из слов “гидроксид” + название металла в родительном падеже. Например, КОН — гидроксид калия, Ва(ОH)2 — гидроксид бария, La(OH)3 — гидроксид лантана.
Если металл образует несколько гидроксидов, то указывают степень его окисления римской цифрой в скобках. Например, Fe(ОН)2 — гидроксид железa (II), Bi(OH)3 — гидроксид висмута (III). Haзвание основания составляют и так: к слову гидроксид добавляют приставки, которые показывают количество гидроксогрупп в основании. Например, Са(ОН)2 — дигидроксид кальция, Вi(ОН)3 — тригидроксид висмута.
Число гидроксогрупп в молекуле основания определяет его кислотность. Например, NaOH, КОН, NH4OH — однокислотные основания, Ca(OH)2, Sr(OH)2, Ва(OH)2 — двухкислотные основания, La(OH)3, Bi(OH)3 — трехкислотные основания, Th(OH)4 — четырехкислотное основание. Пятикислотные и шестикислотные основания неизвестны.
Остатки оснований. Положительно заряженные группы атомов (положительные ионы), которые остаются после отрыва от молекулы основания одной или нескольких гидроксогрупп, называются остатками основания или радикалами основания. Величина положительного заряда остатка основания определяется числом отрывавшихся гидроксогрупп.
Основные гидроксиды содержат гидроксид-ионы, которые могут замещаться на кислотные остатки при соблюдении правила стехиометрической валентности. Все основные гидроксиды находятся в орто-форме; их общая формула М(ОН)n, где n = 1,2 (реже 3,4) и Мn+ катион металла.
Получение основных гидроксидов
2. Взаимодействие оксидов активных металлов с водой: BaO + H2O = Ba(OH)2
3. Электролиз водных растворов солей: 2NaCl + 2H2O = 2NaOH + H2 + Cl2
Химические свойства основных гидроксидов
1. Действие на индикаторы растворимых основных гидроксидов: лакмус – синий;
метилоранж – жёлтый; фенолфталеин – малиновый.
2. Взаимодействие с кислотными оксидами: 2KOH + CO2 = K2CO3 + H2O
KOH + CO2 = KHCO3
3. Взаимодействие с кислотами (реакция нейтрализации) с образованием солей (реакция солеобразования), например: Ca(OH)2 + H2SO4 = CaSO4 + 2H2O
Ca(OH)2 + 2H2SO4 = Ca(HSO4)2 + 2H2O
2Ca(OH)2 + H2SO4 = Ca2SO4(OH)2 + 2H2O
NaOH + HNO3 = NaNO3 + H2O
Cu(OH)2 + 2HCl = CuCl2 + 2H2O
4. Обменная реакция с солями: Ba(OH)2 + K2SO4 = 2KOH + BaSO4 ↓
5. Термический распад: Cu(OH)2 –t° = CuO + H2O
Амфотерные гидроксиды
Амфотерность гидроксидов и оксидов химическое свойство, заключающееся в образовании ими двух рядов солей, например, для гидроксида и оксида алюминия:
(а) 2Al(OH)3 + 3SO3 = Al2(SO4)3 + 3H2O
(б) 2Al(OH)3 + Na2O = 2NaAlO2 + 3H2O
Так, гидроксид в реакциях (а) проявляет свойства основных гидроксидов т.е. реагирует с кислотными гидроксидам и оксидом, образуя соответствующую соль сульфат алюминия Al2(SO4)3, тогда как в реакции (б) он же проявляет свойства кислотных гидроксидов и оксидов, т.е. реагирует с основными гидроксидом и оксидом, образуя соль диоксоалюминат (III) натрия NaAlO2. В первом случае элемент алюминий проявляет свойство металла и входит в состав электроположительной составляющей (Al3+), во втором свойство неметалла и входит в состав электроотрицательной составляющей формулы соли (AlO2). Если указанные реакции протекают в водном растворе, то состав образующихся солей меняется, но присутствие алюминия в катионе и анионе остаётся:
2Al(OH)3 + 3H2SO4 = [Al(H2O)6]2(SO4)3
Al(OH)3 + NaOH = Na[Al(OH)4]
Практическая часть
Основываясь на знаниях способов получения и химических свойств гидроксидов предположите какие продукты реакции образуются, как ведут себя индикаторы в различных растворах гидроксидов, напишите уравнения реакций, ответьте на вопросы контрольного теста и сдайте на проверку преподавателю
Опыт №1 «Взаимодействие кислот и растворимых в воде оснований с индикаторами»
Дано: HCl, H2SO4, HNO3, HBr, H2S; NaOH, KOH, LiOH, Ca (OH)2, Ba (OH)2;
метиловый оранжевый, фенолфталеин, лакмус.
Задание: предположите изменение окраски индикаторов в растворах
гидроксида кальция и бромоводородной кислоты, гидроксида лития и сероводородной кислоты. Сделайте соответствующие выводы, запишите уравнения диссоциации данных веществ
Опыт №2 «Взаимодействие растворов кислот (HCl, H2 SO4 , H3 PO4) и щелочей с металлами »
Дано: NaOH, KOH, LiOH, Ba (OH)2; HCl, H2SO4, Н3 РО4; Cu, Zn, Al
Задание: охарактеризуйте отношение соляной кислоты и гидроксида калия к цинку,серной кислоты и гидроксида натрия к меди.
Сделайте соответствующие выводы, запишите соответствующие уравнения реакций.
Опыт №3 «Взаимодействие растворов кислот и оснований»
Дано: Cu (OH)2, NaOH, HCl, H2SO4, Н3 РО4
Задание: охарактеризуйте отношение гидроксида меди к соляной кислоте и гидроксида натрия (в присутствии индикатора — фенолфталеина) к серной кислоте.
Сделайте соответствующие выводы, запишите соответствующие уравнения реакций.
Опыт №4 «Взаимодействие кислот и щелочей с солями»
Дано: NaOH, KOH, Сa (OH)2; HCl, H2SO4, Н3 РО4, HNO3; ВаCl2, Cu SO4, Ag NO3, Na 2CO3, Na2SiO3, Pb(NO3)2
Задание: проанализируйте данный набор веществ и предложите варианты для работы.
Например: соляная кислота и нитрат серебра; азотная кислота и хлорид бария;
гидроксид калия и сульфат меди (II). Сделайте соответствующие выводы, запишите соответствующие уравнения реакций
Последнее изменение этой страницы: 2018-05-10; просмотров: 196.
stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда.
Источник: stydopedya.ru
Кислотно-основные свойства оксидов и гидроксидов
Свойства соединений элементов IIА группы, в отличие от соединений IА группы, при движении сверху вниз изменяются более резко. Так, во IIА группе при движении сверху вниз резко усиливаются основные свойства, растворимость и термическая устойчивость оксидов и гидроксидов Ме.
Из этих Ме только бериллий образует амфотерные оксид и гидроксид, которые реагируют как с кислотами, так и со щелочами. В воде эти соединения бериллия не растворяются.
Оксид и гидроксид магния также не растворимы в воде, но проявляют уже только основные свойства: реагируют с кислотными оксидами и кислотами, со щелочами и водой не взаимодействуют. Кальций, стронций и барий образуют оксиды и гидроксиды с сильными основными свойствами. Они растворяются в воде, образуя растворы сильных оснований – щелочи. Отсюда произошла первая часть названия Ме кальция, стронция, бария –«щелочноземельные», вторая часть названия произошла из-за сходства термической устойчивости оксидов CaO, SrO, BaO и оксида алюминия, именовавшегося «землей».
Наибольшее практическое применение из оксидов щелочноземельных Ме имеет оксид кальция СаО (техническое название «негашеная известь»). Известняк, мел, мрамор – карбонатные породы, имеющие общую формулу СаСО3. Многие соли s-элементов IIА группы находят применение в медицине.CaCl2*6H2O применяют для снятия сердечно-сосудистого спазма, для улучшения свертываемости крови, при переломах костей и ревматизме.MgSO4*7H2O (горькая соль, магнезия) используется при гипертонии, как слабительное и желчегонное средство.BaSO4 применяют как контрастное вещество при рентгеноскопии пищевода и желудка. 2CaSO4*H2O (алебастр) широко используется в травматологии, стоматологии и строительстве, т.к. при замешивании его с водой образуется нерастворимый CaSO4*2H2O (гипс )
Источник: mydocx.ru