Д. Брожения
Е. С йодом
Ж. Этерификации
Огромная просьба! Если Вы не уверены в правильности Вашего ответа, лучше не отвечайте, от Вашего ответа много зависит, пожалуйста, отнеситесь с пониманием!
Реакция с йодом:
При взаимодействии йода с крахмалом образуется соединение включения (клатрат) канального типа.
Химизм анаэробного разложения, или брожения крахмала, состоит из двух фаз.
Первая фаза – это гидролиз крахмала под действием выделяемых микробами экзоферментов до α-глюкозы:
(С6Н10О5) n + nН2О ® n С12Н22О11 + n Н2О ® nС6Н12О6
крахмал амилаза мальтоза α-глюкоза
Вторая фаза – это маслянокислое брожение поглощенной микробами α-глюкозы:
С6Н12О6 ® СН3СН2СН2СООН + СН3СООН +СО2 +Н2.
Как и для всех других полисахаридов, для крахмала характерна реакция гидролиза – взаимодействие с водой в присутствии катализаторов, которыми выступают кислоты. Крахмал может гидролизоваться частично образуя в качестве продуктов декстрины – (С6Н10О5)n –вещества с молекулярной массой значительно ниже, чем у крахмала.
Опыты по химии. Гидролиз крахмала
Уравнение гидролиза крахмала
Если гидролиз крахмала протекает полностью, образуется глюкоза (C6H12O6). Этот процесс естественный и протекает в процессе переваривания пищи в желудке.
Полисахариды крахмала образуют ряд сложных и простых эфиров. При действии на крахмал азотной кислоты образуютсянитрокрахмалы:
Нитрованию могут подвергаться как три, так и две гидроксильные группы элементарного звена макромолекулы. Нитрокрахмалы являются взрывчатыми веществами.
В процессе ацетилирования крахмала под действием уксусного ангидрида или уксусной кислоты, как и в процессе нитрования под действием азотной кислоты, могут участвовать либо две, либо три ОН-группы:
Продукт полного ацетилирования трех гидроксильных групп элементарного звена макромолекулы называется триацетатом крахмала.
Крахмал вступает в реакции гидролиза, в результате чего образуется глюкоза, дальше у глюкозы может проходить реакция брожения. Также крахмал реагирует с йодом. Имеет место быть и этерификация крахмала.
Источник: educatic.ru
Взаимодействие глюкозы и сахарозы с гидроксидом меди (II).
Цель занятия: научиться решать экспериментальные задачи на идентификацию органических соединений на примере глюкозы, сахарозы и крахмала.
Оборудование и реактивы: пробирки, штатив для пробирок, держатель для пробирок, нож, марля, ножницы, спиртовка, спички, 5%-ный раствор сульфата меди, 10%-й раствор гидроксида натрия, раствор йода, 1%-ный раствор сахарозы, 10% раствор глицерина, 1% раствор крахмала.
Техника безопасности: соблюдать правила работы с растворами щелочей. Аммиачный раствор оксида серебра нельзя хранить. После опыта неиспользованный раствор нейтрализуют соляной кислотой.
Рекомендации по ходу работы.
1. Данная работа охватывает кислородсодержащие соединения: спирты, альдегиды, кислоты, углеводы. Для успешного выполнения работы необходимо повторить сведения об этих соединениях.
Реакция серебряного зеркала
2. Решите задачи, используя информацию из «Теоретических предпосылок».
Ход практической работы.
Задача № 1. Докажите опытным путем, что виноград (сырой картофель, белый хлеб, рис) содержит крахмал.
Задача №2. Докажите опытным путем, что в спелых яблоках (и других фруктах) содержится глюкоза.
Сделайте вывод согласно цели работы.
Взаимодействие глюкозы и сахарозы с гидроксидом меди (II).
В молекулах сахарозы и глюкозы имеется несколько гидроксильных групп. Поэтому соединения взаимодействуют с гидроксидом меди (II) аналогично трехатомному спирту глицерину (качественная реакция на обнаружение многоатомных спиртов).
Если раствор сахарозы прилить к гидроксиду меди (II), образуется ярко-синий раствор сахарата меди (II):
гидроксид меди (II) сахарат меди (II)
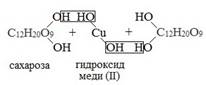
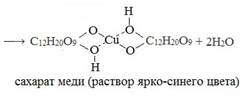
Молекула сахарозы не содержит альдегидной группы.
Глюкоза содержит в своем составе пять гидроксильных групп и одну альдегидную группу. Поэтому она относиться к альдегидоспиртам.
Ее химические свойства похожи на свойства многоатомных спиртов и альдегидов. Реакция с гидроксидом меди (II) демонстрирует восстановительные свойства глюкозы и наличие в ее молекуле нескольких гидроксильных групп. При этом образуется ярко-синий раствор глюконата меди (II).
гидроксид меди (II) глюконат меди (II)
При нагревании полученного раствора с гидроксидом меди (II) идет восстановление двухвалентной меди Cu (II) до одновалентной меди Cu (I). В начале выпадает осадок гидроксида меди (I) CuOН желтого цвета. В процессе дальнейшего нагревания CuOН восстанавливается до оксида меди (I) – Cu2O, который выпадает в виде красного осадка. При этом альдегидная группа окисляется.
В процессе этой реакции глюкоза окисляется до глюконовой кислоты. Подобная реакция указывает на присутствие альдегидной группы в глюкозе.
| С6Н12О6+2Cu(OH)2 t → | СH2OH(CHOH)4-COOH+ 2CuOН↓+ H2O |
| глюкоза | глюконовая кислота желтый |
| 2CuOH t → | Cu2O↓+ H2O |
| желтый | красный |
Реакция «серебряного зеркала» глюкозы доказывает наличие в молекуле альдегидной группы. Реакция серебряного зеркала – это реакция восстановления серебра из аммиачного раствора оксида серебра (реактив Толленса). При этом глюкоза окисляется.
В водном растворе аммиака оксид серебра растворяется с образованием комплексного соединения — гидроксид диамминсеребра(I) [Ag(NH3)2]OH
при добавлении к которому альдегида происходит окислительно-восстановительная реакция с образованием металлического серебра:
Амиачный раствор гидрата окиси серебра получают при взаимодействии нитрата серебра с гидроксидом натрия и гидроксидом аммония:
аммиачный раствор серебра:
Взаимодействие глюкозы с аммиачным раствором оксида серебра при нагревании:

глюкоза глюконовая кислота


Молекула сахарозы является дисахаридим, т.е. состоит из двух моносахаридов: остатков глюкозы и фруктозы. В отличие от свободной глюкозы сахароза не содержит альдегидной группы, что не позволяет веществу вступать в реакцию «Серебряное зеркало».
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Рекомендуем для прочтения:
Электродвижущая сила гальванического элемента (ЭДС) Электрическая работа, получаемая с помощью гальванического элемента, будет максимальной, когда элемент работает в условиях, наиболее.
Психологическая структура личности Психологическая структура личности — это целостная модель.
Анализ состава, структуры и динамики имущества предприятия. Оценка структуры активов Анализ финансового состояния начинают с изучения состава и структуры имущества предприятия по данным актива баланса.
Характеристика кризиса 1-го года Любой кризис в детском развитии обусловлен противоречием между новообразованиями.
Полномочия органов местного самоуправления. Полномочия местного самоуправления – это закрепляемые нормами муниципального права за населением муниципальных образований.
Источник: studopedia.ru
Крахмал вступает в реакции:А. ГидрированияБ. ГидратацииВ. Гидролиза Г. «Серебряного
Крахмал вступает в реакции:
А. Гидрирования
Б. Гидратации
В. Гидролиза
Г. «Серебряного зеркала»
Д. Брожения
Е. С йодом
Ж. Этерификации
Огромная просьба! Если Вы не убеждены в корректности Вашего ответа, превосходнее не отвечайте, от Вашего ответа много зависит, пожалуйста, отнеситесь с пониманием!
Казинова Алиса 2019-09-22 01:47:47
Один вариант ответа?
Artjom Granenov 2019-09-22 01:48:58
Мазутина Варвара 2019-09-22 01:50:43
- Виталя Люханов
- Химия
- 2019-09-22 01:41:05
- 3
- 2
Регина Буман 2019-09-22 01:49:06
Реакция с йодом:
При взаимодействии йода с крахмалом появляется соединение включения (клатрат) канального типа.
Химизм анаэробного разложения, или брожения крахмала, состоит из 2-ух фаз.
1-ая фаза это гидролиз крахмала под деянием выделяемых бактериями экзоферментов до -глюкозы:
(С6Н10О5) n + nН2О n С12Н22О11 + n Н2О nС6Н12О6
крахмал амилаза мальтоза -глюкоза
2-ая фаза это маслянокислое брожение поглощенной бактериями -глюкозы:
С6Н12О6 СН3СН2СН2СООН + СН3СООН +СО2 +Н2.
Как и для всех иных полисахаридов, для крахмала отличительна реакция гидролиза взаимодействие с водой в присутствии катализаторов, которыми выступают кислоты. Крахмал может гидролизоваться отчасти образуя в качестве товаров декстрины (С6Н10О5)n вещества с молекулярной массой веско ниже, чем у крахмала.
Уравнение гидролиза крахмала
Если гидролиз крахмала протекает полностью, образуется глюкоза (C6H12O6). Этот процесс естественный и протекает в процессе переваривания еды в желудке.
Полисахариды крахмала образуют ряд трудных и обычных эфиров. При деяньи на крахмал азотной кислоты образуютсянитрокрахмалы:
Нитрованию могут подвергаться как три, так и две гидроксильные группы простого звена макромолекулы. Нитрокрахмалы являются взрывчатыми субстанциями.
В процессе ацетилирования крахмала под действием уксусного ангидрида или уксусной кислоты, как и в процессе нитрования под действием азотной кислоты, могут участвовать либо две, или три ОН-группы:
Продукт полного ацетилирования 3-х гидроксильных групп элементарного звена макромолекулы именуется триацетатом крахмала.
Источник: obrazovalka.com