План изучения этого вещества целесообразно построить так, чтобы сразу после ознакомления с физическими свойствами альдегидов учащиеся изучили способы получения его, затем химические свойства и т.д. Несколько более раннее ознакомление со способами получения альдегида даст возможность далее, при изучении химических свойств (реакции окисления), рассматривать альдегиды как звено в цепи окисления углеводородов.
В качестве образца при ознакомлении со свойствами формальдегида можно пользоваться формалином. При этом следует сразу же добиться, чтобы учащиеся отчетливо понимали разницу между формалином и формальдегидом.
Запах формальдегида. Из физических свойств формальдегида наиболее доступно на практике ознакомление с запахом. Для этой цели на ученические столы раздаются пробирки с 0,5-1 мл формалина. После того как учащиеся ознакомятся с запахом, формалин может быть собран и использован для дальнейших опытов. Ознакомление с запахом формалина даст возможность учащимся обнаруживать это вещество в других опытах.
Опыты по химии. Окисление муравьиного альдегида гидроксидом меди (II)
Горючесть формальдегида. Нагревают формалин в пробирке и поджигают выделяющиеся пары; они горят почти бесцветным пламенем. Пламя можно заметить, если в нем поджечь лучинку или бумажку. Опыт проводят в вытяжном шкафу.
Получение формальдегида. Так как до ознакомления с химическими свойствами формальдегид может быть обнаружен только по запаху, то первый опыт получения его следует поставить в виде лабораторной работы.
1. В пробирку наливают несколько капель метанола. В пламени горелки нагревают свернутый в трубочку небольшой кусочек медной сетки или спираль из медной проволоки и быстро опускают ее в метанол.
При прокаливании медь окисляется и покрывается черным налетом оксида меди, в спирте она снова восстанавливается и становится красной:
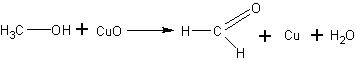
Обнаруживают резкий запах альдегида. Если процесс окисления повторить 2—3 раза, то можно получить значительную концентрацию формальдегида и раствор использовать для последующих опытов.
2. Кроме оксида меди для получения формальдегида могут быть использованы другие знакомые учащимся окислители.
К слабому раствору перманганата калия в демонстрационной пробирке добавляют 0,5 мл метанола и смесь нагревают до кипения. Появляется запах формальдегида, а фиолетовая окраска перманганата исчезает.
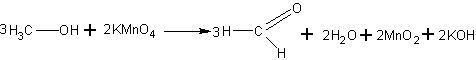
В пробирку наливают 2—3 мл насыщенного раствора бихромата калия К2Сг2О7 и такой же объем концентрированной серной кислоты. Добавляют по каплям метанол и очень осторожно подогревают смесь (отверстие пробирки направляют в сторону!). Далее реакция идет с выделением тепла. Желтая окраска хромовой смеси исчезает, и появляется зеленая окраска сульфата хрома
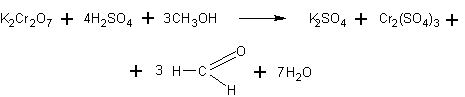
Уравнение реакции с учащимися можно не разбирать. Как и в предыдущем случае, им лишь сообщается, что бихромат калия окисляет метиловый спирт в альдегид, превращаясь при этом в соль трехвалентного хрома Cr2(SO4)3.
Взаимодействие формальдегида с оксидом серебра (реакция серебряного зеркала). Этот опыт должен быть продемонстрирован учащимся так, чтобы он одновременно явился и инструктажем к последующему практическому занятию.
Природа аммиачного раствора оксида серебра может быть подробно разъяснена учащимся, а можно лишь сообщить им, что образующийся при реакции гидроксид серебра — вещество непрочное и легко распадается на оксид серебра и воду:
Оксид серебра обладает свойством растворяться в аммиаке.
Окислительное действие оксида серебра объясняется тем, что это вещество является оксидом благородного металла, поэтому оксид неустойчив и при наличии восстановителя, т.е. вещества, легко окисляющегося, он легко отдает кислород, вследствие чего происходит выделение (восстановление) металлического серебра. Уравнение реакции можно дать в обычном виде:
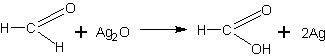
а можно представить полное уравнение реакции:
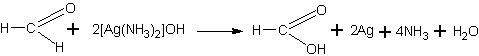
Серебряное зеркано образуется в том случае, если восстанавливающееся серебро осаждается на гладких стенках сосуда из не слишком концентрированных растворов. Малейшие загрязнения мешают восстанавливающемуся серебру «уцепиться» за стекло и заставляют его выделяться в виде рыхлого осадка. Значительно меньшее влияние на успех опыта оказывает характер нагревания. Если сосуд недостаточно чист, то даже самое осторожное нагревание не дает зеркала, и наоборот, если сосуд подготовлен тщательно, то даже нагревание смеси на открытом огне может дать желаемый результат.
Первый опыт получения серебряного зеркала следует провести в колбочке, а не в пробирке.
Колбу емкостью 50—100 мл до урока очищают от механических загрязнений, промывают ершиком с мыльной водой или нагревают в колбе раствор щелочи, затем споласкивают водой, промывают хромовой смесью и наконец начисто промывают дистиллированной водой.
В колбу наливают на четверть объема 2-процентный раствор нитрата серебра, затем добавляют постепенно раствор аммиака
(25-процентный аммиак следует разбавить в 8-10 раз) до тех пор, пока образующийся вначале осадок не растворится в его избытке. К образующемуся раствору добавляют осторожно по стенке 0,5-1 мл формалина и помещают колбу в стакан с горячей (лучше кипящей) водой. Вскоре в колбе образуется красивое серебряное зеркало.
Колбу можно нагревать без водяной бани, непосредственно на маленьком пламени, обнося пламя вокруг колбы и не встряхивая ее.
При демонстрации опыта вместо серебряного зеркала иногда образуется черный осадок. Учитель в таком случае обычно совершенно бракует опыт. Между тем при таком результате следует разъяснить учащимся, что здесь также произошло восстановление серебра только в виде рыхлого черного осадка.
Окисление формальдегида гидроксидом меди (II). В пробирку наливают 2 мл 5-процентного раствора формальдегида, 2 мл 10-процентного раствора гидроксида натрия и при встряхивании добавляют по каплям 2-процентный раствор сульфата меди (11) до появления неисчезающей взвеси. Содержимое пробирки нагревают до начала кипения и наблюдают изменение окраски реакционной смеси а именно: голубая окраска меняется на желтую (осадок), а затем на красную (осадок). Эта реакция, как и реакция серебряного зеркала, является качественной реакцией на альдегиды. Суммарное уравнение этой реакции следующее:
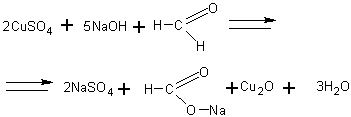
Однако с учащимися целесообразно рассматривать этот процесс поэтапно:
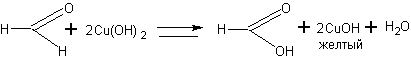
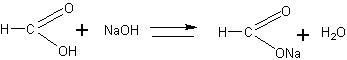
Обращают внимание учащихся на то, что реакция протекает в
щелочной среде, поэтому образуется не муравьиная кислота, а соль как продукт нейтрализации. Изменяющаяся цветовая гамма продуктов является результатом превращений соединений меди, связанных с изменением степени ее окисления.
Дезинфицирующее действие формальдегида. Дезинфицирующее действие формальдегида объясняется его свойством свертывать белок.
К нескольким миллилитрам формалина в пробирке добавляют 1 мл куриного белка. Белок свертывается.
Полимеризация и деполимеризация альдегида. Формальдегид, как это впервые показал А.М.Бутлеров, легко уплотняется.
В продаже существует твердый полимер формальдегида — параформальдегид (СН2О)n или параформ.
а) Параформ может быть легко деполимеризован.
В сухую пробирку помещают несколько крупинок параформа и нагревают. Вещество разлагается, образуя газообразный формальдегид, который частично улетает (запах!), а частично на холодных стенках пробирки снова образуется полимер. Опыт объясняет применение параформа для дезинфекции помещений.
б) Полимеризацию формальдегида можно наблюдать при выпаривании его раствора.
Выпаривают осторожно на водяной бане в фарфоровой чашке 4—5 мл формалина. Образуется твердый остаток. Остаток нагревают на голом огне. Происходит деполимеризация и улетучивание продукта (вытяжной шкаф). Убедившись в этом, прекращают нагревание.
Взаимодействие формальдегида с аммиаком. Нагревая формальдегид с аммиаком, А.М.Бутлеров получил уротропин, широко известное антисептическое средство.
В фарфоровой чашке на водяной бане выпаривают смесь равных объемов формалина и концентрированного раствора аммиака. По мере улетучивания жидкости остаются бесцветные кристаллы уротропина (гексаметилентетрамина (CH2)6N4)N.
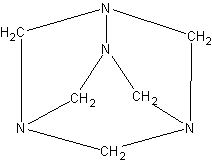
Знакомство учащихся со структурной формулой уротропина может быть лишь довольно поверхностным, так как класс аминов
еще не изучался. Однако структурная формула может быть ими осмыслена на основе знания валентности элементов.
С синтезированным или готовым уротропином можно выполнить следующие опыты. Нагревают уротропин в фарфоровой чашке, он улетучивается не плавясь. Раствор уротропина даст щелочную реакцию. При действии раствора щелочи уротропин разлагается, выделяющийся аммиак можно обнаружить обычными способами. При действии раствора серной кислоты на раствор уротропина (нагревание) также происходит разложение его, выделяющийся формальдегид может быть обнаружен по запаху.
Получение фенолформальдегидных смол. Основная масса получаемого в промышленности формальдегида идет на синтез фенолформальдегидных и других смол, необходимых для производства пластических масс. В основе получения фенолформальдегидных смол лежит реакция поликонденсации.
Наиболее доступен в школьных условиях синтез фенолформальдегидной смолы. Учащиеся к этому времени знакомы уже с обоими исходными веществами для получения смолы — фенолом и формальдегидом; опыт сравнительно несложен и идет безотказно; химизм процесса не представляет особой трудности для учащихся, если изобразить его следующим образом:
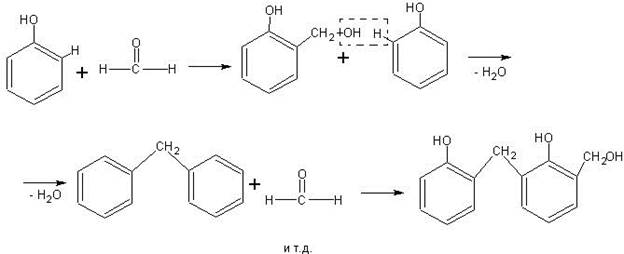
В зависимости от количественного соотношения фенола и формальдегида, а также от применяемого катализатора (кислотный или щелочной) может получаться новолачная или резольная смола. Первая из них термопластична и имеет линейную структуру, приведенную выше. Вторая — термореактивна, так как в ее линейных молекулах содержатся свободные спиртовые группы — СН2ОН, способные реагировать с подвижными водородными атомами других молекул, в результате чего образуется трехмерная структура.
В процессе классного изучения нет необходимости отдельно демонстрировать опыты получения новолачной и резольной смолы. Достаточно показать на одном опыте сам факт образования
высокомолекулярного соединения. В процессе внеклассных занятий можно получить смолы разного типа и даже формовать изделия из них. Опыты необходимо проводить под тягой вследствие летучести формальдегида.
а) Нагревают в пробирке на пламени спиртовки смесь 2,5 г кристаллического фенола и 5 мл формалина (40-процентного). Даже при кипении жидкости в ней не наблюдается химической реакции. Приливают к смеси 7-8 капель соляной кислоты (1 : 1). Вскоре происходит бурная реакция, и жидкость становится мутной. Охлаждают пробирку и дают смеси отстояться: внизу образуется смола, сверху — вода.
Сливают водный слой и выливают смолу на лист картона или жести. Застывшая смола имеет светло-желтую окраску. Опыт убедительно показывает роль соляной кислоты как катализатора реакции.
б) Не ставя целью показать роль катализатора, опыт можно провести проще. Нагревают в пробирке смесь указанных выше количеств фенола, формальдегида и кислоты, пока не начнется бурная реакция. После того как образуется муть, дают смеси расслоиться и далее поступают как в предыдущем случае.
в) Действие аммиака в качестве катализатора можно проследить на следующем опыте, который можно поставить и в несколько укрупненном масштабе.
В большую пробирку насыпают 4—5 г фенола, приливают 10 мл 40-процентного формалина и 1—2 мл концентрированного раствора аммиака. Смесь нагревают в течение нескольких минут в пламени горелки. После того как смесь вскипит (бурная реакция) и затем сделается мутной вследствие образования смолы, охлаждают пробирку и дают жидкости расслоиться.
Сливают верхний водный слой и демонстрируют в пробирке вязкую жидкость — фенолформальдегидную смолу. Затем смолу помещают в пробирке или в какой-нибудь формочке в сушильный шкаф, Через час-полтора (иногда раньше) смола превращается в твердую пластмассу. Так очень упрощенно может быть имитировано производство литых изделий из смолы.
г) Действие щелочного и кислотного катализатора на процесс поликонденсации можно показать одновременно. В две пробирки помешают по 2,5 г фенола и по 5 мл формалина. Затем в одну пробирку приливают 1 мл концентрированного раствора аммиака, а в другую — 7—8 капель соляной кислоты. Пробирки помешают в кипящую водяную баню. Через 5—10 мин в пробирках образуется смола.
Сливают после отстаивания верхний водный слой и затем выливают смолу на листы картона или жести.
д) В химическом кружке учащиеся могут получить фенолфор-
мальдегидную смолу в большем количестве и с более тщательным соблюдением режима.
В круглодонную колбу с обратным холодильником помещают 25 г фенола, 50 мл формалина и 3 мл 40-процентного раствора едкого натра. Осторожно нагревают смесь через асбестированную сетку. Нагрев регулируют так, чтобы жидкость не кипела слишком бурно.
По мере нагревания жидкость становится все более вязкой и примерно через час настолько густеет, что пузырьки газа с трудом вырываются на поверхность. Выливают жидкость в пробирку, При охлаждении она образует непрозрачную твердую массу. Чтобы довести процесс поликонденсации до образования трехмерной структуры, пробирку помещают в сушильный шкаф, где выдерживают продукт 1 ч при 50— 60°С и 3—4 ч при 70— 80°С. Образуется твердая нерастворимая смола ярко-розового цвета.
Дата добавления: 2018-11-26 ; просмотров: 2029 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Источник: poznayka.org
Окисление альдегидов: процесс, конечный продукт

Альдегидами называют органические вещества, относящиеся к карбонильным соединениям, содержащим функциональную группу –СОН, которая именуется карбонильной группой.
В зависимости от характера углеводородного скелета молекулы альдегиды бывают предельными, непредельными и ароматическими. Их молекулы могут также включать атомы галогенов или дополнительные функциональные группы. Общая формула насыщенных альдегидов имеет вид CnH2nO. В соответствии с номенклатурой ИЮПАК названия их оканчиваются суффиксом –аль.
Окисление альдегидов имеет важное значение в промышленности, поскольку они довольно легко превращаются в карбоновые кислоты. Окислителями в этом случае могут послужить гидроксид меди, оксид серебра или даже кислород воздуха.
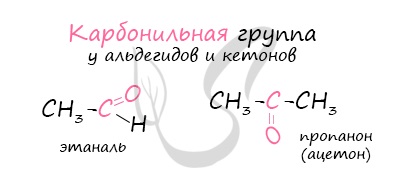
Строение карбонильной группы
Электронное строение двойной связи в группе С=О характеризуется образованием одной σ-связи и еще одной π-связи. Атом С находится в состоянии sp 2 -гибридизации, молекула плоского строения с валентными углами между связями около 120 0 . Отличие двойной связи в этой функциональной группе заключено в том, что она расположена между атомом углерода и весьма электроотрицательным атомом кислорода. В результате электроны притянуты к атому О, а значит, эта связь очень сильно поляризована.
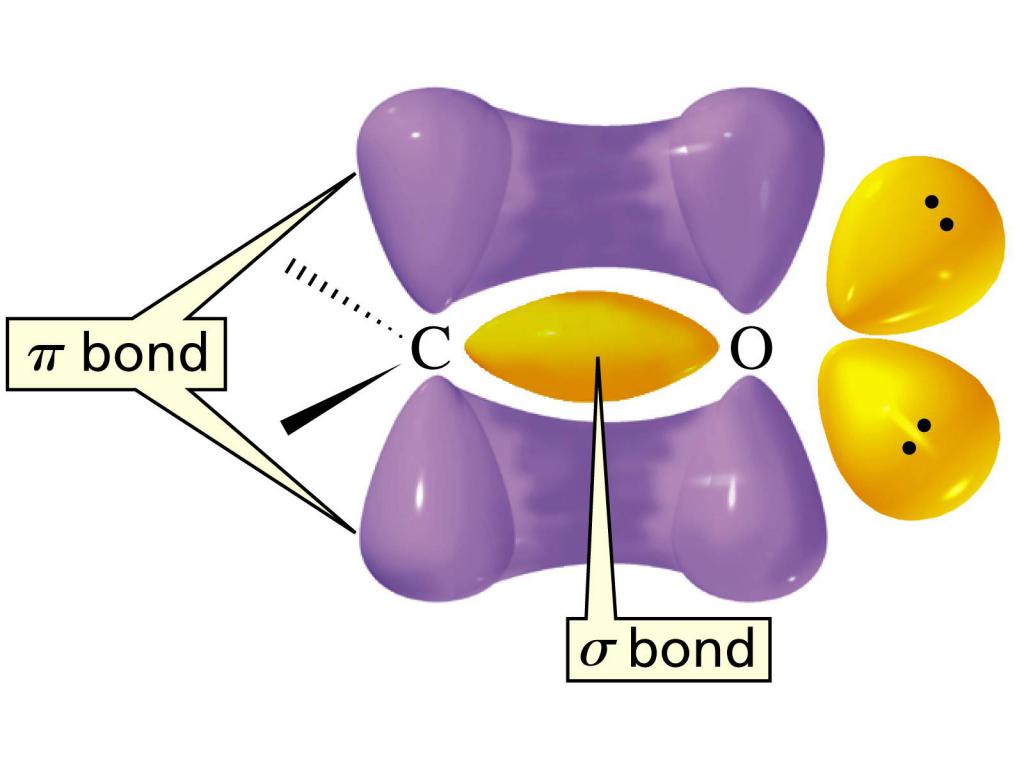
Содержание в альдегидной группе такой поляризованной двойной связи можно назвать главной причиной высокой реакционноспособности альдегидов. Для альдегидов наиболее характерны реакции присоединения атомов или их групп по С=О связи. И легче всего протекают реакции нуклеофильного присоединения.
Также для альдегидов типичны реакции с участием атомов Н из функциональной группы альдегидов. Из-за электроноакцепторного влияния группы С=О происходит повышение полярности связи. Это в свою очередь является причиной относительно легкого окисления альдегидов.
Отдельные представители альдегидов
Формальдегид (муравьиный альдегид или метаналь) СН2О является газообразным веществом с весьма острым запахом, который получают обычно пропусканием смеси паров метанола с воздухом через раскаленную сетку из медной или серебряной сетки. Его 40%-й водный раствор называется формалином. Формальдегид легко вступает в реакции, многие из которых лежат в основе промышленного синтеза целого ряда важных веществ. Его используют и для получения изопренового каучука, пентаэритрита, многих лекарственных веществ, различных красителей, для дубления кожи, в качестве дезинфицирующего и дезодорирующего средства. Формальдегид довольно токсичен, его ПДК в воздухе составляет 0,001 мг/л.
Ацетальдегид (уксусный альдегид, этаналь) СН3СОН является бесцветной жидкостью с удушающим запахом, который при разбавлении его водой приобретает фруктовый аромат. Ацетальдегид обладает всеми основными свойствами альдегидов. Окислением уксусного альдегида производят огромные объемы уксусной кислоты и уксусного ангидрида, разнообразных фармацевтических препаратов.
Акролеин (пропеналь) CH2=CH-СОН, простейший ненасыщенный альдегид является бесцветной легколетучей жидкостью. Его пары сильно раздражают слизистые глаз и верхних дыхательных путей. Очень ядовит, ПДК его содержания в воздухе составляет 0,7 мг/м 3 . Пропеналь — промежуточный продукт синтеза некоторых полимеров, необходим в производстве отдельных лекарственных препаратов.

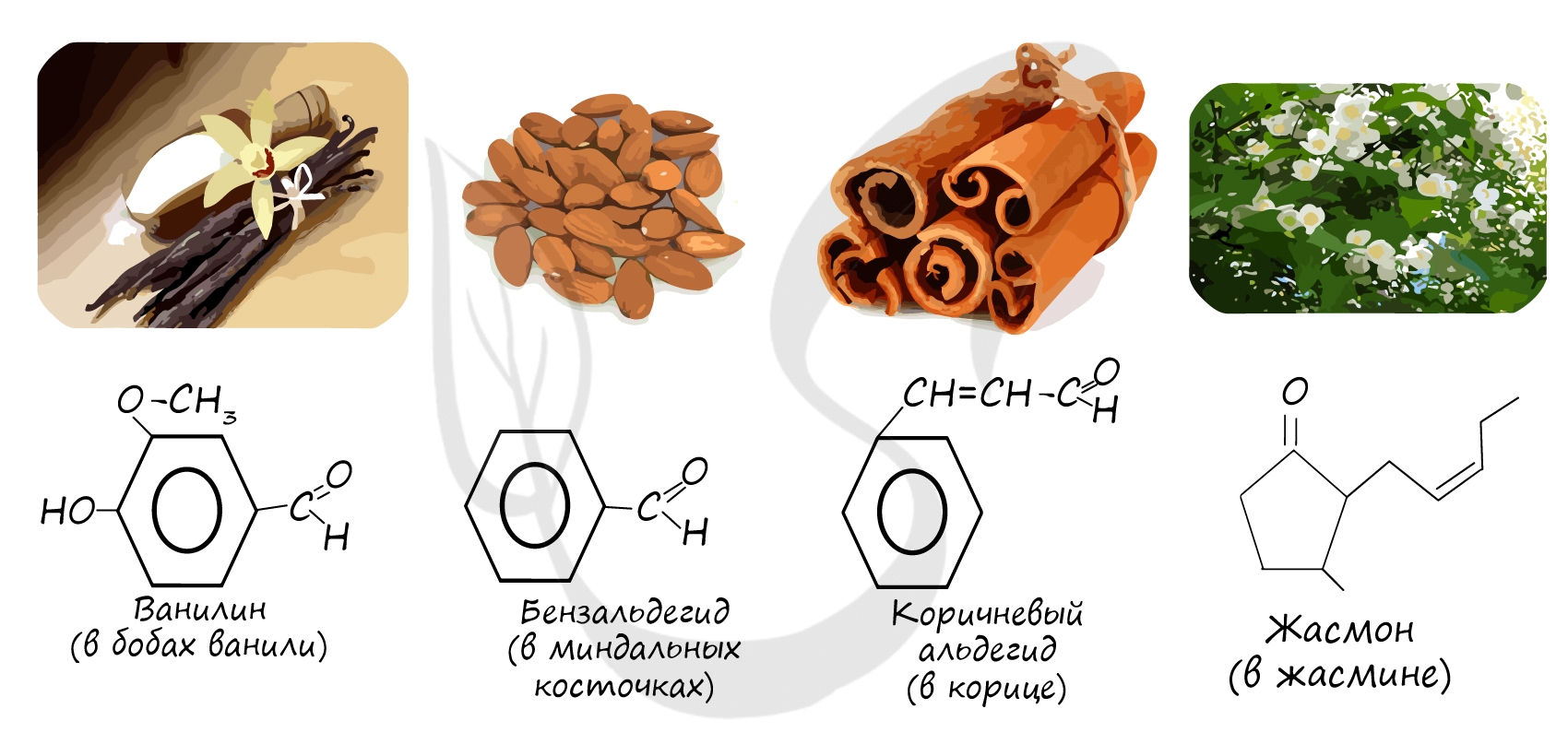
Бензальдегид (бензойный альдегид) С6Н5СОН является бесцветной желтеющей при хранении жидкостью с ароматом горького миндаля. Он довольно быстро окисляется воздухом до бензойной кислоты. Содержится в эфирных маслах растений (нероли, пачулей), а в виде глюкозида — в ядрах косточек горького миндаля, вишни, абрикоса и персика. Как душистое вещество его применяют в парфюмерии, в виде компонента пищевых эссенций, как сырье для синтеза других душистых веществ (коричного альдегида, жасминальдегида).
Реакция серебряного зеркала
Окисление альдегидов оксидом серебра является самой показательной качественной реакцией на соответствующую форму функциональной группы. Свое название эта реакция получила благодаря тонкому серебряному налету на стенках пробирки, образующемуся в ходе этой реакции.
Суть ее заключается во взаимодействии альдегида R-СОН с аммиачным раствором оксида серебра(I), который представляет собой растворимое комплексное соединение [Ag(NH3)2]OH и носит название реактив Толленса. Реакцию осуществляют при температурах, близких к температуре кипения воды (80–100 °С). При этом происходит окисление альдегидов до соответствующих им карбоновых кислот, а окислитель восстанавливается до металлического серебра, выпадающего в осадок.
Приготовление реактивов
Для качественного определения группы -СОН в альдегидах сначала готовят комплексное соединение серебра. Для этого в пробирку наливают немного раствора аммиака (гидроксида аммония) в воде и следом небольшое количество нитрата серебра. При этом образующийся осадок оксида серебра тут же исчезает:
Более надежные результаты дает реактив Толленса, приготовленный с добавлением щелочи. Для этого 1 г AgNO3 растворяют в 10 г дистиллированной воды и добавляют равный объем концентрированного гидроксида натрия. В результате выпадает осадок Ag2O, который исчезает при добавлении концентрированного раствора гидроксида аммония. Использовать для проведения реакции нужно только свежеприготовленный реактив.

Механизм реакции
Стоит отметить, что для альдегидов такое взаимодействие изучено недостаточно. Механизм данной реакции неизвестен, но предполагается радикальный или же ионный вариант окисления. По гидроксиду диамминсеребра вероятнее всего реализуется присоединение с образованием серебряной соли диола, от которого затем отщепляется серебро с образованием карбоновой кислоты.
Для успешного проведения опыта чрезвычайно важна чистота используемой посуды. Связано это с тем, что образующиеся в ходе опыта коллоидные частицы серебра должны прицепиться к поверхности стекла, создав зеркальную поверхность. В присутствии малейших загрязнений оно будет выпадать в виде серого хлопьевидного осадка.
Для очистки емкости следует использовать растворы щелочей. Так, для этих целей можно взять раствор NaOH, который нужно смыть большим объемом дистиллированной водой. На поверхности стекла не должно присутствовать жировых следов и механических частиц.
Окисление гидроксидом меди
Реакция окисления альдегидов гидроксидом меди (II) также довольно эффектна и эффективна в определении типа функциональной группы. Протекает она при температуре соответствующей кипячению реакционной смеси. При этом альдегиды восстанавливают двухвалентную медь в составе реактива Фелинга (свежеприготовленный аммиачный раствор Cu(OH)2) до одновалентной. Сами же они окисляются по причине внедрения атома кислорода по связи С-Η (степень окисления С изменяется с +1 на +3).
Визуально за ходом реакции можно проследить по изменению окраски смеси растворов. Голубоватый осадок гидроксида меди постепенно превращается желтый, соответствующий гидроксиду меди одновалентной и дальнейшее появление яркого красного осадка Cu2O.
Этому процессу соответствует уравнение реакции:
R-СОН + Cu 2+ + NaOH + Н2О -> R-COONa + Cu2O + 4Н +
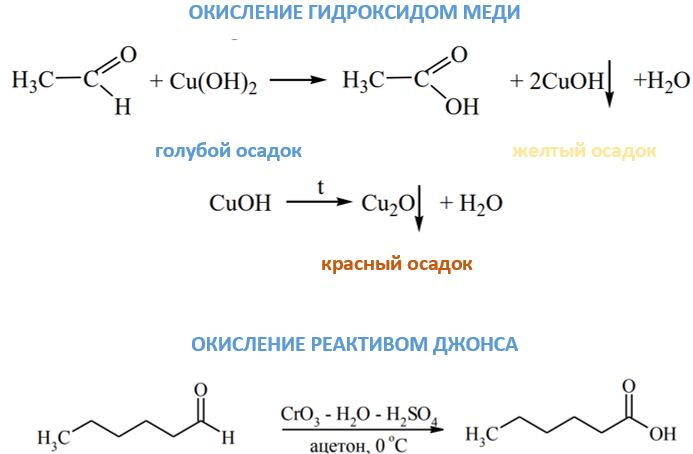
Действие реактивом Джонса
Стоит отметить, что на альдегиды такой реактив действует наилучшим образом. В этом случае окисление не требует нагревания и проводится при температуре 0-20 °С в течение довольно короткого отрезка времени, а выход продуктов составляет больше 80%. Главным недостатком реагента Джонса состоит в отсутствии высокой избирательности в отношении других функциональных групп, да к тому же кислая среда порой приводит к изомеризации или деструкции.
Реагент Джонса представляет собой раствор оксида хрома (VI) в разбавленной серной кислоте и ацетоне. Его также можно получить из дихромата натрия. При окислении альдегидов образуются под действием этого реактива карбоновые кислоты.
Промышленное окисление кислородом
Окисление ацетальдегида в промышленности осуществляют воздействием кислорода в присутствии катализаторов — ионов кобальта или марганца. Сначала образуется надуксусная кислота:
Она в свою очередь взаимодействует со второй молекулой уксусного альдегида и через перекисное соединение дает две молекулы уксусной кислоты:
Окисление ведется при температуре 60-70 °С и давлении 2·10 5 Па.
Взаимодействие с раствором йода
Для окисления альдегидных групп иногда применяется раствор йода в присутствии щелочи. Особое значение этот реактив имеет в процессе окисления углеводов, поскольку действует очень избирательно. Так под его влиянием D-глюкоза превращается в D-глюконовую кислоту.
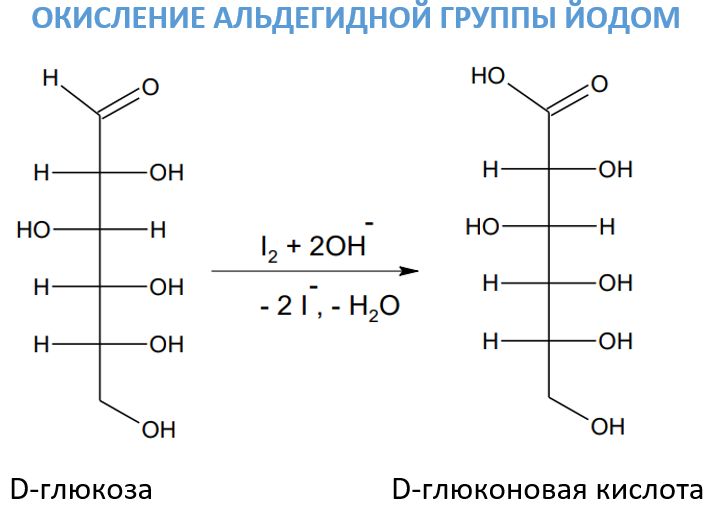
Йод в присутствии щелочей образует гипойодид (весьма сильный окислитель): I2 + 2NaOΗ –> NaIO + NaI + Н2О.
Под действием гипойодида формальдегид превращается в метановую кислоту: ΗСОΗ + NaIO + NaOΗ –> ΗCOONa + NaI + Н2О.
Окисление альдегидов йодом используют в аналитической химии для определения количественного их содержания в растворах.
Окисление диоксидом селена
В отличие от предыдущих реактивов, под действием диоксида селена альдегиды превращаются в дикарбонильные соединения, а из формальдегида образуется глиоксаль. Если рядом с карбонилом расположены метиленовые или метильные группы, то они могут превращаться в карбонильные. Как растворитель для SeO2 обычно используют диоксан, этанол или ксилол.
По одной из методик реакцию проводят в трехгорлой колбе, соединенной с мешалкой, термометром и обратным холодильником. К исходному веществу, взятому в количестве 0,25 моль, каплями прибавляют раствор 0,25 моль диоксида селена в 180 мл диоксана, а также 12 мл Н2О. Температура не должна превышать 20 °C (при необходимости колбу охлаждают).
После этого при постоянном перемешивании раствор кипятят в течении 6 часов. Далее горячий раствор фильтруют для отделения селена и промывают осадок диоксаном. После вакуумной отгонки растворителя остаток фракционируют. Основную фракцию отбирают в широком температурном интервале (20-30 °C) и повторно ректифицируют.
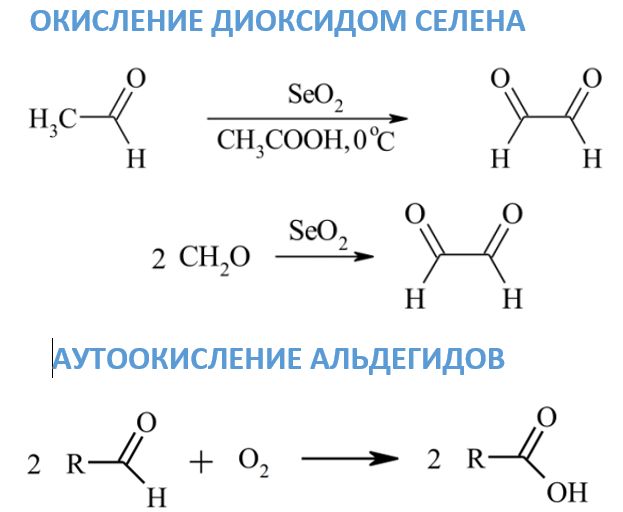
Аутоокисление альдегидов
Под действием кислорода воздуха при комнатной температуре окисление альдегидов происходит очень медленно. Главными продуктами этих реакций являются соответствующие карбоновые кислоты. Механизм аутоокисления родственен промышленному окислению этаналя до уксусной кислоты. Одним из промежуточных продуктов является надкислота, которая взаимодействует с еще одной молекулой альдегида.
Благодаря тому, что этот тип реакций ускоряется под действием света, перекисей, и следов тяжелых металлов, можно сделать вывод о ее радикальном механизме. Формальдегид в водных растворах значительно хуже своих собратьев окисляется воздухом, из-за того, что существует в них в виде гидратированного метиленгликоля.

Окисление альдегидов перманганатом калия
Наиболее успешно эта реакция происходит в кислой среде. Визуально оценить ее прохождение можно по потере интенсивности и полному обесцвечиванию розовой окраски раствора марганцовки. Реакция проходит при комнатной температуре и нормальном давлении, поэтому она не требует особых условий. Достаточно в пробирку налить 2 мл формальдегида и 1 мл подкисленного серной кислотой раствора перманганата калия. Пробирку с раствором нужно осторожно встряхнуть для перемешивания реагентов:
Если ту же реакцию вести при повышенных температурах, то метаналь легко окисляется до углекислого газа:
Источник: fb.ru
Формальдегид реакция серебряного зеркала уравнение
В данном опыте используется 40%-ный водный раствор формальдегида H2C=O (формалин). Для доказательства наличия альдегидной группы CH=O к формалину добавляют аммиачный раствор оксида серебра. В результате реакции на стенках сосуда образуется зеркальный налёт серебра.
Альдегиды
Альдегиды — летучие жидкости органического состава, являющиеся продуктом неполного окисления спиртов. Карбонильная группа в молекулах альдегидов связана с одним атомом водорода и одной группой R.
Не часто встречаются в природе в отдельном виде, но, несомненно, играют важную роль в физиологических процессах растений и животных. Общая формула альдегидов CnH2nO.
Многие альдегиды имеют специфический запах. Высшие альдегиды, в особенности непредельные, используются в пищевой промышленности и парфюмерии.
Номенклатура и изомерия альдегидов
Названия альдегидов формируются путем добавления суффикса «аль» к названию алкана с соответствующим числом атомов углерода: метаналь, этаналь, пропаналь, бутаналь, пентаналь и т.д.
Вы можете встретить их молекулярные формулы, где группа OH записана наоборот — HO. Например: метаналь — HCHO, этаналь — CH3CHO, пропаналь — C2H5CHO. Это делают специально для того, чтобы их было легче отличить от спиртов.
Многие альдегиды имеют тривиальные названия. Наиболее известные: метаналь — формальдегид, этаналь — ацетальдегид. Замечу, что формалином называется 40% раствор формальдегида.
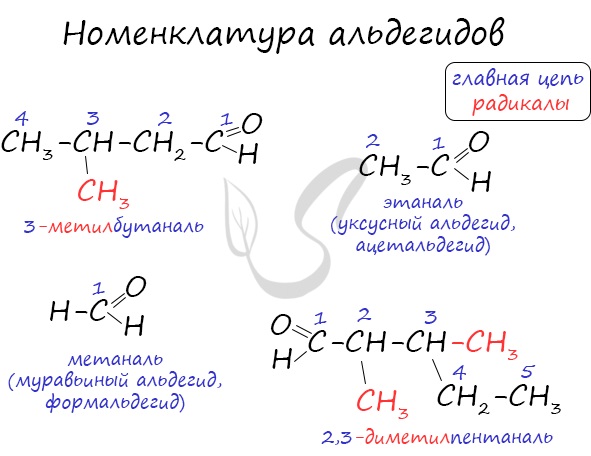
Для альдегидов характерна структурная изомерия: углеродного скелета, межклассовая изомерия с кетонами.
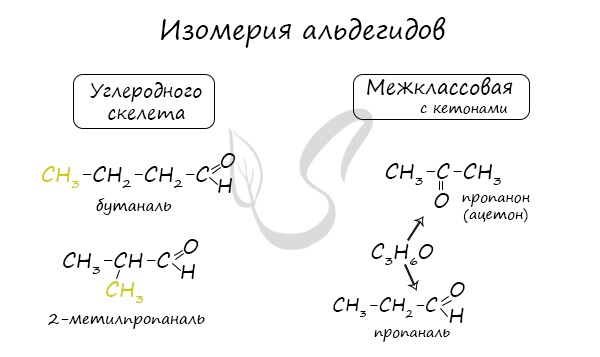
Получение альдегидов и кетонов
- Окисление спиртов
Важно заметить, что при окислении первичных спиртов образуются альдегиды, при окислении вторичных спиртов — кетоны. Окисление с помощью оксида меди относится к лабораторным способам получения альдегидов.
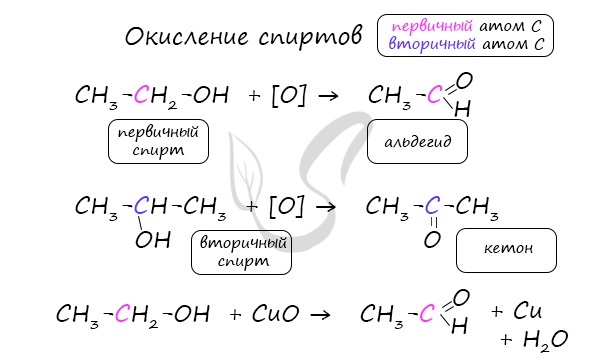
Этот способ также просто осуществить в лабораторных условиях. При пиролизе (нагревании без доступа кислорода) кальциевых или бариевых солей карбоновых кислот возможно получение кетонов.

В присутствии катализатора и при нагревании спиртов от гидроксогруппы и прилежащего к ней атома углерода отщепляется по атому водорода. В результате образуется карбонильная группа.
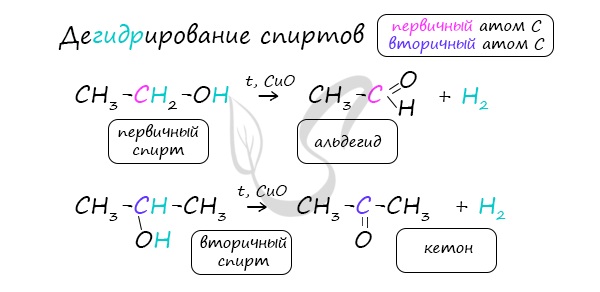
Реакцией Кучерова называют гидратацию алкинов в присутствии солей двухвалентной ртути.
В результате такой реакции ацетилен превращается в уксусный альдегид. Все остальные его гомологи: пропин, бутин, пентин и т.д. превращаются в соответствующие кетоны.
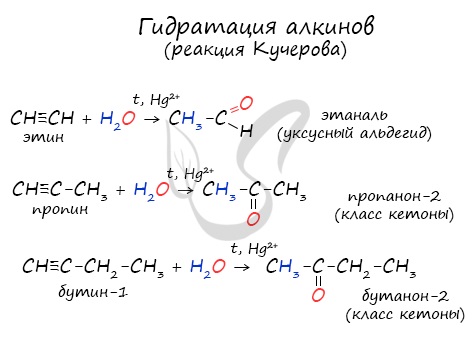
Для получения альдегида два атома галогена должны находиться у первичного атома углерода, для получения кетонов — у вторичного.
В результате такого гидролиза образуются двухатомные спирты, в которых две OH-группы прилежат к одному атому углерода. Такие соединения неустойчивы и распадаются на карбонильное соединение (альдегид или кетон) и воду.
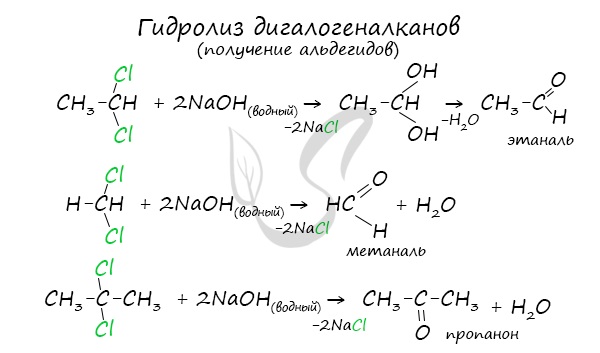
В промышленности окислением метана при температуре 500 °C и в присутствии катализатора получают формальдегид.

В прошлой теме, посвященной фенолам, мы касались данного способа. В результате такой реакции образуется не только фенол, но и ацетон.
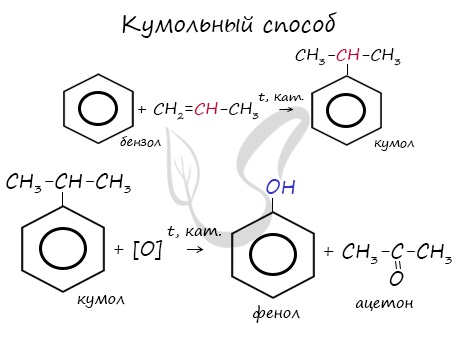
Химические свойства альдегидов и кетонов
Запомните, что для альдегидов и кетонов характерны реакции присоединения по карбонильной группе. Это является важным отличием альдегидов от карбоновых кислот, для которых реакции присоединения не характерны.
Для понимания механизма реакции важно вспомнить об электроотрицательности. В карбонильной группе кислорд, как более электроотрицательный элемент, тянет электронную плотность на себя от углерода. На атоме кислорода возникает частичный отрицательный заряд (δ-), а на атоме углерода частичный положительный (δ+).
Основы школьного курса физики подсказывают, что отрицательный заряд притягивает положительный: именно так и будет происходить при присоединении различных молекул к карбонильной группе альдегидов и кетонов.
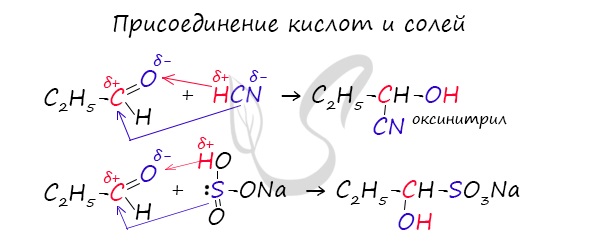
Реакция гидрирования альдегидов происходит по типу присоединения, сопровождается разрывом двойной связи в карбонильной группе. Гидрирование альдегидов приводит к образованию первичных, а гидрирование кетонов — вторичных спиртов.
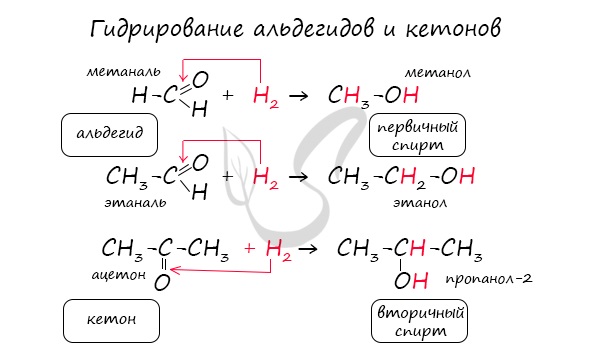
В результате полного окисления, горения, образуется углекислый газ и вода.
Альдегиды легко окисляются до карбоновых кислот в лабораторных условиях. Это осуществляется с помощью известной реакции серебряного зеркала. Данная реакция является качественной для альдегидов.
Кетоны, в отличие от альдегидов, в реакции окисления не вступают.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли

Важно заметить, что при окислении метаналя, образовавшаяся муравьиная кислота тут же окисляется до угольной кислоты, которая распадается на углекислый газ и воду. Это связано с интересным фактом — наличием альдегидной группы у муравьиной кислоты.

Окисление также возможно другим реагентом — гидроксидом меди II. Эта реакция также относится к качественным для альдегидов, в результате образуется кирпично-красный осадок оксида меди I.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Реакция серебряного зеркала
Реакция серебряного зеркала является качественной реакцией на альдегиды, это реакция восстановления серебра из раствора аммиачного комплекса серебра [Ag(NH3)2]OH. Альдегиды легко окисляются под действием мягких окислителей, в том числе и под действием данного комплекса. К тому же реакция может быть очень интересна и для обычных показательных опытов. В результате опыта в колбе (пробирке) образуется тонки красивый зеркальный налет серебра.
На одном из занятий по химии решили получить «серебряное зеркало» . Все реактивы подготовили за неделю до самого опыта. На следующем занятии обнаружили в колбе на стенках осадок, от которого решили избавиться фильтрованием. Но стояло только потрясти колбу, как произошел взрыв!
Объяснение произошедшему в следующем: аммиачный комплекс серебра при хранении разрушается с образованием нитрида серебра Ag3N —«гремучего серебра»
Данное соединение очень неустойчиво и при небольшом физическом воздействии, даже если находится в жидкости, разлагается на азот и серебро:
Реакция происходит настолько интенсивно, что происходит взрыв. Вот почему следует использовать только свежеприготовленные растворы в данном опыте!
Для проведения опыта нам понадобятся:
- Водный раствор аммиака
- нитрат серебра
- формальдегид
В пробирку нальем немного водного раствора аммиака. Добавим немного нитрата серебра. Это необходимо для получения аммиачного комплекса серебра.
Уравнение данной реакции:
К полученному раствору добавим несколько капель формальдегида и немного нагреем пробирку. Через некоторое время на стенках пробирки начнет появляться осадок серебра.
Если опыт проводится в пробирке с чистыми и гладкими стенками, то серебро выпадает в виде тонкого налета, создавая зеркальную поверхность. При наличии малейших загрязнений серебро будет выделяется в виде серого рыхлого осадка.
В результате опыт имеем колбу с тонкой пленкой из чистого серебра:

Источник: al-shell.ru