Электролизом называют процессы, происходящие на электродах под действием электрического тока, подаваемого от внешнего источника.
При электролизе происходит превращение электрической энергии в химическую.
Ячейка для электролиза, называемая электролизером, состоит из двух электродов и электролита (рис. 6.3).
Электрод, на котором идет реакция восстановления (катод), у электролизера подключен к отрицательному полюсу внешнего источника тока. Электрод, на котором протекает реакция окисления (анод), подключен к положительному полюсу источника тока.
Рассмотрим электродные реакции на примере электролиза расплава хлорида натрия.
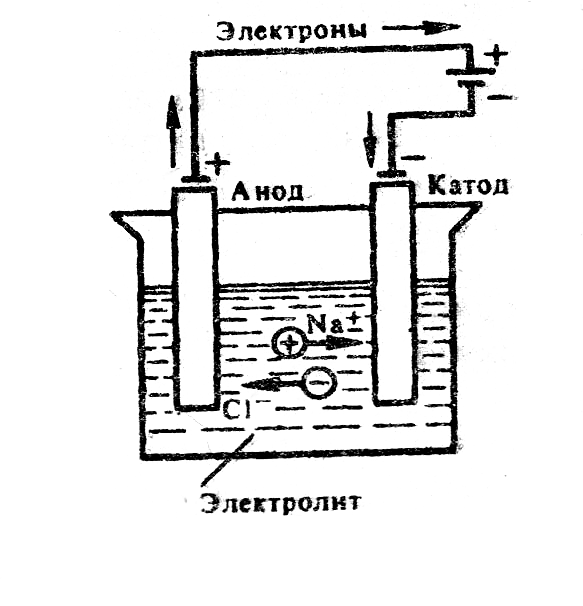
Рис. 6.3. Схема электролиза расплава NaCl
При плавлении происходит термохимическая диссоциация соли:

.
Если погрузить инертные (угольные) электроды и пропускать постоянный электрический ток, то ионы будут двигаться к электродам: катионы Na + – к катоду, анионы Cl — – к аноду (рис. 6.3.). В итоге на катоде выделяется металлический натрий, а на аноде – хлор:
Электролиз расплавов и растворов солей, щелочей, кислот
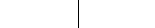
 2 восстановление
2 восстановление
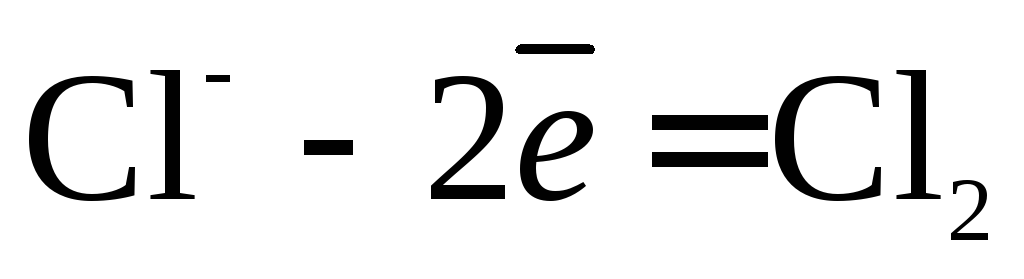
1 окисление


Электролиз растворов солей
Пример 1. Электролиз водного раствора .
При электролизе водных растворов солей нужно учитывать: 1) все ионы в водном растворе гидратированы; 2) в водном растворе помимо самого вещества присутствуют молекулы воды и ионы Н + и ОН — .
Электролит 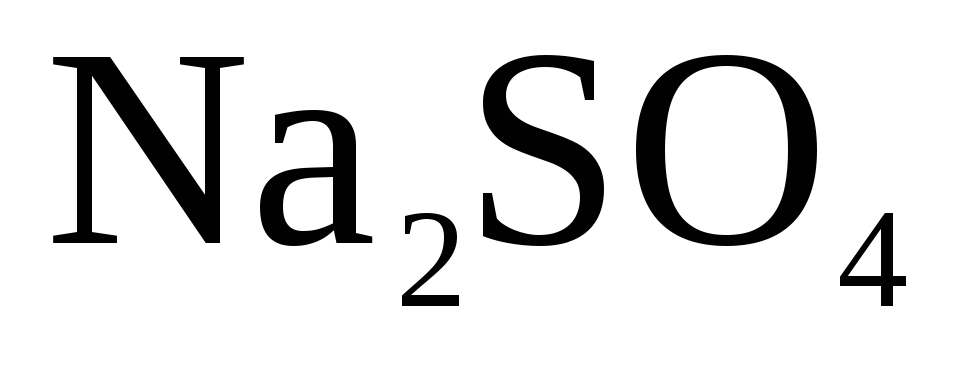 состоит из следующих частиц, способных участвовать в электродных процессах:
состоит из следующих частиц, способных участвовать в электродных процессах: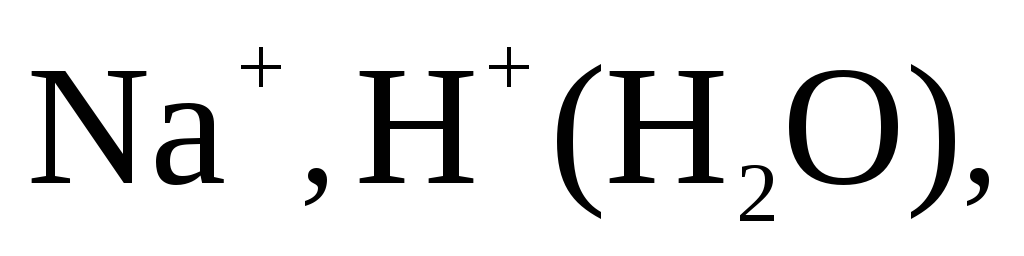
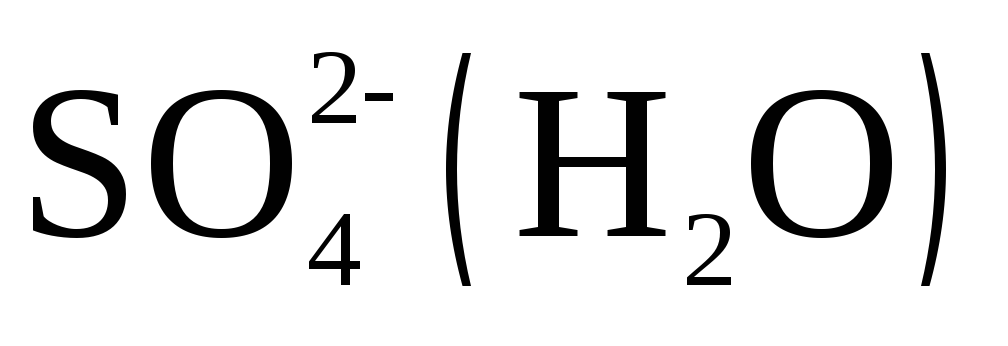 и
и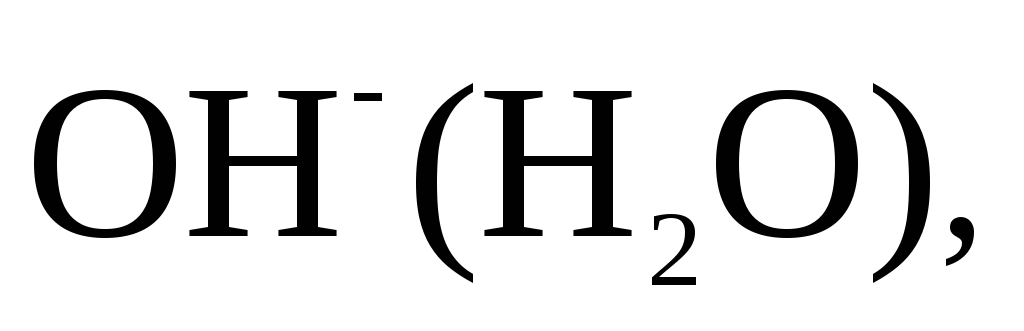 а также воды. Концентрация ионов
а также воды. Концентрация ионов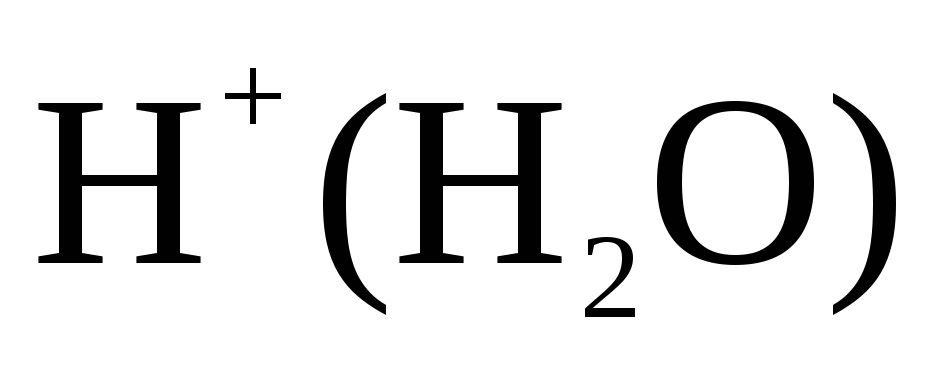 и
и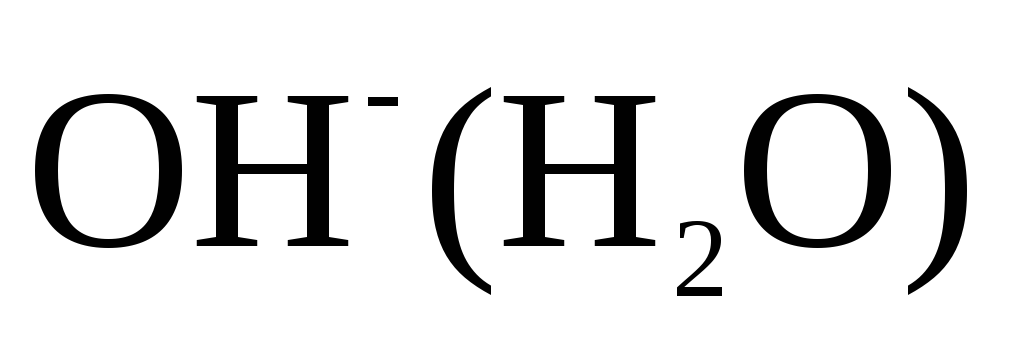 мала, так как обусловлена слабой диссоциацией молекул
мала, так как обусловлена слабой диссоциацией молекул .
.
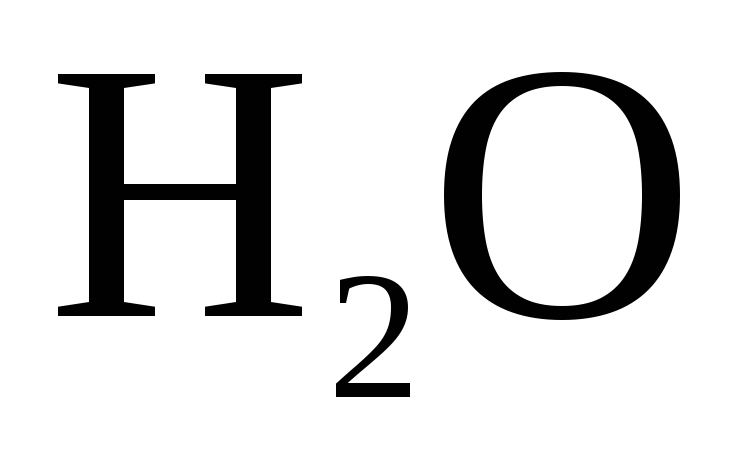
Восстанавливаться на катоде могут только молекулы :
Электролиз серебра по колхозному
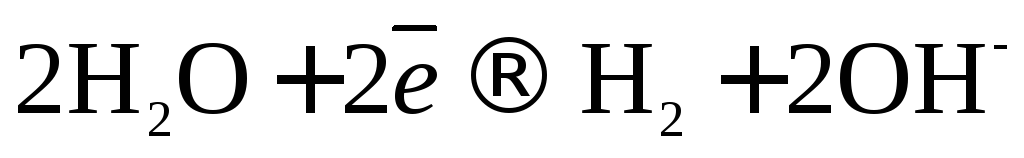
Восстановление катионов 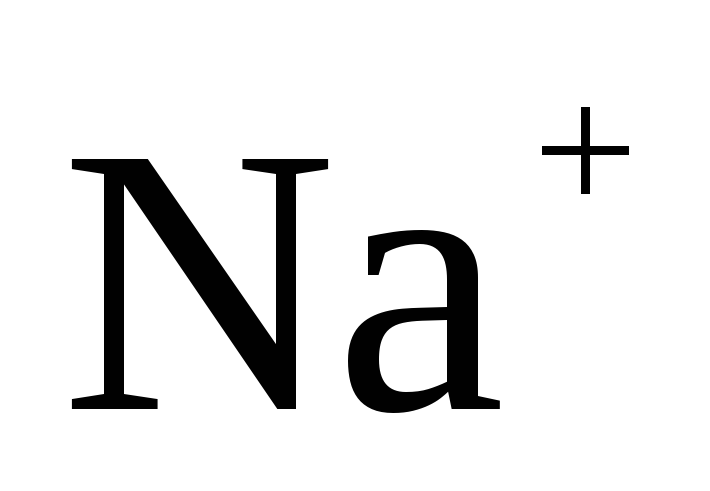 невозможно из-за электроотрицательного потенциала (
невозможно из-за электроотрицательного потенциала (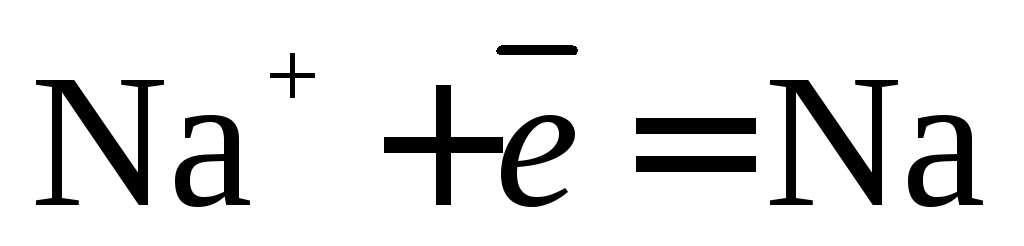
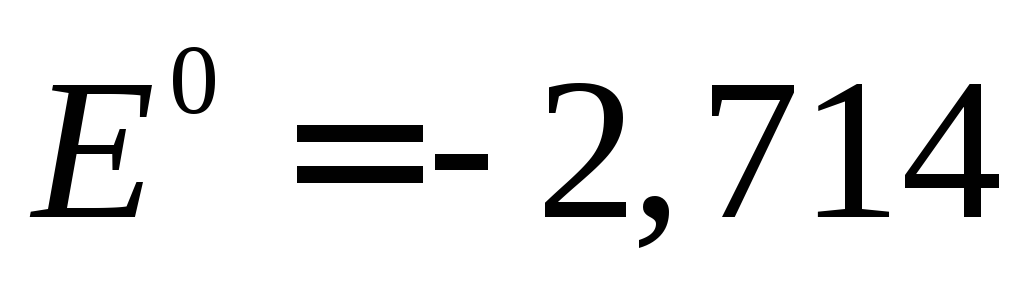 В).
В).
Из-за возможных процессов окисления:

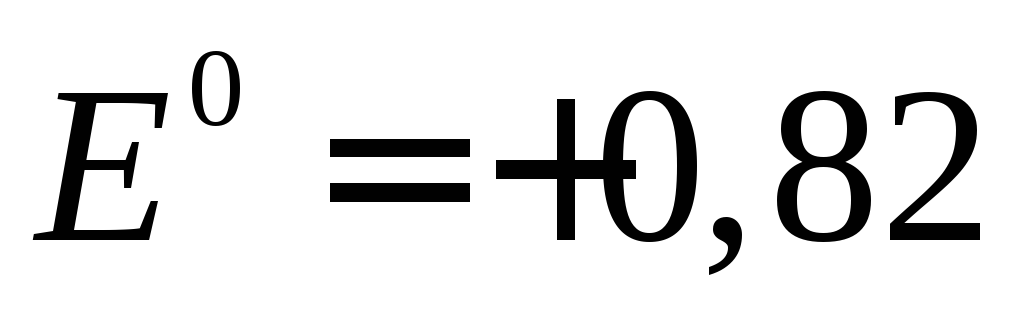 В,
В,
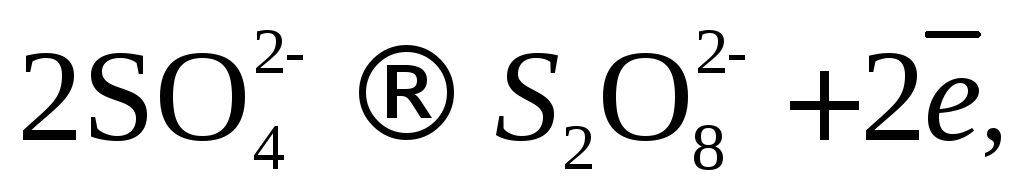
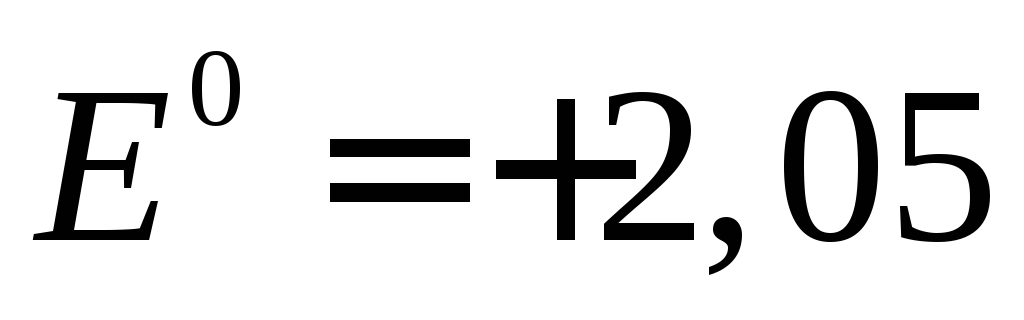 В.
В.
на аноде будет протекать реакция, которой отвечает меньший потенциал, то есть окисление воды с выделением О2.
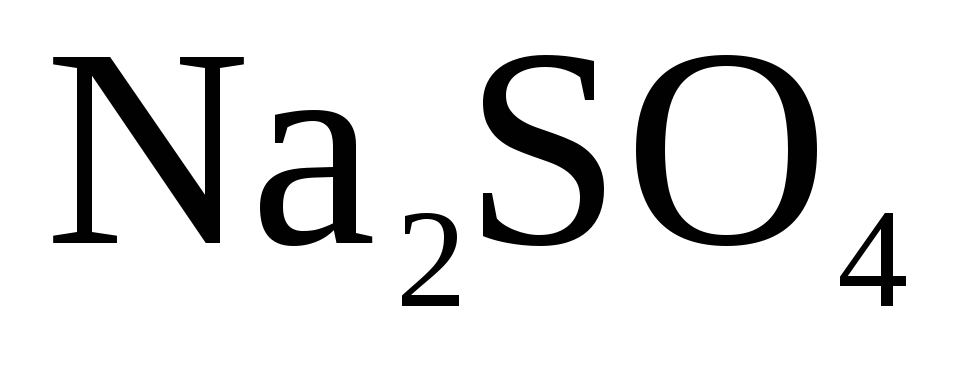
Итак, при электролизе водного раствора на катоде выделяется Н2, а на аноде – О2.
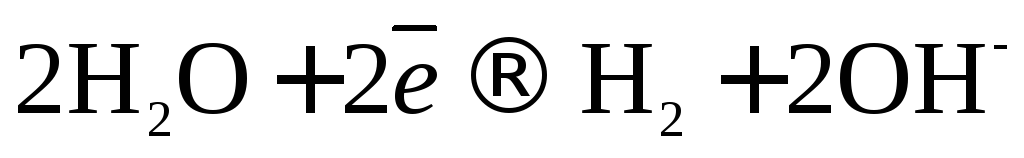
,

.
причем электролит около катода становится щелочным, а около анода – кислым.
Суммарный процесс электролиза

.
Подобное изменение среды в электролите у катода и анода может быть использовано для получения щелочей и кислот, если обеспечить неперемешиваемость растворов у обоих электродов.

Аналогично протекает электролиз водных растворов солей, образованных щелочными и щелочно-земельными металлами и кислородсодержащей кислотой ().
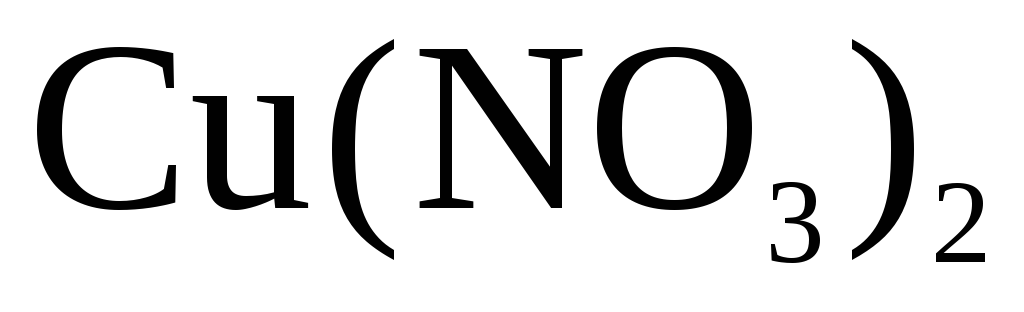
Пример 2. Электролиз водного раствора
На катоде будут восстанавливаться катионы меди:
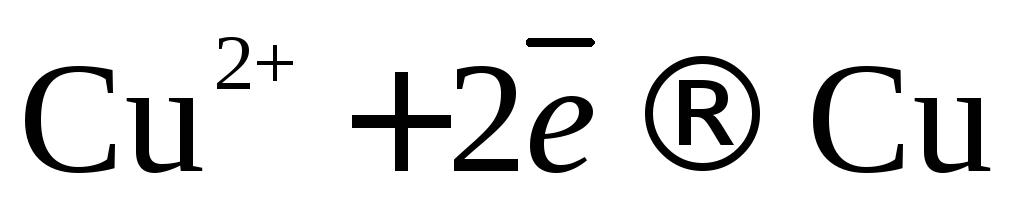
;
на аноде будет кислород в результате реакции окисления воды:

.
Суммарное уравнение электролиза:
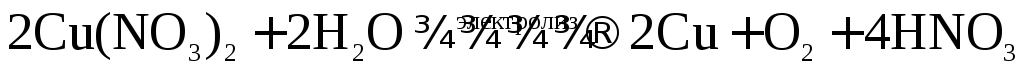
.
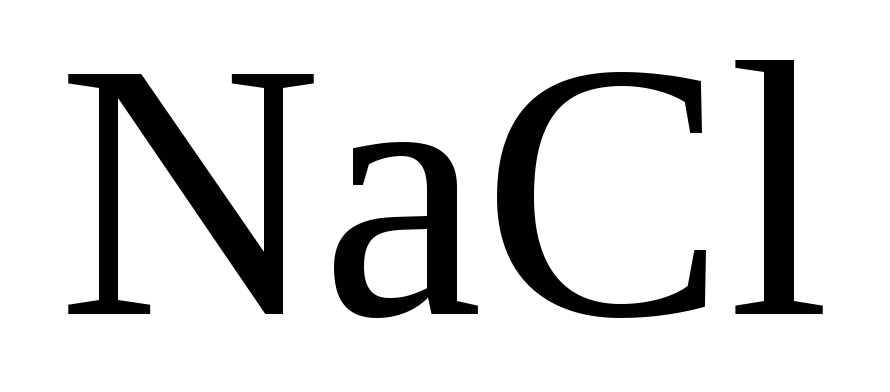
Пример 3. Электролиз раствора .
На катоде при электролизе этого раствора выделяется водород

,
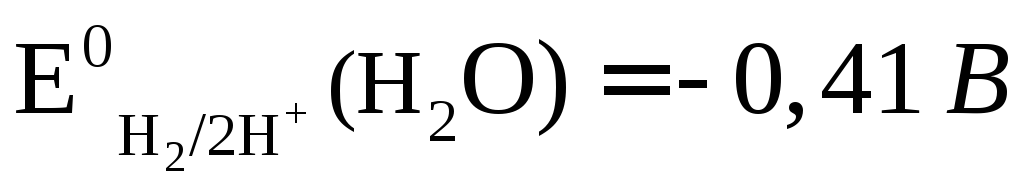
.
На аноде выделяется хлор по реакции
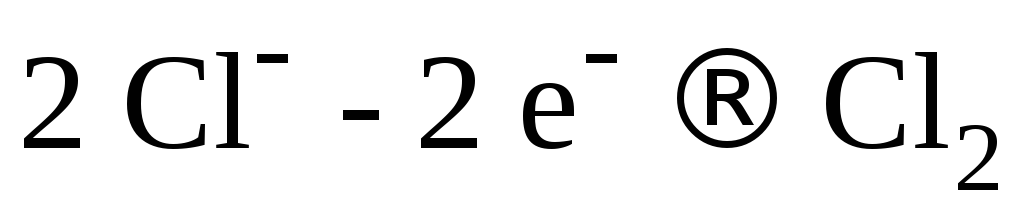
Именно таким путем – электролизом насыщенного раствора хлорида натрия – в промышленности получают хлор.
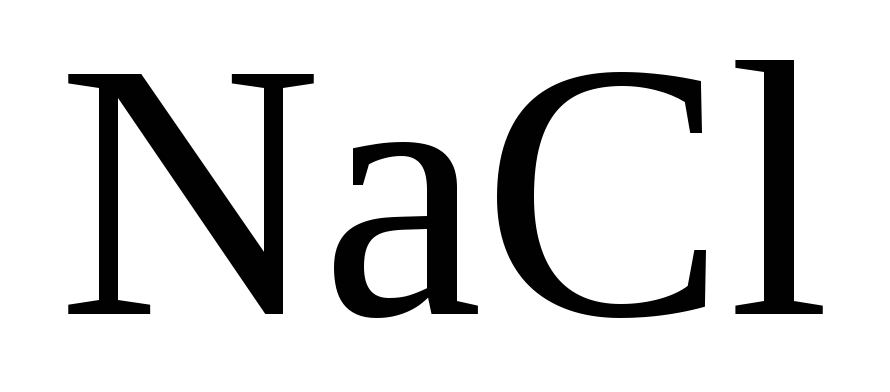
Суммарное уравнение электролиза раствора
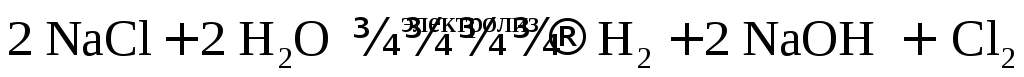
Последовательность разряда ионов.
I. Для процессов, протекающих на катоде:
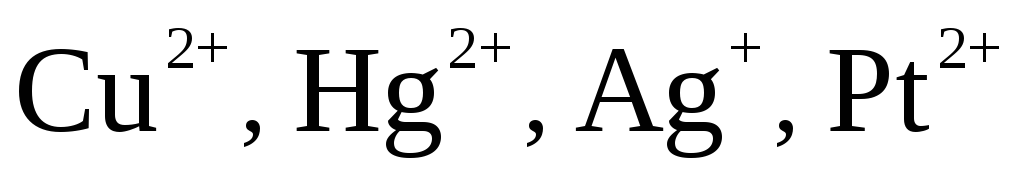
1. При электролизе растворов солей металлов, расположенных в ряду напряжений после Н2 () на катоде выделяется соответствующий металл по схеме:
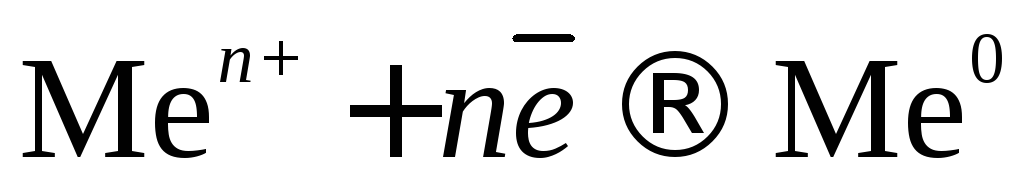
.
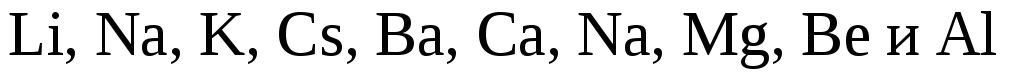
2. При электролизе растворов солей металлов, которые находятся в начале ряда напряжений (), на катоде разряжаются ионы водорода из воды;
3. при электролизе растворов солей металлов, электронные потенциалы которых находятся между потенциалами 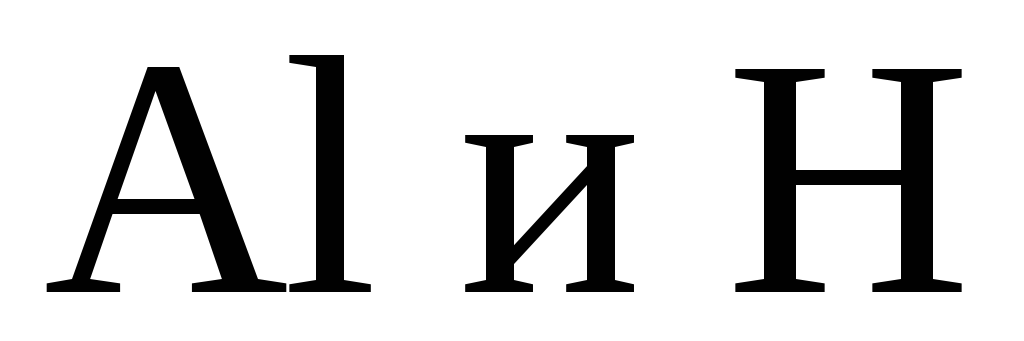 (
(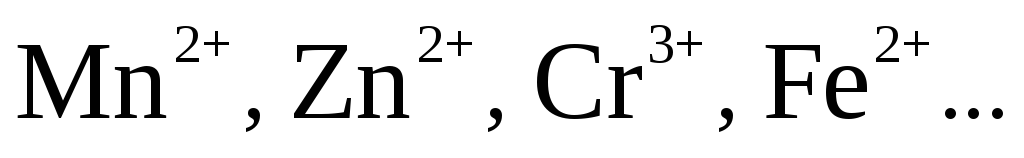 до Н), на катоде выделяется металл и Н2:
до Н), на катоде выделяется металл и Н2:
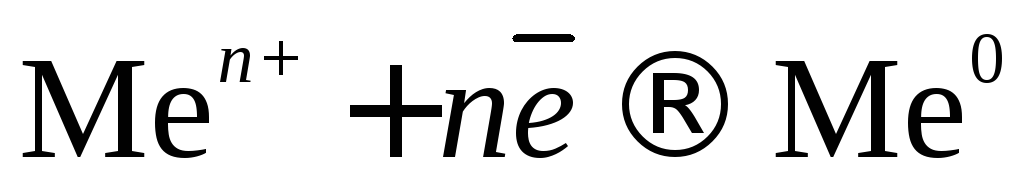
;
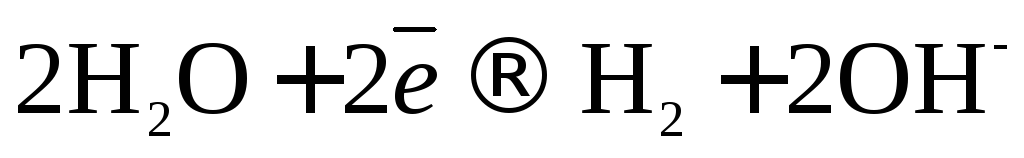
.
Если же водный раствор содержит катионы различных металлов, то при электролизе выделение их на катоде протекает в порядке уменьшения величины стандартного электродного потенциала соответствующего металла. Так, из смеси катионов 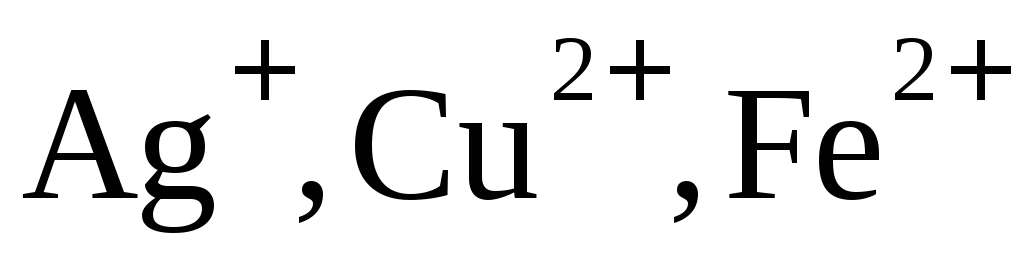
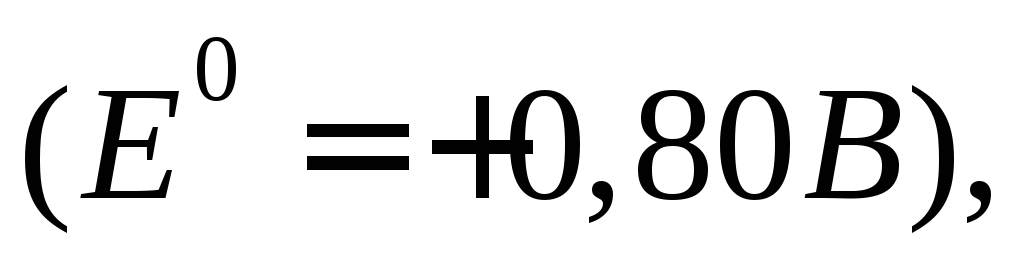 затем катионы меди
затем катионы меди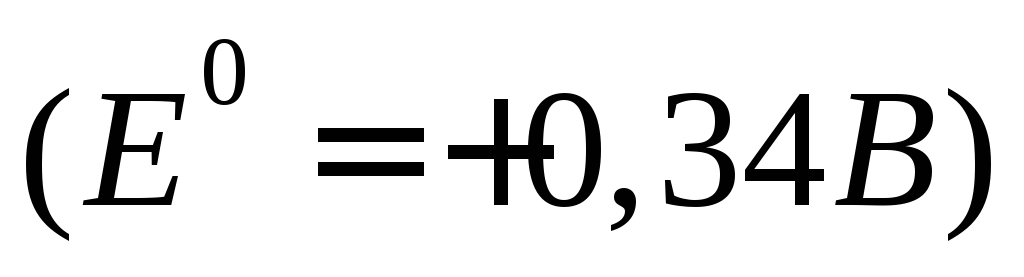 и последними – катионы железа
и последними – катионы железа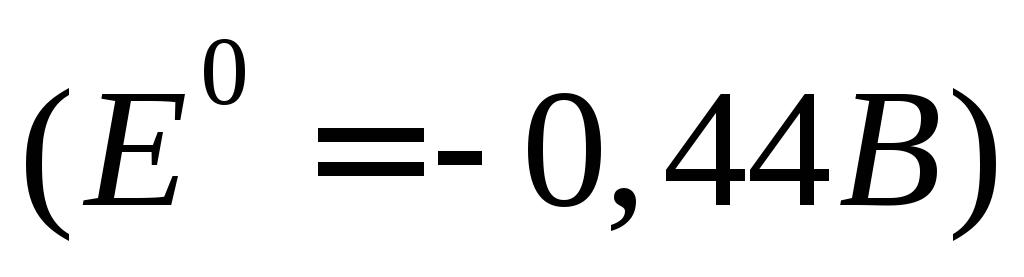 .
.
Вывод. При разрядке ионов на катоде легче разряжаются те из них, которым отвечает наибольшее значение положительного потенциала.
Характер реакций, протекающих на аноде, зависит как от присутствия молекул воды, так и от вещества, из которого сделан анод. Обычно аноды подразделяются на нерастворимые и растворимые. Первые изготавливаются из угля, графита, платины, иридия; вторые – из меди, серебра, цинка, кадмия, никеля и других металлов.
II. Для процессов, протекающих на нерастворимом аноде.
1) При электролизе водных растворов бескислородных кислот и их солей, кроме 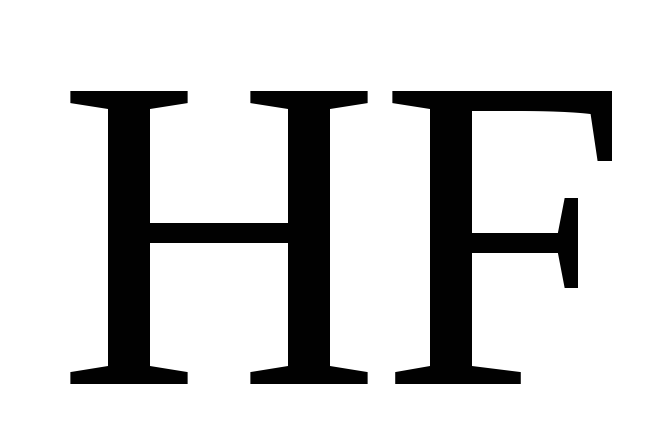 и фторидов, будут окисляться данные анионы. Например, при электролизе (
и фторидов, будут окисляться данные анионы. Например, при электролизе ( и их солей на аноде выделяется
и их солей на аноде выделяется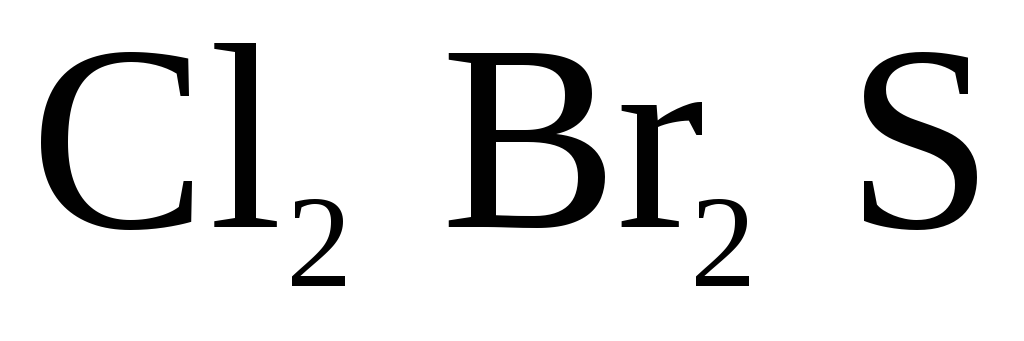 )
)

(галоген)

2) При электролизе кислородсодержащих кислот и их солей (и т. д.) на аноде выделяется О2, так как анодное окисление претерпевают ионы или вода, но потенциал окисления воды значительно меньше, чем для данных анионов.
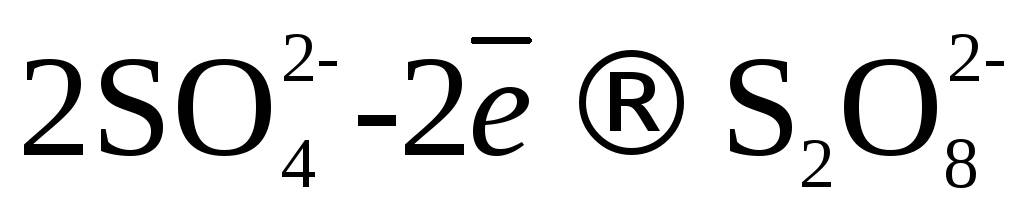
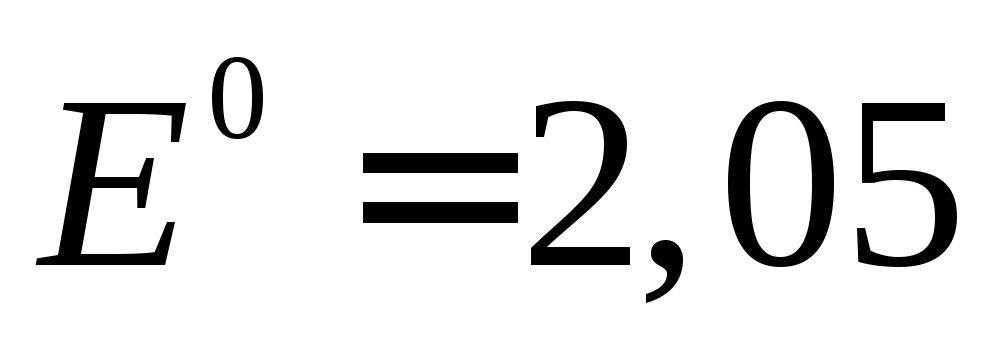 В
В

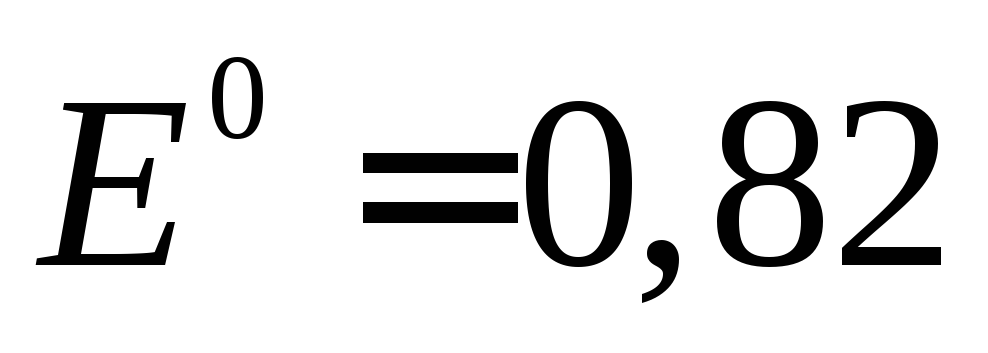 В
В
Вывод. В целом, на аноде происходят в первую очередь те процессы, потенциалы которых более отрицательны, то есть меньше по величине.
Растворимый анод при электролизе сам подвергается окислению, т. е. посылает электроны во внешнюю цепь.
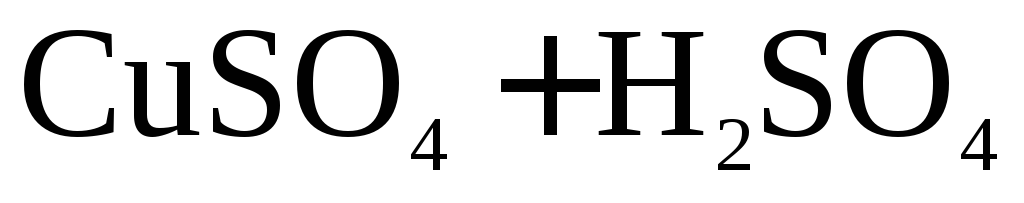
Пример. Два медных электрода помещены в раствор .
Рассмотрим электродные процессы при прохождении электрического тока:
На катоде – восстановление катионов меди:

.
На аноде – окисление меди:
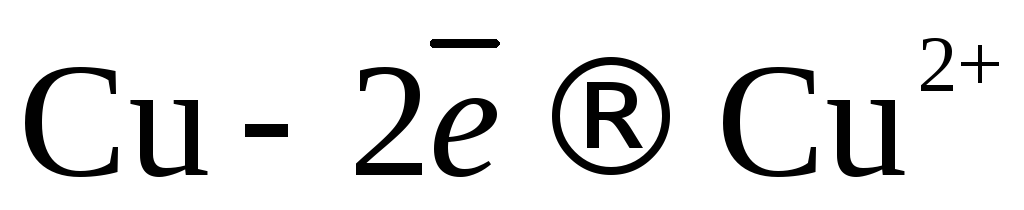
.
Происходит растворение анода:
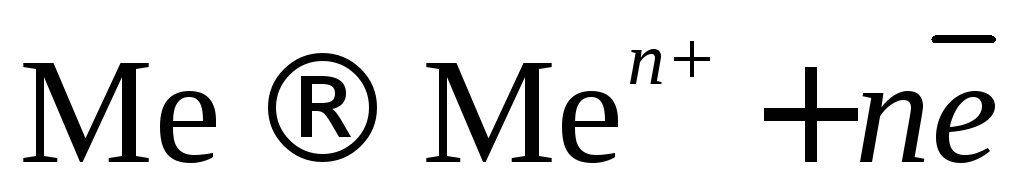
металл уходит уходят во
анода в раствор внешнюю цепь
и анод растворяется. Этот случай электролиза широко используется для очистки металлов.
Источник: studfile.net
Не может быть получен при электролизе водного раствора соли серебра
Электролиз (греч. elektron — янтарь + lysis — разложение) — химическая реакция, происходящая при прохождении постоянного тока через электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно заряженных ионов (анионов) к аноду (заряжен положительно).
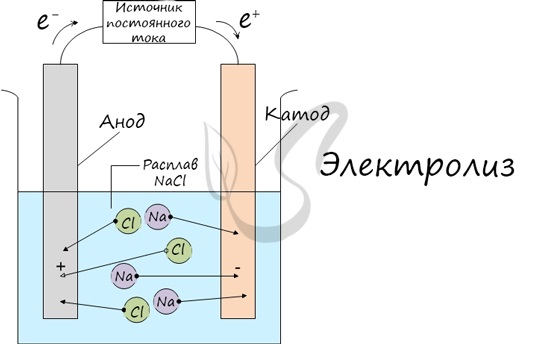
Итак, анионы и катионы устремляются соответственно к аноду и катоду. Здесь и происходит химическая реакция. Чтобы успешно решать задания по этой теме и писать реакции, необходимо разделять процессы на катоде и аноде. Именно так и будет построена эта статья.
Катод
К катоду притягиваются катионы — положительно заряженные ионы: Na + , K + , Cu 2+ , Fe 3+ , Ag + и т.д.
Чтобы установить, какая реакция идет на катоде, прежде всего, нужно определиться с активностью металла: его положением в электрохимическом ряду напряжений металлов.
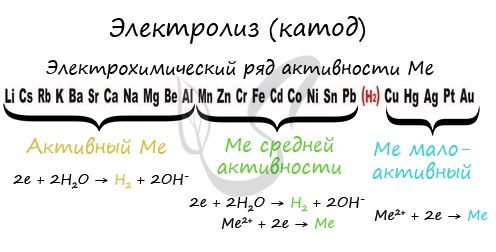
Если на катоде появился активный металл (Li, Na, K) то вместо него восстанавливаются молекулы воды, из которых выделяется водород. Если металл средней активности (Cr, Fe, Cd) — на катоде выделяется и водород, и сам металл. Малоактивные металлы выделяются на катоде в чистом виде (Cu, Ag).
Замечу, что границей между металлами активными и средней активности в ряду напряжений считается алюминий. При электролизе на катоде металлы до алюминия (включительно!) не восстанавливаются, вместо них восстанавливаются молекулы воды — выделяется водород.
В случае, если на катод поступают ионы водорода — H + (например при электролизе кислот HCl, H2SO4) восстанавливается водород из молекул кислоты: 2H + — 2e = H2
К аноду притягиваются анионы — отрицательно заряженные ионы: SO4 2- , PO4 3- , Cl — , Br — , I — , F — , S 2- , CH3COO — .

При электролизе кислородсодержащих анионов: SO4 2- , PO4 3- — на аноде окисляются не анионы, а молекулы воды, из которых выделяется кислород.
Бескислородные анионы окисляются и выделяют соответствующие галогены. Сульфид-ион при оксилении окислении серу. Исключением является фтор — если он попадает анод, то разряжается молекула воды и выделяется кислород. Фтор — самый электроотрицательный элемент, поэтому и является исключением.
Анионы органических кислот окисляются особым образом: радикал, примыкающий к карбоксильной группе, удваивается, а сама карбоксильная группа (COO) превращается в углекислый газ — CO2.
Примеры решения
В процессе тренировки вам могут попадаться металлы, которые пропущены в ряду активности. На этапе обучения вы можете пользоваться расширенным рядом активности металлов.
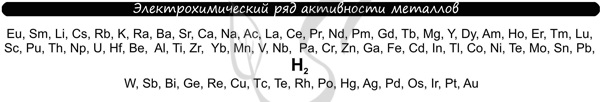
Теперь вы точно будете знать, что выделяется на катоде
Итак, потренируемся. Выясним, что образуется на катоде и аноде при электролизе растворов AgCl, Cu(NO3)2, AlBr3, NaF, FeI2, CH3COOLi.

Иногда в заданиях требуется записать реакцию электролиза. Сообщаю: если вы понимаете, что образуется на катоде, а что на аноде, то написать реакцию не составляет никакого труда. Возьмем, например, электролиз NaCl и запишем реакцию:
NaCl + H2O → H2 + Cl2 + NaOH (обычно в продуктах оставляют именно запись «NaOH», не подвергая его дальнейшему электролизу)
Натрий — активный металл, поэтому на катоде выделяется водород. Анион не содержит кислорода, выделяется галоген — хлор. Мы пишем уравнение, так что не можем заставить натрий испариться бесследно Натрий вступает в реакцию с водой, образуется NaOH.
Запишем реакцию электролиза для CuSO4:
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
Электролиз расплавов
Все, что мы обсуждали до этого момента, касалось электролиза растворов, где растворителем является вода.
Перед промышленной химией стоит важная задача — получить металлы (вещества) в чистом виде. Малоактивные металлы (Ag, Cu) можно легко получать методом электролиза растворов.
Но как быть с активными металлами: Na, K, Li? Ведь при электролизе их растворов они не выделяются на катоде в чистом виде, вместо них восстанавливаются молекулы воды и выделяется водород. Тут нам как раз пригодятся расплавы, которые не содержат воды.
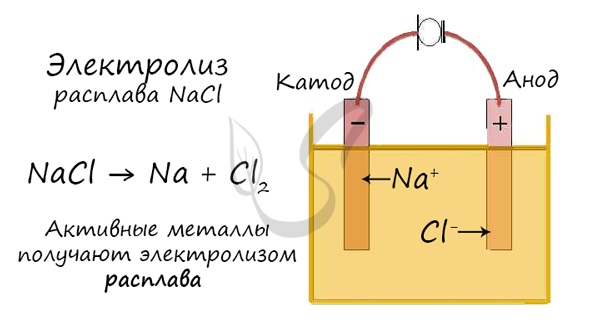
В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Химия, Биология, подготовка к ГИА и ЕГЭ
Электролиз водных растворов солей
Тема электролиза довольна большая, формул в ней много и, как мне кажется, больше ее изучают на уроках физики… Я хочу рассмотреть ту часть, которая касается химии, и при этом только формат ЕГЭ — электролиз водных растворов солей.
Электролиз водных растворов солей
Для начала давайте представим себе систему, в которой происходит электролиз.
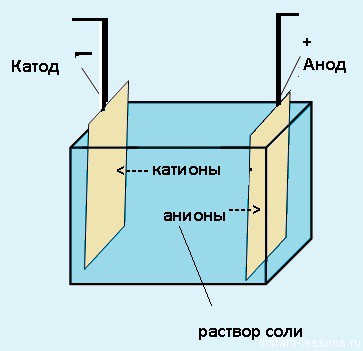
Электролиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других веществ, который возникает при прохождении электрического тока через раствор либо расплав электролита.
Электроды — это такие пластинки или стержни, опущенные в раствор, они подключены к источнику тока.
- Анод — положительно заряженный электрод
- Катод — отрицательно заряженный электрод
Электролиз солей
Самопроизвольные окислительно-восстановительные реакции дают возможность создания гальванических элементов, в которых вырабатывается электрическая энергия. Если же реакция несамопроизвольна, то ее осуществление возможно при помощи электрической энергии. Подобные процессы осуществляют в электролизерах и называются они реакциями электролиза (электролиз солей).
Электролизер
Как видно на рисунке ниже, электролизер состоит из двух электродов, погруженных в расплав или водный раствор соли. Источник электрического тока передает электроны в один из электродов и удаляет их с другого электрода. При отдаче электронов электрод заряжается положительно, а при получении электронов – отрицательно.

Электролиз расплава NaCl
При электролизе расплава NaCl на отрицательном электроде (катоде) происходит присоединение электронов ионом натрия Na + и его восстановление. При этом вблизи электрода концентрация ионов Na + уменьшается и, вследствие этого, к электроду перемещается дополнительное количество ионов Na + .
Аналогично происходит миграция ионов Cl — к положительному электроду, где в результате отдачи электронов протекает процесс окисления. Таким образом, на электродах идет накопление продуктов окисления и восстановления.
Как и в гальваническом элементе, процесс восстановления протекает на катоде, а процесс окисления – на аноде.
При электролизе расплава NaCl протекают следующие реакции:
| Анод | 2Cl — -2e — → Cl2 0 |
| Катод | 2Na + + 2e — → 2Na 0 |
| 2Na + + 2Cl — → 2Na 0 + Cl2 0 |
В промышленности таким образом получают натрий, используя электролизер Даунса, представленный на рисунке ниже.

Сложнее протекает электролиз водных растворов электролитов.
Электролиз водного раствора NaCl
Так, например, при электролизе водного раствора хлорида натрия, происходят иные процессы, нежели при электролизе его расплава. На катоде происходит восстановление воды, а не натрия; на аноде происходит окисление хлорид-ионов:
| Анод | 2Cl — -2e — → Cl2 0 |
| Катод | 2H 2 O + 2e — → H2 0 +2OH — |
| 2H2O + 2Cl — → H2 0 + Cl2 0 |
Таким образом, получить натрий путем электролиза водного раствора его соли не удастся: на катоде выделяется водород, а на аноде хлор.
При электролизе водных растворов солей окислительно-восстановительные процессы, протекающие на катоде и аноде зависят от природы катионов металлов и характера аниона соли.
Процесс на катоде
Предсказать результат восстановительного процесса на катоде можно с помощью таблицы стандартных электродных потенциалов металлов:
- Катионы металлов, имеющие большую величину стандартного потенциала и расположенные в ряду после водорода полностью восстанавливаются на катоде и выделяются в виде металлов: Cu 2+ , Hg2 2+ , Ag + , Hg 2+ , Pt 2+ до Pt 4+
- Катионы металлов, имеющие малую величину стандартного потенциала не восстанавливаются на катоде, вместо этого происходит восстановление воды: от Li + , Na + … до Al 3+ включительно.
- Катионы металлов, имеющие среднюю величину стандартного потенциала будут восстанавливаться на катоде вместе с молекулами воды: от Mn 2+ , Zn 2+ … до H
Если имеется смесь катионов, то легче всего на катоде будут восстанавливаться катионы металла с наиболее положительным потенциалом, например, из смеси Cu 2+ , Ag + , Zn 2+ сначала восстановится Ag + (E = +0,79 В), затем Cu 2+ (E = +0,337 В) и только потом Zn 2+ (E = +0,76 В).
Процесс на аноде
Какие процессы будут протекать на аноде зависит от материала анода и самого электролита. Нерастворимые аноды в процессе электролиза не окисляются, тогда как растворимые аноды разрушаются и в виде ионов переходят в раствор.
Рассмотрим процессы, происходящие на инертном (нерастворимом) аноде:
- При электролизебескислородных кислот и их солей (исключение HF и фториды) на аноде окисляются их анионы.
2Cl — -2e — = Cl2
- При электролизекислородсодержащих кислот и их солей c максимальной степенью окисления на аноде происходит окисление воды, в связи с тем, что потенциал окисления воды меньше, чем для таких анионов.
2H2O -4e — = O2 + 4H +
- При электролизе кислородсодержащих кислот и их солей c промежуточной степенью окисления на аноде происходит окисление анионов кислот
SO3 2- + H2O -2e — = SO4 2- + 2H +
В таблице ниже представлены наиболее типичные случаи электролиза с химической точки зрения
K: Cu 2+ + 2e — = Cu
Т.е. происходит разложение воды
K: Cu 2+ + 2e — = Cu
A: Cu — 2e — = Cu 2+
Электролиз солей — количественные аспекты
Связь между количеством вещества, выделившегося при электролизе соли и количеством прошедшего через него электричества отражена в законах Фарадея.
1 закон Фарадея
Массы веществ (m), выделившихся на катоде или аноде (или образовавшиеся в катодном и анодном пространстве), пропорциональны количеству прошедшего через раствор или расплав электричества (Q):
где k – коэффициент пропорциональности или электрохимический эквивалент, численно равный массе вещества, которое выделяется при прохождении 1 кулона электричества.
2 закон Фарадея
Равные количества электричества в процессе электролиза выделяют эквивалентные количества различных веществ.
Т.е. чтобы выделился один химический эквивалент любого соединения необходимо приложить одинаковое количество электричества, которое равно 96484,56 Кл/моль. Это величина называется постоянной Фарадея.
m – масса вещества,
Э – электрохимический эквивалент,
t – время электролиза.
Законы Фарадея имеют большое значение при проведении расчетов, связанных с электролизом.
Задачи с решениями на составление уравнений электродных реакций, протекающих при электролизе, а также на применение законов Фарадея приведены в разделе Задачи к разделу Электролиз солей
Рубрики
- ОБЩАЯ ХИМИЯ
- Основные понятия и законы химии
- Строение атомов элементов
- Периодический закон Д.И.Менделеева
- Химическая связь и строение молекул
- Основы термодинамики
- Химическая кинетика и равновесие химической реакции
- Растворы
- Окислительно-восстановительные реакции
- Электролиз
- Коррозия металлов
- Комплексные соединения
- Дисперсные системы. Коллоидные растворы
- I группа (щелочные металлы)
- II группа (щелочноземельные металлы)
- III группа (алюминий)
- IV группа (углерод, кремний)
- V группа (азот, фосфор)
- VI группа (кислород, сера)
- VII группа (галогены)
- Краткая история органической химии
- Теория строения А.М. Бутлерова
- Классификация органических соединений
- Изомерия и номенклатура органических соединений
- Типы химических реакций
- Алканы
- Алкены, алкадиены
- Алкины
- Спирты
- Простые эфиры
- Альдегиды, кетоны
- Карбоновые кислоты и сложные эфиры
Источник: zadachi-po-khimii.ru