К 10 мл воды прибавляют 0,5 мл разведенной азотной кислоты, 0,5 мл 2% раствора нитрата серебра. Через 5 минут вода должна оставаться прозрачной.
В присутствии примесей хлоридов выпадает белый творожистый осадок (или белая опалесценция), не растворимый в азотной кислоте и растворимый в растворе гидрооксида аммония.
хлорид ди амина серебра.
К 10 мл воды прибавляют 0,5 мл разведенной хлористоводородной кислоты, 1 мл 5 % раствора бария хлорида. Через 1 0 минут вода должна оставаться прозрачной.
В присутствии примесей сульфатов наблюдают выделение белого кристаллического осадка, который не растворим в растворах минеральных кислот и щелочей.
К 10 мл воды добавляют 1 мл раствора оксалата аммония. Через 10 минут вода должна оставаться прозрачной.
В присутствии солей кальция наблюдают белый осадок, растворимый в азотной и соляной кислотах, но не растворимый в уксусной кислоте и растворе гидроксида аммония.

АЛГОРИТМ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ ВОДЫ ОЧИЩЕННОЙ
1. Работа с рецептом не проводится
2. Письменный контроль
Проверка записей в «Журнале регистрации результатов контроля «Воды очищенной», «Воды для инъекций».
3. Органолептический контроль
Бесцветная прозрачная жидкость без запаха и механических включений.
4.Физический контроль—Не проводится.
По приказу МЗ РФ № 214 от 16.10.97 проводится качественный химический контроль на отсутствие примесей хлоридов, сульфатов, солей кальция.
6.Оформление результатов контроля
Сделать записи в «Журнале регистрации результатов контроля «Воды очищенной», «Воды для инъекций» (наличие и отсутствие ионов отмечается знаком + или -).
7.Контроль при отпуске
Больным не отпускается.
Состоит в проверке правильности оформления баллонов для ассистентской:
проверить этикетку: Aguae purificatae, Дата получения.
— поставить номер анализа и подпись.
ВНУТРИАПТЕЧНЫЙ КОНТРОЛЬ ВОДЫ ДЛЯ ИНЪЕКЦИЙ. AQUA PRO INJECTIONIBUS.
Определение примесей хлоридов, сульфатов и солей кальция см. выше.
4. Восстанавливающие вещества.
100 мл воды доводят до кипения, прибавляют 2 мл разведённой серной к-ты, 1 мл 0,01 моль/л р-ра перманганата калия и кипятят 10 минут. Розовая окраска должна сохраниться. В присутствии примесей восстанавливающих веществ происходит обесцвечивание р-ра.
К 10 мл воды (в пробирке) прибавляют 3 капли реактива Несслера. Через 5 минут вода должна оставаться бесцветной или допускается едва заметное, слегка желтоватое окрашивание.

6. Углерода диоксид
При взбалтывании воды очищенной с равным объемом известковой воды в наполненном доверху и хорошо закрытом сосуде не должно быть помутнения в течение 1 часа.
В присутствие примесей диоксида углерода наблюдают появление белой мути.
Алгоритм внутриаптечного контроля воды для инъекций составьте самостоятельно, аналогично приведенному выше.
ЗАНЯТИЕ 7
АНАЛИЗ РАСТВОРА ПЕРЕКИСИ ВОДОРОДА 3 % — 50 МЛ № 20 ВНУТРИАПТЕЧНАЯ ЗАГОТОВКА
Яр: Solutio Hydrogenii peroxydi 50 ml
№ 20 Внугриаптсчная заготовка
Бесцветная прозрачная жидкость без запаха или со слабым своеобразным запахом, кислой реакции среды.
К 0,5 мл препарата прибавляют 2—3 капли разведенной серной кислоты, 1 2 мл эфира, 3-4 капли раствора калия дихромата и взбалтывают. Эфирный слой окрашивается в синий цвет.

При стоянии синяя окраска переходит в зеленую, вследствие восстановления Cr(VI) в Cr(III).
Помещают 2 мл препарата в мерную колбу емкостью 50 мл и объем доводят водой до метки, перемешивают.
1. Метод перманганатометрии
К 5 мл полученного раствора прибавляют 3 мл разведенной серной кислоты и титруют 0,1 моль/л раствором калия перманганата до слабо-розового окрашивания.
T=Cf •f •M/1000=0,1 •1/2 •34,01/1000=0,001701 г/мл
m= V •K •T •50 •100/2 •5
2. Метод иодометрии
5 мл полученного раствора помещают в склянку с притертой пробкой, прибавляют 2 мл раствора калия иодида, 3 мл разведенной серной кислоты и оставляют в темном месте на 10 минут. Выделившийся иод титруют 0,1 моль/ л раствором натрия тиосульфата до обесцвечивания (индикатор — крахмал).
11мл 0,1 моль/л раствора калия перманганата или натрия тиосульфата соответствует 0,001701 г перекиси водорода, которой в препарате должно быть 2,7 — 3,3 %.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.


Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).
Источник: cyberpedia.su
Нитрат серебра качественное определение
Амидопирин – белые кристаллы или белый кристаллический порошок без запаха, слабогорького вкуса. Температура плавления 110 – 113 ° С. Медленно растворяется в воде, легко – в спирте и в хлороформе.
Водные растворы имеют щелочную реакцию среды. Проявляет свойства восстановителя, с ионами тяжёлых металлов образует устойчивые комплексы.
Методы количественного определения:
2.2 Титрование соляной кислотой . Препарат растворяют в воде, прибавляют 2 капли раствора метилового оранжевого, 1 каплю раствора метиленового синего и титруют 0,1 н. раствором соляной кислоты до появления красно-фиолетовой окраски:
Э= М.м., 1 мл 0,1 н. раствора соляной кислоты соответствует 0,02313 г амидопирина.
Э= М.м. /4, 1 мл 0,1 н. раствора сульфата церия соответствует 0,00587 г амидопирина.
Дибазол – белый или белый со слегка сероватым или желтоватым оттенком кристаллический порошок, горько – соленого вкуса. Гигроскопичен. Температура плавления 182-186 °С. Трудно растворим в воде, легко – в спирте, трудно или практически нерастворим в других органических растворителях.
Проверка подлинности дибазола:
Источник: studyport.ru
Определение хлоридов (определение поправочного коэффициента к титру раствора нитрата серебра)
В коническую колбу вместимостью 250 см 3 вносят пипеткой 10 см 3 раствора хлорида натрия и 90 см 3 дистиллированной воды, добавляют 1 см 3 раствора хромата калия и титруют раствором нитрата серебра до перехода лимонно-желтой окраски в оранжево-желтую, не исчезающую в течение 15 — 20 с.
Полученный результат считают ориентировочным. К оттитрованной пробе прибавляют 1 — 2 капли раствора хлорида натрия до получения желтой окраски. Эта проба является контрольной при повторном, более точном определении. Д
ля этого отбирают новую порцию (10 см 3 ) раствора хлорида натрия и титруют нитратом серебра до получения незначительной разницы оттенков слабо-оранжевого в титруемом растворе и желтого в контрольной пробе.
Поправочный коэффициент вычисляют по формуле:
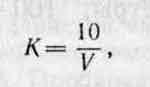
где: V — объем нитрата серебра, пошедший на титрование, см 3 .
Подготовка пробы к анализу
Мутную воду фильтруют через беззольный фильтр, промытый горячей водой. Воду с цветностью свыше 30° обесцвечивают путем добавления суспензии гидроксида алюминия (из расчета 3 см 3 суспензии на 100 см 3 воды), после чего встряхивают до обесцвечивания жидкости. Затем пробу фильтруют через беззольный фильтр. Первые порции фильтрата отбрасывают.
Воду, имеющую щелочную реакцию, нейтрализуют слабым раствором серной кислоты в присутствии фенолфталеина до слабо-розового окрашивания, воду с кислой реакцией — слабым раствором гидрокарбоната натрия, после чего розовую окраску устраняют, взбалтывая воду.
«Руководство к практическим занятиям по методам
санитарно-гигиенических исследований», Л.Г.Подунова
Читайте далее:
- Определение рабочей дозы 1 % хлорной извести (хлорпоглощаемости) в полевых условиях
- Проба на загниваемость
- Определение рабочей дозы 1 % хлорной извести в полевых условиях (пример)
- Проба на стабильность
- Определение рабочей дозы хлора для хлорирования воды (хлорпоглощаемости воды) на водопроводной станции
- Контрольные вопросы и задачи
- Исследование сточных вод
- Коагуляция и хлорирование воды
- Отбор проб
- Коагуляция
- Определение физических свойств
- Коагуляция (оборудование и реактивы)
- Определение физических свойств (ход определения и запах)
- Коагуляция (пример)
- Определение физических свойств (взвешенные вещества)
- Определение активного хлора в хлорной извести
- Определение химического состава (кислотность)
- Определение поправочного коэффициента к титру растворов тиосульфата натрия
Источник: www.meddr.ru