Олово — это лёгкий цветной металл, простое неорганическое вещество. В таблице Менделеева обозначается Sn, stannum (станнум) и числится за номером 50. Между прочим, олово — это один из металлов, которые оказали решающее влияние на развитие цивилизации: Бронзовый век (от 4 до 1 тыс. лет до н.э.) назван так по имени сплава олова с медью.
1. Олово наряду с золотом, серебром, свинцом, медью, ртутью и железом относится к элементам, известным человечеству с глубокой древности. Определить точную дату ознакомления человечества с этим металлом сложно, можно сказать, что сплавы олова с медью — бронзы были известны уже в IV тыс. до н. э., а чистый металл во II тыс. до н. э. Из чистого олова в древности изготовляли посуду и украшения, очень широко применяли изделия из бронзы. Предполагается, что металл был малодоступен и весьма дорог, так как изделия из него редко встречаются среди римских и греческих древностей.
2. Олово в переводе с латинского это значит «прочный, стойкий». Первоначально этим словом называли сплав свинца и серебра, и только значительно позже так стали именовать чистое олово. Слово «олово» имеет славянские корни и обозначает «белый».
223) Антифрикционные металлы олово и свинец (материаловедение)
3. Существует, как минимум, две теории о происхождении русского слова «олово». Согласно первой — индогерманской теории происхождения языков — «олово» и созвучные с ними литовское «alavas», «alvas» и прусское «alwis» (свинец) произошли от латинского «album», фигурирующего в средневековом названии олова Plumbum album. По такому же принципу слово Cuprum производится от Aes cyprium.
По другой версии (более правдоподобной) русское «олово» и польское «olow» (свинец) имеют функциональное происхождение. Дело в том, что славянские народы употребляли хмельной напиток (наподобие пива или браги) из ячменя и жита, этот напиток назывался «оловина» или «ол». Вполне возможно, что оловина хранилась в сосудах из олова.
Либо подобно римлянам, которые выдерживали и хранили вино в сосудах из свинца, славяне держали свой хмельной напиток в свинцовых кувшинах, а ведь в славянских странах свинец называли оловом. Также слово олово можно связать с названием другого жидкого тела — масла (oleum). С лингвистической точки зрения слово «олово» является суффиксальным образованием от корня ol- (ср. древневерхненемецкое elo — «жёлтый», лат. albus — «белый»), получается, что металл назван по цвету. В словаре Срезневского приводятся родственные олову слова — оловце (свинцовая лампада) и оловяник (сосуд из олова).
4. Металл относится к рассеянным элементам, и не самым распространенным на земле (по распространенности в земной коре он занимает 47-ое место). В природе он встречается в виде различных минералов. Самые важные для промышленной добычи: касситерит — оловянный камень, и станнин — оловянный колчедан. Добывают олово из руд, как правило, содержащих не более 0,1 процента этого вещества.
5. При комнатной температуре олово устойчиво к воздействию воздуха или воды (но при температурах выше 150 °C начинается заметное окисление этого металла). При температуре −33 °C, олово трескается и превращается в порошок (в старые времена рассыпание оловянных изделий называли «оловянной чумой»).
Получение свинцово-оловянного сплава
6. Олово плавится при температуре — 231,9 °C. Большая часть выплавляемого олова используется в металлургии для производства различных сплавов. Эти сплавы идут на изготовление подшипников, фольги для упаковки, белой пищевой жести, бронзы, припоев, проводов, литер типографских шрифтов.
7. Олово легко вступает в реакции с неметаллами. Серная и соляная кислота в разбавленном состоянии воздействуют на олово крайне медленно, а в концентрированном виде при нагревании растворяют его. При соединении с соляной кислотой получают хлорид олова, при реакции с серной — сульфат олова. Со щелочами вступает в реакции только при нагревании. С кислородом образует два оксида, со степенью окисления 2 и 4. Является основой целого класса оловоорганических соединений.
8. Треть всех мировых запасов олова приходится на Китай. Китай обладает запасами в 1 500 000 тонн олова, тогда как на все остальные страны приходится 3 330 000 тонн олова. Богатые оловянные месторождения России расположены в Чукотском автономном округе, Якутии, Приморском крае, Хабаровском крае и т.д.
9. Мировое производство олова достигает в настоящий момент около 3,3 млн. тонн в год. Из них более четверти миллиона тонн попадает в атмосферу в виде выхлопных газов!
10. В 1912 году погибла отправившаяся на штурм Южного полюса экспедиция Скотта. Среди снежной пустыни люди остались без горючего, поскольку керосин вытек из разрушившихся по неизвестной причине жестяных баков. Оказалось, что олово паяных швов превратилось в серый порошок — его поразила «оловянная чума».
Полиморфное превращение «белого олова» в «серое» было известно давно — на складах многих армий, бывало, не досчитывались то пуговиц на шинелях, то котелков. Однако далеко не сразу разобрались, что развивается это явление только в условиях низких температур — быстрее всего процесс идет при –33 °C. Причем, если пораженные вещи соседствуют с целыми, происходит заражение «здорового» металла, прямо как при настоящей «человеческой» чуме. «Оловянная чума» погубила многие ценнейшие коллекции оловянных солдатиков. Например, в запасниках питерского музея Александра Суворова превратились в труху десятки фигурок — в подвале, где они хранились, лопнули зимой батареи отопления.
11. Некоторые историки считают, что «оловянная чума» послужила одной из причин поражения армии Наполеона в России, так как превратила пуговицы на одежде французских солдат и пряжки для ремней в порошок, и тем самым оказала на армию деморализующее влияние.
12. Олово считается безопасным для человека, оно есть в нашем организме и каждый день мы получаем его в минимальных количествах (0,2-3,5 мг) с пищей. В теле человека содержится примерно (1-2)•10–4 % олова. Олово представляет опасность для человека, если находится в виде пара или пыли. Токсичная доза олова для человека — 2 г.
13. Многие растения способны аккумулировать олово, содержащееся в почве, воде, в выхлопных газах автомобилей. Так, брусника и черника, собранные в лесу, расположенном даже в 25 км от автострад с большим движением, содержат около 40 мг олова на 1 кг ягод при норме 2 мг/кг.
14. В 1976 году начало работать необычное предприятие, которое сокращенно называют РЭП. Расшифровывается оно так: разведочно-эксплатуционное предприятие. Оно размещается в основном на кораблях. За Полярным кругом, в море Лаптевых, в районе Ванькиной губы РЭП добывает с морского дна оловоносный песок. Здесь же, на борту одного из судов, работает обогатительная фабрика.
15. В жилых помещениях, расположенных ближе, чем за километр от автострады, в воздухе фиксируют избыток олова. Олово создает условия для появления злокачественных опухолей в организме.
16. Одна из основных областей применения олова обусловлена тем, что этот металл является безопасным, нетоксичным, коррозионностойким покрытием, как в чистом виде, так и в сплавах с другими металлами. По этим причинам главное промышленное применение пятидесятого элемента — изготовление белой жести (луженого железа) для производства тары пищевых продуктов, которая используется в консервной промышленности. На эти нужды расходуется порядка 33 % всего добываемого олова. Еще большее количество этого металла (60 %) расходуется в металлургии на создание различных сплавов, важнейший из которых — бронза (сплав олова с медью). Этот сплав один из незаменимых материалов в области машиностроения.
17. Как я уже сказал выше, олово широко используется в металлургии для получения различных сплавов. Оловянные сплавы чаще всего применяют в качестве антифрикционных материалов или припоев. Первые уменьшают трение в машинах и механизмах, вторые соединяют металлические детали.
Из всех антифрикционных сплавов наилучшими свойствами характеризуются оловянные баббиты, содержащие до 90% олова. Главное их применение — изготовление подшипниковых вкладышей. В последнее время стали известны сплавы олова с цирконием, титаном, редкоземельными элементами, отличающиеся повышенной тугоплавкостью и другими ценными свойствами, обеспечивающими их использование в атомной и космической технике.
19. Химические источники тока, в роли анодного материала в которых используют оловянные сплавы (марганцево-оловянный элемент, окисно-ртутно-оловянный элемент), при равном напряжении (со свинцовыми аккумуляторами) обладает в 2,5 раза большей емкостью и в 5 раз большей энергоплотностью на единицу объёма, внутреннее сопротивление его значительно ниже.
20. Олово — это металл Юпитера, который нередко использовался для предсказания будущего. Этот металл сильно связан с достатком и изобилием, с получением каких-то необходимых человеку благ, которые даются человеку за исполнение долга; например, человек может служить обществу или религии. Это металл иерархов, священников и социальных лидеров.
21. Упоминание об олове есть в ранних книгах Ветхого Завета (Четвёртой Книге Моисеевой), об олове в своих трудах говорит и Гомер.
Ещё по теме:
Ваш Промблогер №1 Игорь (ZAVODFOTO)! Подписывайтесь на мой канал, я Вам ещё много чего интересного покажу: https://zen.yandex.ru/zavodfoto
На данный момент я уже лично посетил более 400 предприятий, а вот и ссылки на все мои промрепортажи:
Я всегда рад новым друзьям, добавляйтесь и читайте меня в:
Источник: dzen.ru
Обзор сплавов олова
Олово — это металл, для которого характерны устойчивость к образованию коррозии и экологичность (нетоксичность). Благодаря этим качествам его широко используют в пищевой и электронной промышленности. Довольно часто олово выступает составляющим элементом металлосплавов. Оловянные сплавы по сфере применения классифицируются на подшипниковые, легкоплавкие и припои.
На основе олова производятся баббиты, бронза, припои и пьютеры. Каждый из них имеет свой специфический химический состав, свойства и сферу применения.
Баббиты
- 90% олова и 10% меди — баббиты на основе олова с добавлением меди;
- 89% олова, 7% сурьмы и 4 % меди — оловянный сплав с добавлением сурьмы и меди;
- 80% свинца, 15% сурьмы и 5% олова. — баббиты на основе свинца с добавлением сурьмы и олова.
Легирующими присадками могут выступать в этих сплавах различные металлы.
Баббиты плавятся при температуре от 300 градусов Цельсия. Как уже было отмечено выше, в основе этих материалов лежит олово. Маркируются они как Б88, Б83, Б83С. Данные сплавы применяются в целях повышения вязкости и, напротив, снижения коэффициента трения. Если сравнить эти показатели у оловянного и свинцового баббита, то первый отличается большой стойкостью к появлению коррозии, теплопроводностью и прочностью к различного рода воздействиям.
Сплавы на основе свинца имеют высокие температуры применения (даже выше, чем у оловянных баббитов). Они используются при изготовлении подшипников для двигателей дизельного типа. Также свинцовые баббиты применяют в производстве прокатных станов.
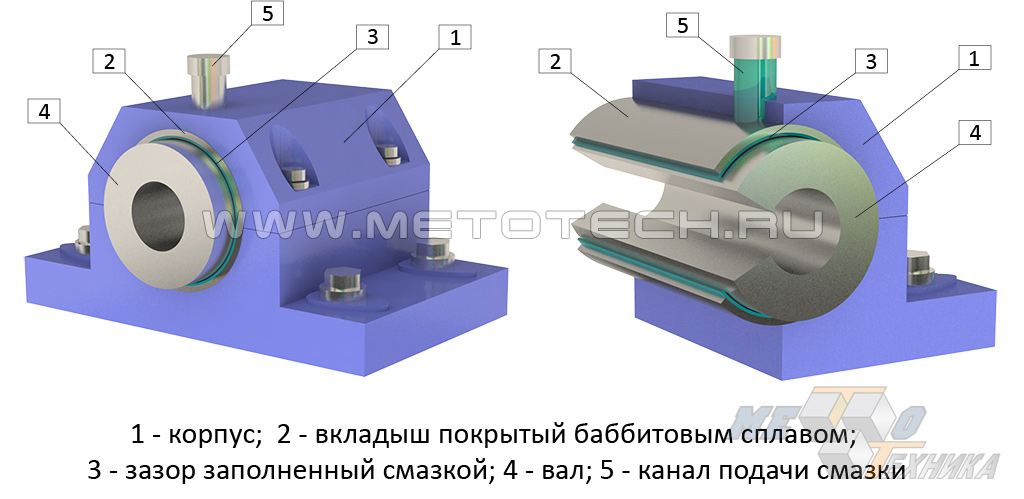
Рисунок 1. Подшипник скольжения
Для всех баббитов характерен такой значительный минус, как малое сопротивление усталости. Незначительная степень прочности этих лигатур позволяет применять их лишь в производстве подшипников, которые, напротив, отличаются износостойким и надежным корпусом, выполненным из стали или бронзы. Долговечность подшипников напрямую зависит от толщины слоя баббитового сплава, залитого на вкладыш из стали. И, соответственно, чем тоньше баббитовый слой, тем меньше срок эксплуатации подшипника.

Рисунок 2. Оловянные баббиты
Бронзы
Другим распространенным видом оловянных сплавов является бронза – оловянно-медный сплав. В принципе, под бронзой подразумевают также и медные сплавы в сочетании с другими элементами. В составе любого типа бронзы содержатся незначительные пропорции различных добавок (цинка, свинца, фосфора и других элементов).
Известную всем бронзу человечество начало изготавливать еще в эпоху Бронзового века. Ее применяли достаточно долгий период времени. Осталась она востребованной и при Железном веке. Она плавится при 930—1140 °C. А плотность бронзы равна 7800-8700 кг/м 3 .
Если изначально в мире была востребована мышьяковая бронза, то с развитием гужевого транспорта и внешней экономики в ряде стран мира начали применять оловянную бронзу. Особенно актуально было использование данного сплава в стремительно развивающейся сфере крупной промышленности. Правда, в последние десятилетия ее начали вытеснять неоловянные сорта бронзы (алюминиевые, медные и др.). Считается, что они превосходят оловянный сплав по своим свойствам.
- Твердость;
- Прочность;
- Легкоплавкость.
Оловянная бронза обладает данными свойствами в большей степени, нежели чистая медь. Данный сплав устойчив к затачиванию и другим видам обработки. Это говорит о том, что он относится к литейным металлам. Усадка у бронзы сравнительно низкая. Она составляет всего 1% (к примеру, у латуни и чугуна она равна 1,5%, у стали – превышает 2%).
Это позволяет применять оловянные бронзы для изготовления отливок.
Их плюсами являются такие качества, как устойчивость к образованию коррозии и отличные антифрикционные свойства. Это объясняет использование данных сплавов в химической промышленности. В частности, их применяют для изготовления литой арматуры. Не менее популярны оловянные бронзы и в других промышленных отраслях.
- Цинк;
- Никель;
- Фосфор;
- Свинец;
- Мышьяк.
- Бр ОФ 6,5-0,15;
- Бр.ОЦ 4-3;
- Бр.ОЦ10-2;
- Бр.ОФ 10-1;
- Бр.ОНС 11-4-3.
Сегодня эти сплавы широко применяются в транспортной промышленности.
Устойчивость оловянных бронз к ржавчине и механическим повреждениям позволяет использовать их в производстве деталей машин. Производимые элементы относятся к расходным материалам, поскольку необходима их регулярная замена.
Бронза отличается долговечностью. Она устойчива к атмосферным осадкам и механическим воздействиям. Изделия, выполняющие декоративную функцию в театрах и дворцах, также производятся из бронз.

Рисунок 3. Изделия из бронзы для нефтегазового оборудования
Пьютер
Пьютером называется сплав олова с такими элементами периодической системы, как медь, сурьма и висмут. Иногда олово смешивают со свинцом. Сплав маркируется символами JJ. Пьютер плавится уже при 170-230 градусах. Следует отметить внешнюю эстетичность данных сплавов. Их легко полировать. Пьютеры необходимы при изготовлении декоративной посуды.
Также сплавы используются в производстве различных украшений. Одним из существенных минусов изделий, изготавливаемых с применением пьютеров, является их низкая устойчивость перед так называемой оловянной чумой. Еще один не менее значимый недостаток данных сплавов – их токсичность. В некоторых странах (к примеру, в Англии) их запретили к использованию. Однако пьютер все же содержится в изделиях, относящихся к антиквариату.
Припои
Легкоплавкие припои используются для монтажа и сборки радиоаппаратуры и различной электроники. Хотя они не такие прочные, как твердые сплавы, однако для данных целей они наиболее приемлемы. Их температура плавления составляет 300-450 градусов Цельсия (иногда меньше).
Сплавы ПОС-40 и ПОС-90 также, как и ПОС-30, полностью расплавляются при 220-265 градусах Цельсия. Однако такую температуру «выдерживают» далеко не все электро- и радиоприборы. Поэтому оптимальным вариантом ля применения являются припои ПОС-61.
Поскольку припои выпускаются в тюбиках, то их состав можно прочитать на самих упаковках. Там бывает четко обозначено процентное соотношение олова и других элементов в данном сплаве.
Существует еще один сорт оловянных припоев. Речь идет о марке ПОССу. Этот сплав содержит в себе олово, свинец и сурьму. Его используют в производстве автотранспорта и холодильников, а также в целях запаивания обмоток машин электрического типа, электроники и кабелей. Содержание сурьмы в таких припоях варьируется от 0,5 % до 2%.
ПОССу плавится при 189 градусах Цельсия.
И, пожалуй, наиболее «оловянным» можно назвать припой марки ПОССу 95-5. Олова и свинца в данном сплаве соответственно 95 к 5 процентам. Он плавится при 234-240 градусах.
Существуют также низкотемпературные припои. Это те сплавы, которые вследствие своей низкой температуры плавления можно без опасений использовать при запайке чувствительных к высоким температурам деталей приборов. Один из таких припоев – ПОСК-50-18. Он расплавляется при 142-145 градусах Цельсия. В данном сплаве олово составляет половину от всего содержимого припоя.
В ПОСК–50-18 также бывает добавлен кадмий, который увеличивает его антикоррозийную устойчивость. Однако этот же легирующий компонент повышает токсичность данного сплава.
Таким образом, олово способно сочетаться в сплавах с другими металлами. Полученные металлопродукты отличаются высокой устойчивостью к появлению коррозии и внешней эстетичностью (яркий металлический блеск). В те или иные оловянные сплавы нередко добавляют легирующие компоненты для улучшения их свойств. Благодаря большому разнообразию соединений такого рода олово нашло применение в ряде отраслей промышленности.
телефоны:
8 (800) 200-52-75
(495) 366-00-24
(495) 504-95-54
(495) 642-41-95
Источник: www.metotech.ru
Олово

Олово — пластичный, ковкий и легкоплавкий блестящий металл серебристо-белого цвета. Используется в основном как безопасное, нетоксичное, коррозионностойкое покрытие в чистом виде или в сплавах с другими металлами. Главные промышленные применения олова – в белой жести (луженое железо) для изготовления тары, в припоях для электроники, в домовых трубопроводах, в подшипниковых сплавах и в покрытиях из олова и его сплавов.Элемент состоит из 10 изотопов с массовыми числами 112, 114-120, 122, 124; последний слабо радиоактивен; изотоп 120 Sn наиболее распространен (около 33%).
- Структура
- Свойства
- Запасы и добыча
- Происхождение
- Применение
- Классификация
- Физические свойства
- Оптические свойства
- Кристаллографические свойства
Смотрите так же:
![]()
СТРУКТУРА
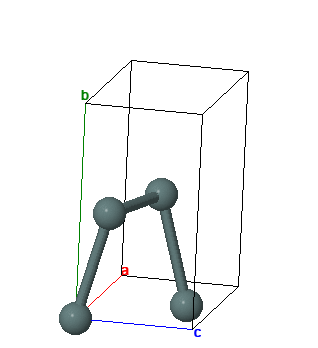
Олово имеет две аллотропные модификации: a-Sn (серое олово) с гранецентрированной кубической кристаллической решеткой и b-Sn (обычное белое олово) с объемноцентрированной тетрагональной кристаллической решеткой. Фазовый переход b -> a ускоряется при низких температурах (-30° С) и в присутствии зародышей кристаллов серого олова; известны случаи, когда оловянные изделия на морозе рассыпались в серый порошок (“оловянная чума”), но это превращение даже при очень низких температурах резко тормозится наличием мельчайших примесей и поэтому редко встречается, представляя скорее научный, чем практический интерес.
СВОЙСТВА

Плотность b-Sn 7,29 г/см 3 , плотность a-Sn 5.85 г/см 3 ,. Температура плавления 231,9°C, температура кипения 2270°C.
Температурный коэффициент линейного расширения 23·10 -6 (0-100 °С); удельная теплоемкость (0°С) 0,225 кдж/(кг·К), то есть 0,0536 кал/(г·°С); теплопроводность (0°С) 65,8 вт/(м·К.), то есть 0,157 кал/(см·сек·°С); удельное электрическое сопротивление (20 °С) 0,115·10 -6 ом·м, то есть 11,5·10 -6 ом·см. Серое олово является диамагнетиком, а белое – парамагнетиком.
Предел прочности при растяжении 16,6 Мн/м 2 (1,7 кгс/мм 2 ); относительное удлинение 80-90%; твердость по Бринеллю 38,3-41,2 Мн/м 2 (3,9-4,2 кгс/мм 2 ). При изгибании прутков олова слышен характерный хруст от взаимного трения кристаллитов.
Чистое олово обладает низкой механической прочностью при комнатной температуре (можно согнуть оловянную палочку, при этом слышится характерный треск, обусловленный трением отдельных кристаллов друг о друга) и поэтому редко используется.
ЗАПАСЫ И ДОБЫЧА
В России запасы оловянных руд расположены в Чукотском автономном округе (Пыркакайские штокверки; рудник/посёлок Валькумей, Иультин — разработка месторождений закрыта в начале 1990-х годов), в Приморском крае (Кавалеровский район), в Хабаровском крае (Солнечный район, Верхнебуреинский район (Правоурмийское месторождение)), в Якутии (месторождение Депутатское) и других районах.
ПРОИСХОЖДЕНИЕ

Основная форма нахождения олова в горных породах и минералах — рассеянная (или эндокриптная). Однако олово образует и минеральные формы, и в этом виде часто встречается не только как акцессорий в кислых магматических породах, но и образует промышленные концентрации преимущественно в окисной (касситерит SnO2) и сульфидной (станнин) формах.
В общем можно выделить следующие формы нахождения олова в природе:
- Рассеянная форма: конкретная форма нахождения олова в этом виде неизвестна. Здесь можно говорить об изоморфно рассеянной форме нахождения олова вследствие наличия изоморфизма с рядом элементов (Ta, Nb, W — с образованием типично кислородных соединений; V, Cr, Ti, Mn, Sc — с образованием кислородных и сульфидных соединений). Если концентрации олова не превышают некоторых критических значений, то оно изоморфно может замещать названные элементы. Механизмы изоморфизма различны.
- Минеральная форма: олово установлено в минералах-концентраторах. Как правило, это минералы, в которых присутствует железо Fe +2 : биотиты, гранаты, пироксены, магнетиты, турмалины и т. д. Эта связь обусловлена изоморфизмом, например, по схеме Sn +4 + Fe +2 → 2Fe +3 . В оловоносных скарнах высокие концентрации олова установлены в гранатах (до 5,8 вес.%) (особенно в андрадитах), эпидотах (до 2,84 вес.%) и т. д.
На сульфидных месторождениях олово входит как изоморфный элемент в сфалериты (Силинское месторождение, Россия, Приморье), халькопириты (Дубровское месторождение, Россия, Приморье), пириты. Высокие концентрации олова выявлены в пирротине грейзенов Смирновского месторождения (Россия, Приморье). Считается, что из-за ограниченного изоморфизма происходит распад твёрдых растворов с микровыделениями Cu2 +1 Fe +2 SnS4 или тиллита PbSnS2 и других минералов.
ПРИМЕНЕНИЕ

Олово используется в основном как безопасное, нетоксичное, коррозионностойкое покрытие в чистом виде или в сплавах с другими металлами. Главные промышленные применения олова — в белой жести (лужёное железо) для изготовления тары пищевых продуктов, в припоях для электроники, в домовых трубопроводах, в подшипниковых сплавах и в покрытиях из олова и его сплавов.
Важнейший сплав олова — бронза (с медью). Другой известный сплав — пьютер — используется для изготовления посуды. Для этих целей расходуется около 33 % всего добываемого олова.
До 60 % производимого олова используется в виде сплавов с медью, медью и цинком, медью и сурьмой (подшипниковый сплав, или баббит), с цинком (упаковочная фольга) и в виде оловянно-свинцовых и оловянно-цинковых припоев. В последнее время возрождается интерес к использованию металла, поскольку он наиболее «экологичен» среди тяжёлых цветных металлов. Используется для создания сверхпроводящих проводов на основе интерметаллического соединения Nb3Sn.
Дисульфид олова SnS2 применяют в составе красок, имитирующих позолоту («поталь»).
Искусственные радиоактивные ядерные изомеры олова 117m Sn и 119m Sn — источники гамма-излучения, являются мёссбауэровскими изотопами и применяются в гамма-резонансной спектроскопии.
Интерметаллические соединения олова и циркония обладают высокими температурами плавления (до 2000 °C) и стойкостью к окислению при нагревании на воздухе и имеют ряд областей применения.
Олово является важнейшим легирующим компонентом при получении конструкционных сплавов титана.
Двуокись олова — очень эффективный абразивный материал, применяемый при «доводке» поверхности оптического стекла.
Смесь солей олова — «жёлтая композиция» — ранее использовалась как краситель для шерсти.
Олово применяется также в химических источниках тока в качестве анодного материала, например: марганцево-оловянный элемент, окисно-ртутно-оловянный элемент. Перспективно использование олова в свинцово-оловянном аккумуляторе; так, например, при равном напряжении, по сравнению со свинцовым аккумулятором свинцово-оловянный аккумулятор обладает в 2,5 раза большей емкостью и в 5 раз большей энергоплотностью на единицу объёма, внутреннее сопротивление его значительно ниже.
Исследуются изолированные двумерные слои олова (станен), созданные по аналогии с графеном.
Олово (англ. Tin) – Sn
| Молекулярный вес | 118.71 г/моль |
| Происхождение названия | от ср. древневерхненемецкого elo — «жёлтый», лат. albus — «белый», так что металл назван по цвету |
| IMA статус | действителен, описан впервые до 1959 (до IMA) |
КЛАССИФИКАЦИЯ
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | оловянный-белый, серо-белый |
| Цвет черты | серо-белый |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | 1.5 – 2 |
| Прочность | ковкий |
| Излом | зазубренный |
| Плотность (измеренная) | 7.31 г/см 3 |
| Радиоактивность (GRapi) | |
| Магнетизм | серое олово – диамагнетик, белое – парамагнетик |
ОПТИЧЕСКИЕ СВОЙСТВА
| Тип | изотропный |
| Анизотропия | умеренная |
| Плеохроизм | не плеохроирует |
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
КРИСТАЛЛОГРАФИЧЕСКИЕ СВОЙСТВА
| Точечная группа | 4/mmm (4/m 2/m 2/m) – дитетрагональная дипирамидальная |
| Пространственная группа | I 41/amd |
| Сингония | тетрагональная |
| Параметры ячейки | a = 5.831Å, b = 5.831Å, c = 3.182Å, α = 90°, β = 90°, γ = 90° |
| Двойникование | общая по (111) |
Источник: mineralpro.ru