Изобретение относится к способам определения физико-химических свойс веществ в водной среде и может быть использовано для анализа растворов при производстве полупроводников, в сборных водах, в технологии получения различных изделий из серебра, его соединений и сплавов. Известен потенциометрический способ непрерывного автоматического к онтроля концентрации различных ионов, в котором использован ионоселективный электрод, содержащий поликристаллическую мембрану на основе халькогенидов и металлический контакт. -Определяемая концентрация находится в интервале 1 моль/л 10 моль/л . Однако известный способ обладает невысокой точностью.
Наиболее близким к изобретению по технической сущности и достигаемому эффекту является способ потенциометрического определения микрограммовых концентраций ионов серебра в воде, заключающийся в измерении потенциала индикаторного электрода из алюмосиликатного стекла в анализируемых и калибровочных растворах 2. Недостатком известного способа является низкая чувствительность стеклянного ионоселективного электрода, с его помощью можно определять концентрацию ионов серебра не менее 1080 мкг/л (5,0 ед. рА). Целью изобретения является расширение диапазона измеряемых концен траций ионов серебра и повышение чувствительности и воспроизводимости определения.
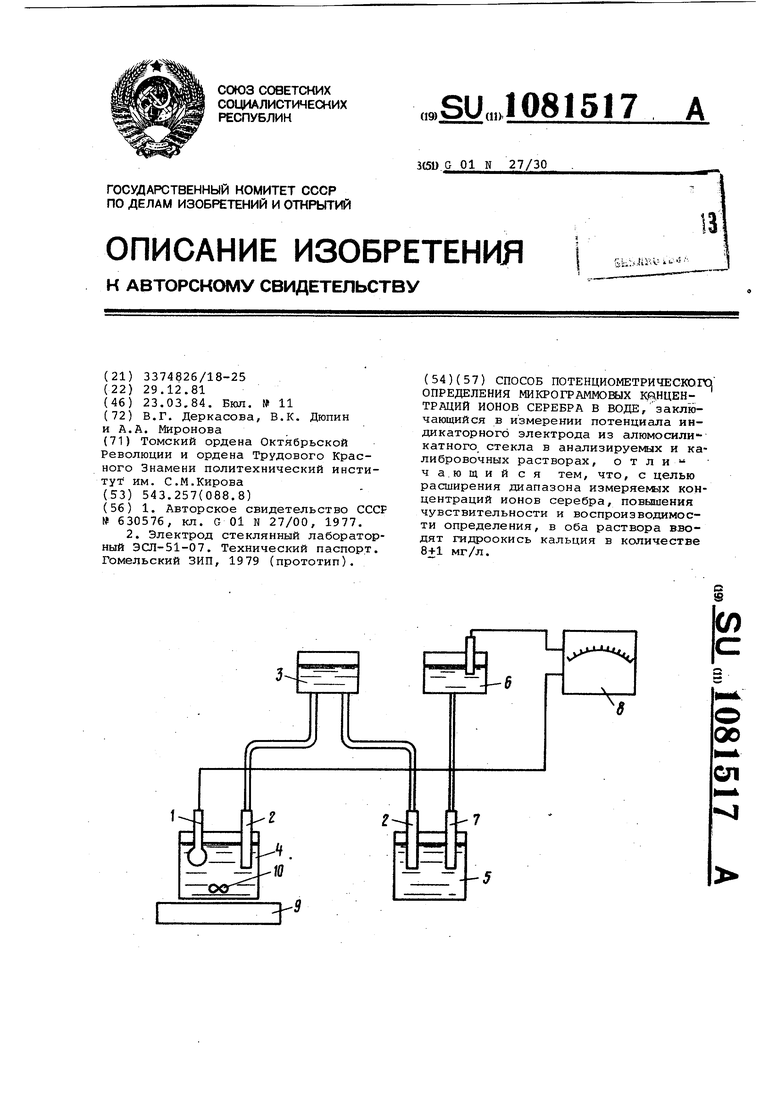
I Поставленная цель достигается тем, что согласно способу потенциометрического определения микрограммовых концентраций ионов серебра в воде, заключающемуся в измерении потенциала индикаторного электрода из алюмосиликатного стекла в анализируе1уых и калибровочных растворах в оба раствора вводят гидроокись кальция в количестве 8±1 мг/л. Определение концентрации ионов серебра проводилось прямым потенцио метрическим способом, в котором использован концентрационный элемент внутренний полуэлемент стеклянного электрода, внутренний раствор стек лянного электрода, мембрана стеклян ного электрода, исследуемый раствор электролитический ключ с 10%-ным Ca(NO3)2, электролитический ключ с насыщенным КС1, электрод сравнения Л, .. На чертеже изображена предлагаемая установка.
Установка содержит стеклянный электрод 1 ЭСЛ-51-07, электрические ключи 2 двойного солевого моста емкость 3,.заполненную 10%-ным раствором Ca(N03l2 / емкость 4, заполненную исследуемым раствором, емкость 5, заполненную 10%-ным раствором CalNOjIj , емкость 6, заполненную насыщенным pacTBOjioM KCl, электролитический ключ 7, заполненный насыщенным раствором КС1, вторичный прибор 8, мешалку 9, магнит 10. Приготавливалась серия калибровочных растворов с заданными значениями концентраций ионов серебра, в каждый из которых вводилось различное количество фонового электролита.
После этого многократно измерялся потенциал электрода на установке с двоичным солевым мостом. Полученные данные обрабатывались математически. Для доказательства существенности предлагаемых в изобретении признаков в качестве фонового электролита применялись растворы гидроокисей натрия, калия, бария и кальция.
Исходным для приготовления калибровочных растворов является раствор азотнокислого серебра с концентрацией 1000 мкг/л, который приготавливался из 0,001 н. раствора В свою очередь, 0,001 н раствор приготавливался из навески Ao-ftoj с последующим титриметрическим (по методу Мора ) определением концентрации ионов серебра. Калибровочные растворы и растворы гидрооки-сей готовились с применением дистиллированной воды, из которой предварительно был удален COg Удаление СО производилось длительнь1М (2-3 ч) кипячением дистиллированной воды с последующим охлаждением воды в емкостях, закрытых стеклянными трубками, заполненными аскаритом.
Насыщенные растворы Са(ОН Ij и Ва(ОН)2 приготавливались.растворением 2 г/л Са (он )2 или Ва(ОН)2В дистиллированной воде без СО2 с последующей выдержкой Са(ОН осадком в течение 1 сут., после чего раствор отфильтровывался. После приготовления серии калибровочных растворов с добавкой растворов гидроокисей натрия, калия, бария и кальция производилась градуировка электрода ЭСЛ-51-07 на предлагаемой установке. Для этого последовательно каждым из калибровочных растворов заполнялась емкость 4, электрод выдерживался в данном растворе 2 мин (показания вторичного прибора при этом не записывсшись, раствор выливалсяJ. Затем снова этим же раствором заполнялась емкость 4, после чего записывались показания электрода через 2 мин и 5 мин с момента второго заполнения. По такой же методике производилось измерение потенциала элек трода в каждом из последующих растворов, причем измерения осуществлялись
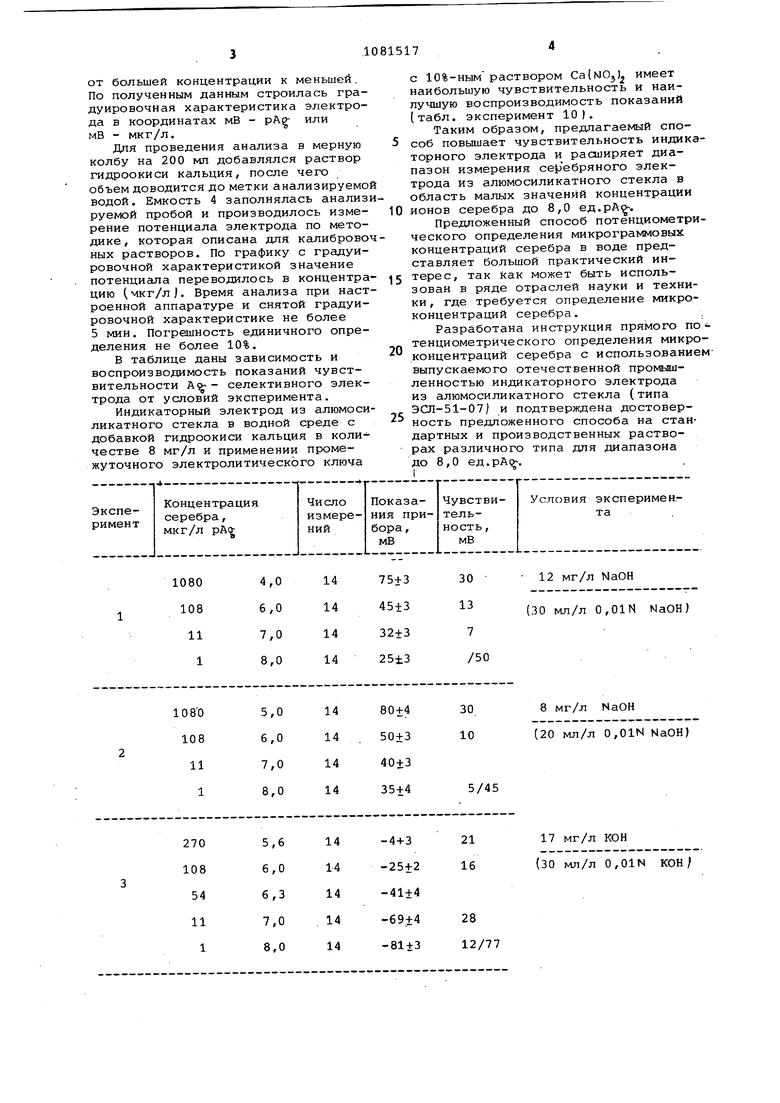
от большей концентрации к меньшей. По полученным данным строилась градуировочная характеристика электрода в координатах мВ — pAg; или мВ — мкг/л.
Для проведения анализа в мерную колбу на 200 мп добавлялся раствор гидроокиси кальция, после чего объем доводится до метки анализируемо водой. Емкость 4 заполнялась анализруемой пробой и производилось измерение потенциала электрода по методике, которая описана для калибровоных растворов. По графику с гращуировочной характеристикой значение потенциала переводилось в концентрацию (мкг/л I. Время анализа при настроенной аппаратуре и снятой градуировочной характеристике не более 5 мин. Погрешность единичного определения не более 10%.
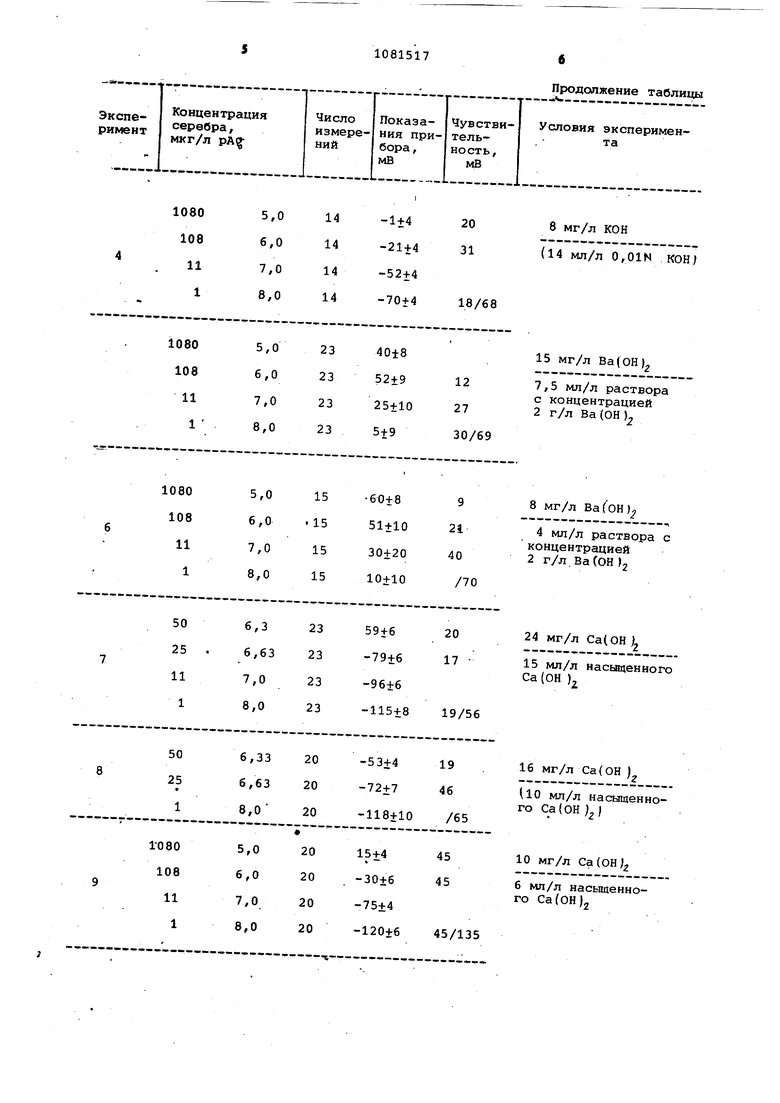
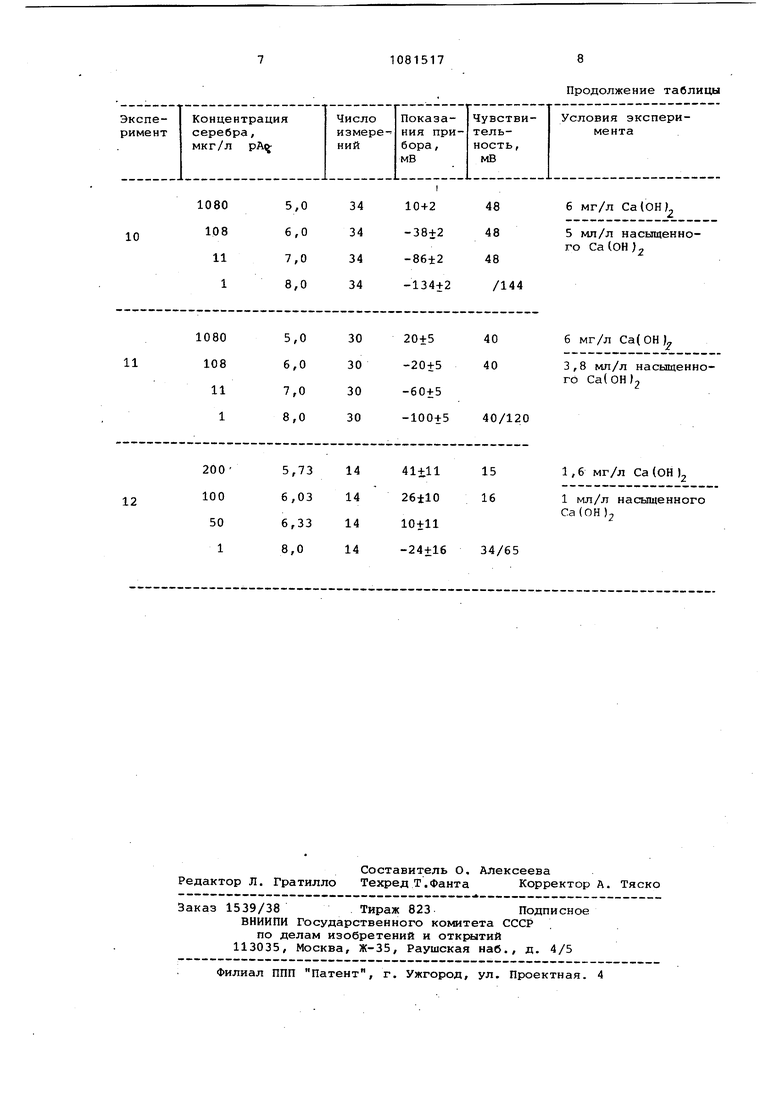
В таблице даны зависимость и воспроизводимость показаний чувствительности А — селективного электрода от условий эксперимента.
Индикаторный электрод из алюмосиликатного стекла в водной среде с добавкой гидроокиси кальция в количестве 8 мг/л и применении промежуточного электролитического ключа
с 1C%-ным раствором Ca(NOj) имеет наибольшую чувствительность и наилучшую воспроизводимость показаний (табл. эксперимент 10).
Таким образом, предлагаемый способ повышает чувствительность индикаторного электрода и расширяет диапазон измерения се| ебряного электрода из алюмосиликатного стекла в область малых значений концентрации 0 ионов серебра до 8,0 ед.рА.
Предложенный способ потенциометрического определения микрограммовых концентраций серебра в воде представляет большой практический интерес, так как может быть исполь5зован в ряде отраслей науки и техники, где требуется определение микроконцентраций серебра.
Разработана инструкция прямого потенциометрического определения микро0концентраций серебра с использованиемвыпускаемого отечественной промышленностью индикаторного электрода из алюмосиликатного стекла (типа ЭСЛ-51-07) и подтверждена достоверность предложенного способа на стандартных и производственных растворах различного типа для диапазона до 8,0 ед.рА(.
Похожие патенты SU1081517A1
- Деркасова Валентина Георгиевна
- Деркасова Валентина Георгиевна
- Деркасова Валентина Георгиевна
- Григорова Лариса Ивановна
- Квадяева Галина Ивановна
- Карелин Владимир Александрович
- Деркасова Валентина Георгиевна
- Мовчан Н.И.
- Умарова Н.Н.
- Юсупов Р.А.
- Сопин В.Ф.
- Зинкичева Т.Т.
- Коноплев Юрий Иванович
- Кораблев Игорь Васильевич
- Морозов Алексей Валерьевич
- Гальцова Галина Анатольевна
- Айдиев Айди Ясупиевич
- Евглевский Дмитрий Анатольевич
- Левашова Оксана Васильевна
- Смирнов Игорь Иванович
- Кулешова Елена Анатольевна
- Денисова Ариадна Захаровна
- Калецкая Галина Николаевна
- Корзун Анатолий Григорьевич
- Чеботарев Виктор Константинович
- Терентьев Роман Александрович
- Пасека Александра Евгеньевна
- Чеботарев Виктор Константинович
- Терентьев Роман Александрович
- Пасека Александра Евгеньевна
Реферат патента 1984 года Способ потенциометрического определения микрограммовых концентраций ионов серебра в воде
СПОСОБ ПОТЕНЦИОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ МИКРОГРАММОВЫХ КОНЦЕНТРАЦИЙ ИОНОВ СЕРЕБРА В ВОДЕ,заключающийся в измерении потенциала индикаторного электрода из алюмосиликатного стекла в анализируемых и калибровочных растворах, о т л и ча.ющийся тем, что, с целью расширения диапазона измеряемых концентраций ионов серебра, повышения чувствительности и воспроизводимости определения, в оба раствора вводят гидроокись кальция в количестве 8+1 мг/л. 00 ел
Источник: patenton.ru
ГОСТ 23268.13-78
Воды минеральные питьевые лечебные, лечебно-столовые и природные столовые. Метод определения ионов серебра
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО «ЦНТИ Нормоконтроль»
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на лечебные, лечебно-столовые и природные столовые питьевые минеральные воды и устанавливает метод определения ионов серебра колориметрическим титрованием
Ограничение срока действия снято: Протокол № 4-93 МГС от 21.10.93 (ИУС 4-94)
Оглавление
2 Аппаратура, реактивы и материалы
3 Подготовка к анализу
4 Проведение анализа
5 Обработка результатов
| 01.01.1980 |
| 01.09.2013 |
| 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 67 ПРОИЗВОДСТВО ПИЩЕВЫХ ПРОДУКТОВ
- Раздел 67.160 Напитки
- Раздел 67.160.20 Безалкогольные напитки
- Раздел Электроэнергия
- Раздел 67 ПРОИЗВОДСТВО ПИЩЕВЫХ ПРОДУКТОВ
- Раздел 67.160 Напитки
- Раздел 67.160.20 Безалкогольные напитки
Организации:
| Утвержден | Госстандарт СССР | 2411 |
Drinking medicinal, medicinal-table and natural table mineral water. Method of determination of silver ions
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:
- Сканы страниц ГОСТа
- Текст ГОСТа
УДК 663.64:542.3:006.354 Группа PH
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
ВОДЫ МИНЕРАЛЬНЫЕ ПИТЬЕВЫЕ ЛЕЧЕБНЫЕ, ЛЕЧЕБНО-СТОЛОВЫЕ И ПРИРОДНЫЕ СТОЛОВЫЕ
Метод определения ионов серебра
Drinking medicinal, medicinal-table and natural-table mineral waters. Method of determination of silver ions
Постановлением Государственного комитета СССР по стандартам от 1 сентября 1978 г. № 2411 срок действия установлен
с 01.01.80 до 01.6165
Несоблюдение стандарта преследуется по закону
Настоящий стандарт распространяется на лечебные, лечебно-столовые и природные столовые питьевые минеральные воды и устанавливает метод определения ионов серебра колориметрическим титрованием.
Метод основан на образовании в кислой среде окрашенного в желтый цвет дитизоната серебра.
Метод позволяет определять от Ы0~ 4 мг ионов серебра в пробе.
1.2. Объем пробы воды для определения серебра — не менее 150 см 3 .
2. АППАРАТУРА, РЕАКТИВЫ И МАТЕРИАЛЫ
Посуда мерная стеклянная лабораторная по ГОСТ 1770-74, вместимостью: колбы 100, 500, 1000 см 3 ; цилиндры 50 и 100 см 3 .
Колбы стеклянные лабораторные конические по ГОСТ
25336—82, вместимостью 100 и 150 см 3 .
Приборы мерные лабораторные стеклянные по ГОСТ
20292—74, вместимостью: бюретки 5 см 3 , пипетки 2, 5, 10, 50 см 3 .
Издание официальное Перепечатка воспрещена
Переиздание. Сентябрь 1983 г.
Воронки делительные вместимостью 150, 200, 500 см 3 .
Весы лабораторные аналитические.
Весы технические типа В Л Т-200.
Плитка электрическая по ГОСТ 306-76.
Серебро азотнокислое по ГОСТ 1277-75.
Метиловый оранжевый по ГОСТ 10816-64.
Аммоний хлористый по ГОСТ 3773-72.
Углерод четыреххлористый по ГОСТ 20288-74.
Кислота соляная фиксанал, 0,1 н. раствор.
Кислота азотная по ГОСТ 4461 -77.
Соль динатриевая этилендиамин-N, N, М’М’-тетрауксусной кислоты, 2-водная (трилон Б) по ГОСТ 10652-73.
Вода дистиллированная по ГОСТ 6709-72.
Гидроксиламин сернокислый по ГОСТ 7298-79.
Бумага фильтровальная лабораторная по ГОСТ 12026-76.
Все реактивы должны быть квалификации х.ч. или ч.д.а.
3. ПОДГОТОВКА К АНАЛИЗУ
3.1. Приготовление основного стандартного раствора азотнокислого серебра
0,1573 г азотнокислого серебра взвешивают с погрешностью не более ±0,0002 г, помещают в мерную колбу вместимостью 100 см 3 , растворяют в небольшом количестве дистиллированной воды, добавляют 3 капли концентрированной азотной кислоты и доводят объем раствора дистиллированной водой до метки. 1 см 3 раствора содержит 0,1 мг ионов серебра.
3.2. Приготовление рабочего стандартного раствора азотнокислого серебра
10 см 3 основного стандартного раствора азотнокислого серебра помещают в мерную колбу вместимостью 1000 см 3 , объем раствора доводят дистиллированной водой до метки. Для анализа следует использовать свежеприготовленный раствор.
1 см 3 раствора содержит 0,001 мг ионов серебра-
3.3. Приготовление раствора аммиака
1,5 см 3 раствора аммиака плотностью 0,95 г/см 3 помещают в мерную колбу вместимостью 1000 см 3 и доводят объем раствора дистиллированной водой до метки.
3.4. Приготовление 30%-ного раствора хлористого аммония
30 г хлористого аммония взвешивают с погрешностью не более ±0,01| г и растворяют в 70 см 3 дистиллированной воды.
3.5. Приготовление 10% -н о г о раствора трило-н а Б
10 г трилона Б взвешивают с погрешностью не более ±0,01 г и растворяют в 90 см* дистиллированной воды.
3.6. Приготовление 1%-ного раствора сернокислого гидроксил амина
1 г сернокислого гидроксиламина взвешивают с погрешностью не более ±0,01 г и растворяют в 99 см 3 дистиллированной воды.
3.7. Приготовление 1 н. раствора соляной кислоты
Раствор готовят из фиксанала. Содержимое ампулы для приготовления 0,1 н. раствора соляной кислоты количественно переносят в мерную колбу вместимостью 100 см 3 и доводят объем раствора дистиллированной водой до метки.
3.8. Приготовление основного стандартного раствора дитизона
Дитизон предварительно очищают от содержащихся в нем примесей, используя способность дитизона растворяться в щелочных водных растворах. Продукты окисления при разделении •остаются в слое органического растворителя.
0,17 г дитизона, предназначенного для очистки, взвешивают с погрешностью не более ±0,001 г, помещают в делительную воронку вместимостью 500 см 3 , растворяют в 100 см 3 четыреххлористого углерода, добавляют 100 см 3 водного раствора аммиака и встряхивают несколько раз. Нижний слой, представляющий собой раствор неочищенного дитизона в четыреххлористом углероде, сливают в другую воронку и снова экстрагируют, добавив 50 см 3 водного раствора аммиака. Экстракцию повторяют до тех пор, пока верхний водноаммиачный слой не перестанет окрашиваться в оранжево-желтый цвет. Водно-аммиачные экстракты оранжево-желтого цвета, содержащие аммиачные соли дитизона, фильтруют через вату, собирают в делительную воронку, нейтрализуют концентрированной соляной кислотой до перехода цвета раствора в бледно-зеленый и выпадения темных хлопьев. Добавляют еще 2 капли соляной кислоты и экстрагируют 3—4 раза четыреххлористым углеродом порциями по 50 см 3 .
Нижний слой зеленого цвета, представляющий раствор дитизона в четыреххлористом углероде, сливают через бумажный фитьтр в склянку из темного стекла. Общий объем раствора дитизона доводят четыреххлористым углеродом до 300 см 3 .
3.9. Приготовление рабочего стандартного раствора дитизона
10 см 3 основного стандартного раствора дитизона помещают в мерную колбу вместимостью 250 см 3 и объем раствора доводят четыреххлористым углеродом до метки.
3.10. Приготовление 0,1%-ного раствора индикатора метилового оранжевого
0,1 г метилового оранжевого взвешивают с погрешностью не более ±0,01- г, растворяют в небольшом объеме дистиллированной воды и объем раствора доводят дистиллированной водой до-100 см 3 .
4. ПРОВЕДЕНИЕ АНАЛИЗА
4.1. В колбу вместимостью 100—150 см 3 вносят 50 см 3 анализируемой воды. Присутствующие гидрокарбонат-ионы в пробе нейтрализуют 1 н. раствором соляной кислоты, количество которой определяют титрованием отдельной пробы, используя в качестве индикатора метиловый оранжевый. Для перевода нерастворимых галогенидов серебра в растворимые комплексные соединения добавляют 7 см 3 30 %-ного раствора хлористого аммония. Содержимое колбы кипятят, быстро охлаждают до 20°С и переносят в делительную воронку вместимостью 150—200 см 3 . Для маскировки катионов приливают 2 см 3 10’%-ного раствора трияона Б. Влияние окислителей устраняют добавлением, 2 см 3
1 % -ного раствора сернокислого гидроксиламина. Вносят 2 см 3 рабочего стандартного раствора дитизона. Пробу встряхивают в течение 5 мин. Если слой дитизона после встряхивания окрашивается В’ желтый или оранжевый цвет, добавляют следующую порцию дитизона и снова встряхивают.
Операцию повторяют до тех пор, пока слой дитизона в воронке не примет желто-зеленый цвет.
Параллельно те же операции проводят с контрольной пробой дистиллированной воды, не содержащей серебра. Контрольную-пробу титруют рабочим стандартным раствором азотнокислого серебра до выравнивания интенсивности цвета в анализируемой и контрольной пробах.
5. ОБРАБОТКА РЕЗУЛЬТАТОВ
5.1. Массовую концентрацию ионов серебра (X), мг/дм 3 , вычисляют по формуле
где Vt — объем рабочего стандартного раствора азотнокислого серебра, израсходованный на титрование, см 3 ;
0,001 — масса серебра в 1 см 3 рабочего стандартного раствора, мг;
Vi — объем воды, взятый на анализ, см 3 .
За окончательный результат принимают среднее арифметическое двух параллельных определений, допускаемые расхождения между которыми не должны превышать 2%.
Источник: standartgost.ru
ГОСТ 4245-72 Вода питьевая. Методы определения содержания хлоридов

Настоящий стандарт распространяется на питьевую воду и устанавливает методы определения содержания хлоридов (хлор-иона).
Определение содержания хлор-иона в питьевой воде производят:
при содержании хлор-иона от 10 мг/дм 3 и выше титрованием азотнокислым серебром в присутствии хромовокислого калия в качестве индикатора;
при содержании хлор-иона до 10 мг/дм 3 титрованием азотнокислой ртутью в присутствии индикатора дифенилкарбазона.
1. МЕТОДЫ ОТБОРА ПРОБ
1.1. Отбор проб производят по ГОСТ 2874 и ГОСТ 4979.
1.2. Объем пробы воды для определения содержания хлоридов должен быть не менее 250 см 3 .
1.3. Пробы воды, предназначенные для определения хлоридов, не консервируют.
2. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ХЛОР-ИОНА ТИТРОВАНИЕМ АЗОТНОКИСЛЫМ СЕРЕБРОМ
2.1. Сущность метода
Метод основан на осаждении хлор-иона в нейтральной или слабощелочной среде азотнокислым серебром в присутствии хромовокислого калия в качестве индикатора. После осаждения хлорида серебра в точке эквивалентности образуется хромовокислое серебро, при этом желтая окраска раствора переходит в оранжево-желтую. Точность метода 1-3 мг/дм 3 .
2.2 Аппаратура, материалы и реактивы
Посуда мерная стеклянная лабораторная по ГОСТ 1770, ГОСТ 29227, ГОСТ 29251, вместимостью: пипетки 100, 50 и 10 см 3 без делений; пипетка 1 см 3 с делением через 0,01 см 3 ; цилиндр мерный 100 см 3 ; бюретка 25 см 3 со стеклянным краном.
Колбы конические по ГОСТ 25336, вместимостью 250 см 3 .
Капельница по ГОСТ 25336.
Пробирки колориметрические с отметкой на 5 см 3 .
Воронки стеклянные по ГОСТ 25336.
Фильтры беззольные «белая лента».
Серебро азотнокислое по ГОСТ 1277.
Натрий хлористый по ГОСТ 4233.
Квасцы алюмокалиевые (алюминий-калий сернокислый) по ГОСТ 4329.
Калий хромовокислый по ГОСТ 4459.
Аммиак водный по ГОСТ 3760, 25 %-ный раствор.
Вода дистиллированная по ГОСТ 6709.
Все реактивы, используемые для анализа, должны быть квалификации чистые для анализа (ч. д. а.).
2.3. Подготовка к анализу
2.3.1. Приготовление титрованного раствора азотнокислого серебра.
2,40 г химически чистого AgNO 3 растворяют в дистиллированной воде и доводят объем раствора дистиллированной водой до 1 дм 3 .
1 см 3 раствора эквивалентен 0,5 мг С l — .
Раствор хранят в склянке из темного стекла.
2.3.2. Приготовление 10%-ного раствора (подкисленного азотной кислотой) азотнокислого серебра
10 г AgNO 3 растворяют в 90 см 3 дистиллированной воды и добавляют 1-2 капли HNO 3 .
2.3.3. Приготовление титрованного раствора хлористого натрия
0,8245 г химически чистого NaCl , высушенного при 105 °С, растворяют в дистиллированной воде и доводят объем раствора дистиллированной водой до 1 дм 3 .
1 см 3 раствора содержит 0,5 мг С l — .
2.3.4. Приготовление гидроокиси алюминия
125 г алюмокалиевых квасцов [ AlK ( SO 4 )2 × 12H2O] растворяют в 1 дм 3 дистиллированной воды, нагревают до 60 °С и постепенно прибавляют 55 см 3 концентрированного раствора аммиака при постоянном перемешивании. После отстаивания в течение 1 ч осадок переносят в большой стакан и промывают декантацией дистиллированной водой до исчезновения реакции на хлориды.
2.3.5. Приготовление 5 %-ного раствора хромовокислого калия
50 г К2С r О4 растворяют в небольшом объеме дистиллированной воды и доводят объем раствора дистиллированной водой до 1 дм 3 .
2.3.6. Установка поправочного коэффициента к раствору азотнокислого серебра.
В коническую колбу вносят пипеткой 10 см 3 раствора хлористого натрия и 90 см 3 дистиллированной воды, добавляют 1 см 3 раствора хромовокислого калия и титруют раствором азотнокислого серебра до перехода лимонно-желтой окраски мутного раствора в оранжево-желтую, не исчезающую в течение 15-20 с. Полученный результат считают ориентировочным. К оттитрованной пробе прибавляют 1-2 капли раствора хлористого натрия до получения желтой окраски. Эта проба является контрольной при повторном, более точном определении. Для этого отбирают новую порцию раствора хлористого натрия и титруют азотнокислым серебром до получения незначительной разницы оттенков слабо-оранжевого в титруемом растворе и желтого в контрольной пробе. Поправочный коэффициент (К) вычисляют по формуле
где v — количество азотнокислого серебра, израсходованное на титрование, см 3 .
2.4. Проведение анализа
2.4.1. Качественное определение
Характеристика осадка или мути
1. Опалесценция или слабая муть
3. Образуются хлопья, осаждаются не сразу
4. Белый объемный осадок
2.4.2. Количественное определение
В зависимости от результатов качественного определения отбирают 100 см 3 испытуемой воды или меньший ее объем (10-50 см 3 ) и доводят до 100 см 3 дистиллированной водой. Без разбавления определяются хлориды в концентрации до 100 мг/дм 3 . p Н титруемой пробы должен быть в пределах 6-10. Если вода мутная, ее фильтруют через беззольный фильтр, промытый горячей водой.
Если вода имеет цветность выше 30°, пробу обесцвечивают добавлением гидроокиси алюминия. Для этого к 200 см 3 пробы добавляют 6 см 3 суспензии гидроокиси алюминия, а смесь встряхивают до обесцвечивания жидкости. Затем пробу фильтруют через беззольный фильтр. Первые порции фильтрата отбрасывают.
Отмеренный объем воды вносят в две конические колбы и прибавляют по 1 см 3 раствора хромовокислого калия. Одну пробу титруют раствором азотнокислого серебра до появления слабого оранжевого оттенка, вторую пробу используют в качестве контрольной пробы. При значительном содержании хлоридов образуется осадок AgCl , мешающий определению. В этом случае к оттитрованной первой пробе приливают 2-3 капли титрованного раствора NaCl до исчезновения оранжевого оттенка, затем титруют вторую пробу, пользуясь первой, как контрольной пробой.
Определению мешают: ортофосфаты в концентрации, превышающей 25 мг/дм 3 ; железо в концентрации более 10 мг/дм 3 . Бромиды и йодиды определяются в концентрациях, эквивалентных С l — . При обычном содержании в водопроводной воде они не мешают определению.
2.5. Обработка результатов.
Содержание хлор-иона (X), мг/дм 3 , вычисляют по формуле
где v — количество азотнокислого серебра, израсходованное на титрование, см 3 ;
К — поправочный коэффициент к титру раствора нитрата серебра;
g — количество хлор-иона, соответствующее 1 см 3 раствора азотнокислого серебра, мг;
V — объем пробы, взятый для определения, см 3 .
Расхождения между результатами повторных определений при содержании С l — от 20 до 200 мг/дм 3 — 2 мг/дм 3 ; при более высоком содержании — 2 отн. %.
3. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ХЛОР-ИОНА В ВОДЕ ТИТРОВАНИЕМ АЗОТНОКИСЛОЙ РТУТЬЮ В ПРИСУТСТВИИ ИНДИКАТОРА ДИФЕНИЛКАРВАЗОНА
3.1. Сущность метода
Хлориды титруют в кислой среде раствором азотнокислой ртути в присутствии дифенилкарбазона, при этом образуется растворимая, почти диссоциирующая хлорная ртуть. В конце титрования избыточные ионы ртути с дифенилкарбазоном образуют окрашенное в фиолетовый цвет комплексное соединение. Изменение окраски в эквивалентной точке выражено четко, в связи с этим конец титрования определяется с большой точностью.
Точность метода 0,5 мг/дм 3 .
3.2. Аппаратура, материалы и реактивы.
Посуда мерная стеклянная лабораторная по ГОСТ 1770, ГОСТ 29227, ГОСТ 29251, вместимостью: пипетки 100 и 50 см 3 без делений, цилиндр мерный 100 см 3 микробюретка 2 см 3 .
Колбы конические по ГОСТ 25336, вместимостью 250 см 3 .
Капельница по ГОСТ 25336.
Ртуть азотнокислая окисная по ГОСТ 4520.
Натрий хлористый по ГОСТ 4233.
Кислота азотная по ГОСТ 4461.
Спирт этиловый ректификованный по ГОСТ 5962.
Бромфеноловый синий (индикатор).
Все реактивы, используемые для анализа, должны быть квалификации чистые для анализа (ч. д. а.).
3.3. Подготовка к анализу
3.3.1. Приготовление 0,0141 н. раствора азотнокислой ртути
2,42 г Hg ( N О3)2 × 1 /2Н2 O растворяют в 20 см 3 дистиллированной воды к которой прибавлено 0,25 см 3 концентрированной азотной кислоты, затем объем раствора доводят дистиллированной водой до 1 дм 3 .
1 см 3 этого раствора эквивалентен 0,5 мг С l — .
Раствор устойчив в течение четырех месяцев.
Поправочный коэффициент к титру раствора азотнокислой ртути определяют титрованием 5 см 3 хлористого натрия (1 см 3 — 0,5 мг С l — ), разбавленного до 100 см 3 дистиллированной водой, в тех же условиях, как при анализе пробы воды.
3.3.2. Приготовление дифенилкарбазона, спиртового раствора смешанного индикатора
0,5 г дифенилкарбазона и 0,05 г бромфенолового синего растворяют в 100 см 3 95 %-ного этилового спирта. Хранят в склянке из темного стекла.
3.3.3. Приготовление 0,2 н. раствора азотной кислоты
12.8 мл концентрированной азотной кислоты разводят дистиллированной водой до 1 дм 3
Все растворы готовят на дважды перегнанной дистиллированной воде.
3.4. Проведение анализа
Отбирают 100 см 3 испытуемой воды, прибавляют 10 капель смешанного индикатора и по каплям 0,2 н. раствор HNO 3 до появления желтой окраски (рН 3,6), после чего прибавляют еще пять капель 0,2 н. раствора HNO 3 и титруют из микробюретки раствором азотнокислой ртути. К концу титрования окраска раствора приобретает оранжевый оттенок. Титрование продолжают медленно, по каплям добавляя раствор азотнокислой ртути, сильно взбалтывая пробу до появления слабо-фиолетового оттенка.
Для определения более четкого конца титрования используют контрольную пробу, в которой к 100 см 3 дистиллированной воды прибавляют индикатор, 0,2 н. раствор азотной кислоты и одну каплю раствора азотнокислой ртути.
Определению не мешают цветность воды выше 30° и железо в концентрации, превышающей 10 мг/дм 3 . Йодиды и бромиды определяют в концентрациях, эквивалентных С l — .
3.5. Обработка результатов
Содержание хлор-иона (X) в мг/дм 3 вычисляют по формуле
где v — количество азотнокислой ртути, израсходованное на титрование, см 3 ;
К — поправочный коэффициент к титру раствора азотнокислой ртути;
V — объем воды, взятый для определения, см 3 .
Расхождения между результатами повторных определений при содержании С l — в воде до 10 мг/дм 3 — 0,5 мг/дм 3 .
ИНФОРМАЦИОННЫЕ ДАННЫЕ
1. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР
2. ВЗАМЕН ГОСТ 4245-48
3. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка
Источник: znaytovar.ru