Основной компонент мела мрамора известняка это
Мел, мрамор и известняк с химической точки зрения одно и то же вещество — карбонат кальция, а точнее, одна из его кристаллических модификаций — кальцит.
Мел — это мягкая горная порода, которую легко истереть в порошок. Мел используется в качестве белого пигмента в лакокрасочной и резиновой промышленности, в производстве портландцемента, как пишущий материал.
Известняк обладает большей твёрдостью: издавна его использовали как материал для каменных сооружений. Большинство храмов великокняжеской Москвы было построено из мячковского известняка, который добывали у села Мячково на Москве-реке и на специальных судах доставляли к месту постройки. Недаром Москву в старину называли белокаменной. В настоящее время известняк служит ценным материалом при производстве цемента, в металлургии в качестве флюса (флюсом в металлургии называют вещества, вводимые в шихту для связывания примесей, например Р2О5, SiO 2 , в легкоплавкие шлаки,) и в химической промышленности при производстве соды, хлорной извести, карбида кальция.
Известь, её производство и применение, 1961
Мел и известняк — это осадочные горные породы, образовавшиеся из остатков панцирей живых организмов (в первую очередь древних простейших — радиолярий и фораминифер).

Успенский собор на Городке. Звенигород. Около 1399 г.

Белокаменная резьба Успенского собора на Городке.
Мрамор — метаморфическая горная порода, образующаяся при перекристаллизации под давлением осадочных карбонатных пород — главным образом известняков. Он также состоит из кальцита (карбоната кальция), однако, в отличие от мела и известняка, это крупнокристаллический материал: на сколе
куска мрамора хорошо заметна его зернистая структура. По сравнению с мелом и известняком мрамор твёрд: недаром древние строили из него храмы. Благодаря различным примесям мрамор часто бывает окрашен, мрамор некоторых месторождений имеет красивую структуру, в которой чередуются слои разной окраски. В древности особенно ценились белоснежный каррарский мрамор, розовый паросский, жёлтый сиенский. Главный храм афинского акрополя — знаменитый Парфенон построен из блоков пентелийского мрамора, который добывали в местечке Пентеликон к северо-востоку от Афин. Пентелийский мрамор имеет едва заметный золотистый оттенок, который усиливается, когда смотришь на Парфенон вечером, на закате солнца. В Италии распространённым сортом мрамора является чипполино — так называют белый мрамор с мелкими жёлтыми или зелёными прожилками. А вот знаменитый красный веронский мрамор ( rosso di Verona ) — на самом деле известняк коричнево-красного цвета, в котором часто встречаются окаменелости.
Различия мела и извести — детальный рассказ

Колонны Парфенона. Афины. Середина V в. до н. э.
Авторы: Андрей Дроздов, Илья Леенсон, Дмитрий Трифонов, Денис Жилин, Александр Серов, Андрей Бреев, Андрей Шевельков, Вадим Ерёмин, Юлия Яковлева, Оксана Рыжова, Виктория Предеина, Наталья Морозова, Алексей Галин, Сергей Каргов, Сергей Бердоносов, Александр Сигеев, Оксана Помаз, Григорий Середа, Владимир Тюрин, Антон Максимов, Вячеслав Загорский, Леонид Каневский, Александр Скундин, Борис Сумм, Игнат Шилов, Екатерина Менделеева, Валерий Лунин, Абрам Блох, Пётр Зоркий, Александр Кури, Екатерина Иванова, Дмитрий Чаркин, Сергей Вацадзе, Григорий Серела, Анастасия Ростоцкая, Александр Серое, Анастасия Сигеева
ИсточникКарбонат кальция

Это СаСО3 — одно из самых распространенных на Земле соединений. Минералы на основе СаСО3 покрывают около 40 млн. км2 земной поверхности. Мел, мрамор, известняки, ракушечники — все это СаСО3 с незначительными примесями, а кальцит — чистый СаСО3.
Самый важный из этих минералов — известняк. (Правильнее говорить не об известняке, а об известняках: известняки разных месторождений отличаются по плотности, составу и количеству примесей.) Известняки есть практически везде. Ракушечники — известняки органического происхождения — особенно распространены на северном побережье Черного моря. Знаменитые Одесские катакомбы — это бывшие каменоломни, в которых добывали ракушечник. Из известняков главным образом сложены и западные склоны Урала.
В чистом виде известняки — белого или светло-желтого цвета, но примеси придают им более темную окраску.
Наиболее чистый СаСО3 образует прозрачные кристаллы известкового или исландского шпата, широко применяемого в оптике. А обычные известняки используются очень широко —почти во всех отраслях народного хозяйства.
Больше всего известняка идет на нужды химической промышленности. Он незаменим в производстве цемента, карбида кальция, соды, всех видов извести (гашеной, негашеной, хлорной), белильных растворов, цианамида кальция, известковой воды и многих других полезных веществ.
Значительное количество известняка расходует и металлургия — в качестве флюсов. Без известняка не обходится ни одно строительство.
Во-первых, из него самого строят, во-вторых, из известняка делают многие строительные материалы.
Известняками (щебенкой) укрепляют дороги, известняками (в виде порошка) уменьшают кислотность почв. В сахарной промышленности известняк используют для очистки свекловичного сока. Другая разновидность углекислого кальция — мел. Мел — это не только зубной порошок и школьные мелки. Его используют в бумажной и резиновой промышленности — в качестве наполнителя, в строительстве и при ремонте зданий — для побелки.
Третья разновидность карбоната кальция — мрамор — встречается реже. Считается, что мрамор образовался из известняка в давние геологические эпохи. При смещениях земной коры отдельные залежи известняка оказывались погребенными под слоями других пород. Под действием высокого давления и температуры там происходил процесс перекристаллизации, и известняк превращался в более плотную кристаллическую породу — мрамор.
Естественный цвет мрамора — белый, но чаще всего различные примеси окрашивают его в разнообразные цвета. Чистый белый мрамор встречается не часто и идет в основном в мастерские скульпторов. Из менее ценных сортов белого мрамора делают распределительные щиты и панели в электротехнике. В строительстве мрамор (всех цветов и оттенков) используют не столько как конструкционный, сколько как облицовочный материал.
И, чтобы покончить с углекислым кальцием, несколько слов о доломите — важном огнеупорном материале и сырье для производства цемента.
Это двойная магние-кальциевая соль угольной кислоты, В состав — СaCO3 · MgCO3.
Карбонат кальция

Очищенный от посторонних примесей, карбонат кальция широко используется в бумажной и пищевой промышленности, при производстве пластмасс, красок, резины, продукции бытовой химии, в строительстве. Производители бумаги используют карбонат кальция одновременно в качестве отбеливателя, наполнителя (заменяя им дорогостоящие волокна и красители), а также раскислителя. Производители стеклянной посуды, бутылок, стекловолокна используют карбонат кальция в огромных количествах в качестве источника кальция — одного из основных элементов, необходимых для производства стекла. Широко используется при производстве продукции личной гигиены (например, зубной пасты), и в медицинской промышленности. В пищевой промышленности часто используется в качестве антислеживающего агента и разделителя в сухих молочных продуктах. При употреблении сверх рекомендованной дозы (1,5 г в день) может вызывать молочно-щелочной синдром (синдром Бернетта). Рекомендован при болезнях костных тканей.
Производители пластмассы — одни из основных потребителей карбоната кальция (более 50 % всего потребления). Используемый в качестве наполнителя и красителя, карбонат кальция необходим при производстве поливинилхлорида (PVC), полиэфирных волокон (кримплен, лавсан, и т. п.), полиолефинов. Изделия из данных видов пластмасс распространены повсеместно — это трубы, сантехника, кафельная плитка, черепица, линолеум, ковровые покрытия, и т. п. Карбонат кальция составляет порядка 20 % красящего пигмента, используемого при производстве красок.
Строительство
Строительство — еще один из основных потребителей карбоната кальция. Шпатлевки, различные герметики — все они содержат карбонат кальция в значительных количествах. Также, карбонат кальция является важнейшим составным элементом при производстве продукции бытовой химии — средств для чистки сантехники, кремов для обуви.
Карбонат кальция также широко используется в очистительных системах, как средство борьбы с загрязнением окружающей среды, при помощи карбоната кальция восстанавливают кислотно-щелочной баланс почвы.
Нахождение в природе

Карбонат кальция находится в минералах в виде полиморфов:
Тригональная кристаллическая структура кальцита является наиболее распространенной.
ИсточникКарбонат кальция

Карбонат кальция (углекислый кальций) — неорганическое химическое соединение, соль угольной кислоты и кальция. Химическая формула CaCO3 .
В природе встречается в виде многочисленных минералов, например, кальцита, арагонита и ватерита, является главной составной частью известняка, мрамора, мела, входит в состав скорлупы яиц птиц.
Нерастворим в воде и этаноле.
Зарегистрирован как белый пищевой краситель (E170).
Содержание
- 1 Применение
- 1.1 Массовое производство/использование
- 1.2 В строительстве
Применение
Используется как белый пищевой краситель E170. Являясь основой мела, используется для письма на досках. Используется в быту для побелки потолков, покраски стволов деревьев, для подщелачивания почвы в садоводстве.
Массовое производство/использование


Очищенный от примесей, карбонат кальция широко используется в бумажной и пищевой промышленности, в качестве наполнителя при производстве пластмасс, красок, резины, продукции бытовой химии, в строительстве.
При производстве бумаги карбонат кальция применяют одновременно в качестве отбеливателя, наполнителя, а также раскислителя.
Используется при производстве силикатного стекла, — материала для производства оконного стекла, стеклянных бутылок, стекловолокна.
Применяется при производстве предметов гигиены (например, зубной пасты), в медицине.
В пищевой промышленности часто используется в качестве препарата препятствующего слеживанию и для препятствования слипания в комки сухих молочных продуктах.
При употреблении сверх рекомендованной дозы (1,5 г в день) может вызывать молочно-щелочной синдром (синдром Бернетта). Рекомендован при болезнях костных тканей.
Производители пластмассы — одни из основных потребителей чистого карбоната кальция (более 50% всего потребления). Используемый в качестве наполнителя и красителя, карбонат кальция необходим при производстве поливинилхлорида (PVC), полиэфирных волокон (кримплен, лавсан, и т. п.), полиолефинов. Изделия из данных видов пластмасс распространены повсеместно — это трубы, сантехника, кафельная плитка, черепица, линолеум, ковровые покрытия, и т.п. Карбонат кальция составляет порядка 20% красящего пигмента, используемого при производстве красок.
В строительстве
Строительство — ещё один из основных потребителей карбоната кальция. Например, в качестве наполнителя шпаклёвок и герметиков.
Также карбонат кальция является важным составным элементом при производстве продукции бытовой химии — средств для чистки сантехники, кремов для обуви.
Карбонат кальция широко применяется для раскисления кислых почв.
Нахождение в природе
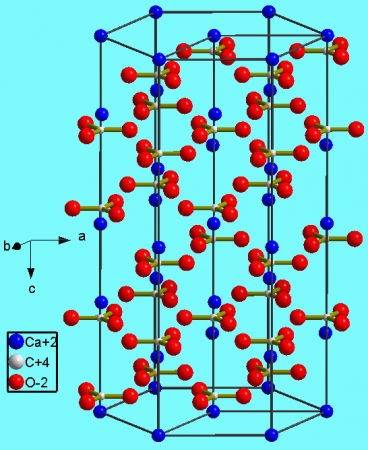
Карбонат кальция находится в минералах в виде полиморфов:
Тригональная кристаллическая структура кальцита является наиболее распространенной.
Минералы карбоната кальция находятся в следующих горных породах:



Геология
Залежи карбоната кальция в виде меловых пластов — отложений известковых раковин моллюсков, в основном, мелового периода является распространенным минералом на всех континентах.
В природе встречаются три кристаллические модификации (минералы с одинаковым химическим составом, но с различной кристаллической структурой): кальцит, арагонит и фатерит (ватерит).
Некоторые горные породы (известняк, мел, мрамор, травертин и другие известковые туфы) практически полностью состоят из карбоната кальция с различными примесями.
Кальцит является устойчивой кристаллической модификацией карбоната кальция и встречается в самых разнообразных геологических условиях: в осадочных, метаморфических и магматических горных породах.
Около 10 % всех осадочных пород составляют известняки, сложенные преимущественно кальцитовыми остатками раковин морских организмов. Арагонит является второй по распространённости кристаллической модификацией CaCO3 и в основном формируется в раковинах моллюсков и скелетах некоторых других организмов.
Также арагонит может образовываться и в неорганических процессах, например в карстовых пещерах или гидротермальных источниках.
Фатерит является наименее стабильной разновидностью этого карбоната, и очень быстро превращается в воде либо в кальцит, либо в арагонит. В природе встречается относительно редко, когда его кристаллическая структура стабилизирована теми или иными примесями.
Получение
Подавляющее количество карбоната кальция, добывающееся из полезных ископаемых, используется в промышленности. Чистый карбонат кальция (например, для производства продуктов питания или использования в фармацевтических целях), может быть изготовлен из природного минерала с малым количеством вредных примесей, например, из мрамора.
В лаборатории карбонат кальция может быть приготовлен предварительным гашением оксида кальция — негашеной извести. При этом образуется гидроксид кальция, и затем в суспензию продувается углекислый газ для получения карбоната кальция:
Химические свойства
При нагревании до 900—1000 °C разлагается на кислотный оксид — углекислый газ CO2 и основный оксид — негашёную известь CaO:
Растворяется в воде при избытке углекислого газа образуя кислую соль — гидрокарбонат кальция Ca(HCO3)2:
Из-за этой реакции образуются сталактиты, сталагмиты. Природные подземные воды, обильные углекислом газом, растворяют плохо растворимый карбонат кальция с образованием много лучше растворимого в воде гидрокарбоната кальция, при выделении подземной воды в виде капель с потолков пещер при попадании в воздух с низкой концентрацией углекислого газа происходит обратная реакция превращения гидрокарбоната кальция в плохо растворимый осадок карбоната кальция, образующего красивые природные формы в пещерах, и из-за этого же механизма образуются карстовые пещеры.
При обжиге с температурой свыше 1500 °C с углеродом, например, в форме кокса, образует карбид кальция и угарный газ:
Источник