Металлы платиновой группы: список
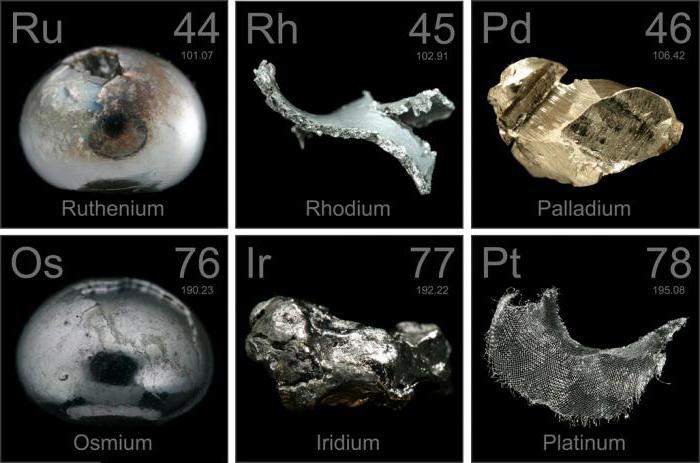
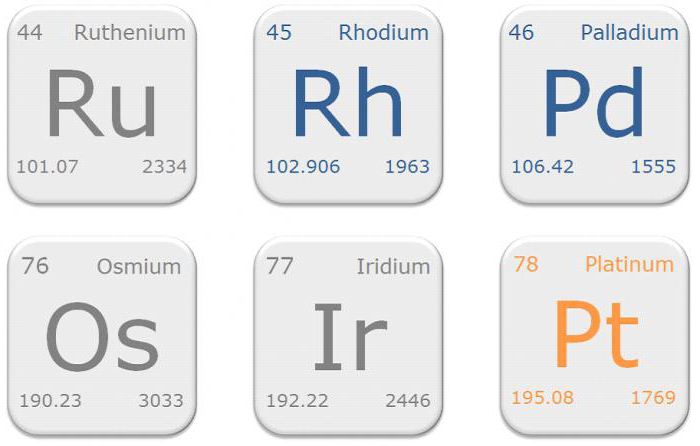
Группа состоит из следующих шести химических элементов, расположенных в порядке возрастания атомного веса:
- Ru – рутений.
- Rh – родий.
- Pd – палладий.
- Os – осмий.
- Ir – иридий.
- Pt – платина.
Металлы платиновой группы обладают серебристо-белым оттенком, за исключением осмия, цвет которого голубовато-белый. Их химическое поведение парадоксально в том, что они обладают высокой устойчивостью к воздействию большинства реагентов, но используются в качестве катализаторов, легко ускоряющих или контролирующих скорость окисления, восстановления и реакций гидрирования.
Рутений и осмий кристаллизуются в гексагональную плотноупакованную систему, а другие обладают гранецентрированной кубической структурой. Это выражается в большей твердости рутения и осмия.
САМЫЙ ДОРОГОЙ МЕТАЛЛ В МИРЕ . ТОП-5 золото, платина, иридий, родий, серебро(gold, silver, platinum)
История открытия
Хотя платиносодержащие золотые артефакты датированы 700 г. до н. э., присутствие этого металла является, скорее, случайностью, чем закономерностью. Иезуиты в XVI веке упоминали серые плотные камешки, связанные с аллювиальными месторождениями золота. Эти камешки нельзя было расплавить, но они образовывали сплав с золотом, при этом слитки становились ломкими, и их уже было невозможно очистить. Камешки стали называть platina del Pinto – гранулы серебристого материала из реки Пинто, впадающей реку Сан-Хуан в Колумбии.
Ковкая платина, которую можно получить только после полной очистки металла, была выделена французским физиком Шабано в 1789 году. Из нее был сделан кубок, преподнесенный папе Пию VI. Об открытии палладия в 1802 году сообщил английский химик Уильям Волластон, который назвал хим. элемент группы платиновых металлов в честь астероида.
Волластон впоследствии заявлял об обнаружении еще одного вещества, присутствующего в платиновой руде. Его он назвал родием из-за розового цвета солей металла. Открытия иридия (по имени богини радуги Ириды из-за пестрой окраски его солей) и осмия (от греческого слова «запах» из-за хлорного запаха его летучего окисла) были сделаны английским химиком Смитсоном Теннантом в 1803 году. Французские ученые Ипполит-Виктор Колле-Дескоти, Антуан-Франсуа Фуркруа, и Николя-Луи Воклен выделили два металла одновременно. Рутений, последний изолированный и идентифицированный элемент, получил свое название по латинскому наименованию России от русского химика Карла Карловича Клауса в 1844 году.
В отличие от таких легко выделяемых в относительно чистом состоянии путем простого огневого рафинирования веществ, как золото, серебро, металлы платиновой группы требуют сложной водно-химической обработки. Эти методы не были доступны до конца 19 века, поэтому выявление и изоляция платиновой группы отстала от серебра и золота на тысячи лет.
Кроме того, высокая температура плавления этих металлов ограничивала их применение, пока исследователи в Британии, Франции, Германии и России не разработали методы преобразования платины в форму, пригодную для обработки. Как драгоценные металлы платиновой группы начали использоваться в ювелирных изделиях с 1900 года. Хотя такое применение остается актуальным и сегодня, промышленное намного его превзошло. Палладий стал очень востребованным материалом для контактов в телефонных реле и других системах проводной коммуникации, обеспечивая длительный срок службы и высокую надежность, а платина, из-за своей устойчивости к искровой эрозии, во время Второй мировой войны стала применяться в свечах зажигания боевых самолетов.
После войны расширение методов молекулярной конверсии при переработке нефти создало огромный спрос на каталитические свойства, которыми обладают металлы платиновой группы. К 1970-м годам потребление выросло еще больше, когда стандарты автомобильных выбросов в США и других странах привело к использованию данных химических элементов в каталитической конверсии выхлопных газов.
Руды
За исключением малых россыпных месторождений платины, палладия и осмистого иридия (сплава иридия и осмия), практически нет руды, в которой бы основным компонентом был химический элемент – металл платиновой группы. Минералы, как правило, содержатся в сульфидных рудах, в частности в пентландите (Ni, Fe)9S8. Наиболее распространены лаурит RuS2, ирарсит, (Ir,Ru,Rh,Pt)AsS, осмиридиум (Ir,Os), куперит, (PtS) и браггит (Pt,Pd)S.
Крупнейшее в мире месторождение металлов платиновой группы – Бушвельдский комплекс в ЮАР. Большие запасы сырья сосредоточены в месторождениях Садбери в Канаде и Норильско-Талнахском в Сибири. В США наибольшие залежи минералов платиновой группы расположены в Стилуотере, Монтана, но здесь они значительно меньше, чем в ЮАР и России. Крупнейшими в мире производителями платины являются Южная Африка, Россия, Зимбабве и Канада.

Добыча и обогащение
Основные южноафриканские и канадские месторождения эксплуатируются шахтным способом. Практически все металлы платиновой группы извлекаются из медных или никелевых сульфидных минералов с помощью флотационной сепарации. Плавка концентрата производит смесь, которая вымывается из меди и сульфидов никеля в автоклаве. Твердый остаток выщелачивания содержит от 15 до 20% металлов платиновой группы.
Иногда до флотации используется гравитационное разделение. В результате получается концентрат, содержащий до 50% платиновых металлов, что избавляет от необходимости выплавки.
Механические свойства
Металлы платиновой группы значительно отличаются механическими свойствами. Платина и палладий довольно мягкие и очень ковкие. С этими металлами и их сплавами можно работать как в горячем, так и в холодном состоянии. Родий сначала обрабатывают горячим, а позже его можно обрабатывать холодным с довольно частым отжигом. Иридий и рутений должны быть нагреты, холодной обработке они не поддаются.
Осмий – самый твердый из группы и имеет наиболее высокую температуру плавления, но его склонность к окислению накладывает свои ограничения. Иридий наиболее коррозионностойкий из платиновых металлов, а родий ценится за сохранение своих свойств при высоких температурах.

Структурные применения
Поскольку дочиста отожженная платина очень мягкая, она восприимчива к царапинам и порче. Для увеличения твердости ее сплавляют со множеством других элементов. Платиновые драгоценности очень популярны в Японии, где ее называется «хаккин» и «белое золото». Сплавы для ювелирных изделий содержат 90% Pt и 10% Pd, который легко обрабатывать и паять.
Добавление рутения повышает твердость сплава, сохраняя стойкость к окислению. Сплавы платины, палладия и меди используются в кованых изделиях, так как они тверже платино-палладиевых и менее затратны.
Тигли, используемые для производства монокристаллов в полупроводниковой промышленности, требуют коррозионной устойчивости и стабильности при высоких температурах. Для этого применения лучше всего подходят платина, платина-родий и иридий. Платинородиевые сплавы используются в производстве термопар, которые предназначены для измерения повышенных температур до 1800 °C. Палладий применяют как в чистом, так и в смешанном виде в электрических устройствах (50% потребления), в стоматологических сплавах (30%). Родий, рутений и осмий редко используются в чистом виде – они служат легирующей добавкой для других металлов платиновой группы.

Катализаторы
Около 42% всей платины, произведенной на Западе, используется в качестве катализатора. Из них 90% применяется в автомобильных выхлопных системах, где тугоплавкие гранулы или сотовые конструкции с платиновым покрытием (а также палладиевым и родиевым) содействуют преобразованию несгоревших углеводородов, окиси углерода и окислов азота в воду, углекислый газ и азот.
Сплав платины и 10% родия в виде раскаленной докрасна металлической сетки служит катализатором в реакции между аммиаком и воздухом для получения окислов азота и азотной кислоты. При подаче вместе со смесью аммиака метана можно получить синильную кислоту. При переработке нефти платина на поверхности гранул оксида алюминия в реакторе является катализатором преобразования длинноцепочечных молекул нефти в разветвленные изопарафины, которые желательны в смеси высокооктановых бензинов.

Гальваника
Все металлы платиновой группы можно наносить гальванически. Из-за твердости и блеска получаемого покрытия наиболее часто применяется родий. Хотя его стоимость выше, чем платины, меньшая плотность позволяет использовать меньшую массу материала при сопоставимой толщине.
Палладий – металл платиновой группы, который проще всего использовать для нанесения покрытий. Благодаря этому прочность материала значительно повышается. Рутений нашел применение в инструментах, предназначенных для обработки трением при низком давлении.
Химические соединения
Органические комплексы металлов платиновой группы, такие как комплексы алкилплатины, используются в качестве катализаторов в процессе полимеризации олефинов, производстве полипропилена и полиэтилена, а также при окислении этилена в ацетальдегид.
Соли платины находят все более широкое применение в химиотерапии рака. Например, они входят в состав таких лекарств, как «Карбоплатин» и «Цисплатин». Покрытые оксидом рутения электроды используются в производстве хлора и хлората натрия. Сульфат и фосфат родия применяются в родиевых гальванических ваннах.
Источник: fb.ru
Изучите 6 металлов платиновой группы за 3 минуты
Помимо золота и серебра, наиболее часто упоминаемым благородным металлом в быту является платина. Из-за своей редкости и драгоценности платина пользуется большим спросом у европейских королевских семей. Например, король Франции Людовик XVI заявил, что «платина — единственный металл, подходящий для королей», у него была платиновая чаша.

Как наиболее признанный металл среди металлов платиновой группы, широкое использование платины также раскрыло тайну металлов платиновой группы (МПГ).
Шесть металлов платиновой группы — это платина, палладий, родий, иридий, рутений и осмий. Они имеют схожие физические и химические свойства и, как правило, встречаются вместе в одних и тех же месторождениях полезных ископаемых.
Платина

Химический символ: Pt
Атомный номер (количество протонов в ядре): 78
Температура плавления: 3215,1 градуса по Фаренгейту (1768,4 градуса по Цельсию)
Назван от испанского «platina del Pinto», что означает «маленькое серебро реки Пинто».
Платина очень популярна в ювелирной промышленности, а платина часто используется в обручальных кольцах, чтобы выразить невинность и долговечность любви.
Платина является превосходным хорошим катализатором окисления. Одним из наиболее популярных применений для нее являются каталитические нейтрализаторы, используемые для устранения выбросов оксида азота, монооксида углерода или выбросов углеводородов из несгоревшего топлива. Количество платины, доступной в каталитическом нейтрализаторе, может значительно различаться в зависимости от модели. и производитель. Но в среднем в стандартном каталитическом нейтрализаторе содержится от 3 до 7 граммов платины.
В стекольной промышленности платиновые тигли используются для плавки и обработки расплавленных оптических приборов и стекла специального назначения.
 Платиновое кольцо
Платиновое кольцо Платина в каталитических нейтрализаторах
Платина в каталитических нейтрализаторах Преобразователи платиновых тиглей
Преобразователи платиновых тиглей
Палладий

Химический символ: Pd
Атомный номер (количество протонов в ядре): 46
Температура плавления: 2831 градус по Фаренгейту (1555 градусов по Цельсию)
Назван в честь астероида Паллада.
Палладий, известный как наиболее устойчивый к коррозии чистый металл, устойчив к солям, оксидам и неорганическим кислотам, но подвержен влиянию хлорида натрия и цианида натрия. Он также имеет высокую температуру плавления (хотя и самую низкую из всех металлов платиновой группы) и устойчивость к деформации, что полезно для упрочнения сплавов.
Палладий также используется в ювелирных изделиях, хотя он не так популярен, как платина.
Уникальное качество палладия заключается в его способности поглощать в 900 раз больше собственного объема водорода при комнатной температуре. Это делает его эффективным и безопасным носителем и очистителем водорода. Он также используется в химических процессах, требующих обмена водородом между двумя реагентами, такими как бутадиен, сырье для производства синтетического каучука.
Палладий обладает прекрасными каталитическими свойствами, как и платина, поэтому его можно использовать в качестве замены более дорогой платины в каталитических нейтрализаторах.
 Кольцо из палладия
Кольцо из палладия Палладий в синтетическом каучуке
Палладий в синтетическом каучуке Палладий в каталитических нейтрализаторах
Палладий в каталитических нейтрализаторах
Родий

Химический символ: Rh
Атомный номер (количество протонов в ядре): 45
Температура плавления: 3567 градусов по Фаренгейту (1964 градуса по Цельсию)
Назван в честь розового цвета его солей.
Как родственные металлы платина и палладий, родий также обладает превосходной каталитической активностью. Поэтому родий в основном используется в каталитических нейтрализаторах автомобилей, где он уменьшает количество оксидов азота (NOx), выбрасываемых выхлопными газами в атмосферу. Это предпочтительный металл для контроля NOx.
Родий обладает высокой отражательной способностью для видимого света и может использоваться для изготовления покрытий для промышленных зеркал и отражателей.
Высокая температура плавления родия, стабильность при высоких температурах и коррозионная стойкость делают его ключевым элементом многих промышленных процессов, таких как производство стекла и стекловолокна. Родий также используется для изготовления стекла из-за его высокой температуры плавления и температурной стабильности.
 Родий в каталитических нейтрализаторах
Родий в каталитических нейтрализаторах Зеркало с родиевым покрытием
Зеркало с родиевым покрытием Родий в производстве стекла
Родий в производстве стекла
Иридий

Химический символ: Ir
Атомный номер (количество протонов в ядре): 77
Температура плавления: 4435 F (2446 C)
Назван в честь Ирис, богини радуги.
Иридий — самый редкий металл платиновой группы и самый устойчивый к коррозии из известных элементов.
Иридий очень твердый и часто смешивается с осмием, образуя осмиево-иридиевый сплав для перьев ручек и подшипников компаса.
Биосовместимость Iridium помогает нам больше всего. Иридий можно использовать в ряде медицинских приложений, таких как медицинские технологии для борьбы с раком, сердечными заболеваниями и даже глухотой и слепотой.
Иридий обладает лучшей отражательной способностью в рентгеновских лучах, чем никель, золото и платина, поэтому он также используется в рентгеновских телескопах.
 Иридий в ручках
Иридий в ручках Иридиум в медицинских приложениях
Иридиум в медицинских приложениях Иридий в рентгеновских телескопах
Иридий в рентгеновских телескопах
Рутений

Химический символ: Ru
Атомный номер (количество протонов в ядре): 44
Температура плавления: 4233 F (2334 C)
Назван в честь русской нации
Рутений является одним из наиболее эффективных упрочнителей для платины и палладия и образует сплавы с этими металлами для изготовления электрических контактов и чип-резисторов с высокой износостойкостью.
Рутений используется в катализаторах производства аммиака и уксусной кислоты. Соединения рутения используются в солнечных батареях для преобразования энергии света в электричество.
 Рутений в чип-резисторах
Рутений в чип-резисторах Рутений в катализаторах
Рутений в катализаторах Рутений в солнечных батареях
Рутений в солнечных батареях
Осмий

Химический символ: Ос
Атомный номер (количество протонов в ядре): 76
Температура плавления: 5491,4 F (3033 C)
Назван от греческого слова «запах».
Осмий имеет красивый светло-серо-голубой цвет. В отличие от других металлов платиновой группы (платина, иридий, рутений, родий и палладий), которые имеют серебристый цвет.
Это самый плотный элемент в периодической таблице и самый твердый из всех металлов платиновой группы. Он в десять раз тверже платины. Осмий также имеет более высокую температуру плавления, чем другие металлы платиновой группы.
Высокая твердость делает его полезным там, где требуется твердость и долговечность. Например, перьевые ручки, электрические контакты и жесткие шарикоподшипники.
Осмий является чрезвычайно эффективным катализатором окисления. Когда осмий используется в качестве катализатора для синтеза аммиака или гидрирования, более высокая скорость превращения может быть получена при низкой температуре.
Четырехокись осмия (OsO4), важное соединение осмия, используется для окрашивания биологических образцов для микроскопии и обнаружения отпечатков пальцев.
 Шарикоподшипники из осмиевого сплава
Шарикоподшипники из осмиевого сплава Осмий в катализаторах
Осмий в катализаторах Осмий для обнаружения отпечатков пальцев
Осмий для обнаружения отпечатков пальцев
Вывод
От платиновых украшений до ручек, от лекарств от рака до сотовых телефонов, от автомобильных каталитических преобразователей до электрических контактов, эти 6 металлов платиновой группы играют жизненно важную роль в нашей повседневной жизни и промышленном развитии. Подсчитано, что четверть производимых сегодня товаров содержат МПГ или что МПГ играют ключевую роль в процессе их производства.
Растущее значение МПГ также привлекло внимание к добыче и переработке МПГ, что является предметом нашего следующего сообщения в блоге.

Автор : Jordan Джордан — автор блога, обладающий обширными знаниями в этой отрасли. Самое Самое главное, он искренне надеется помочь вам в ваших проектах.
- Интересные факты, которые вы должны знать о барите
- 5 неожиданных применений порошка слюды, о которых вы могли не знать
- Металлический никель в аккумуляторе: почему его называют металлом дьявола?
Источник: www.ftmmachinery.com
Все о платиновых металлах

Практически каждый человек знает о существовании драгоценных металлов. К их числу относят серебро, золото и платину. При этом далеко не каждому известно о существовании платиновой группы. Ее представителей также относят к числу благородных.
Особенности
Платиновые металлы – это группа из 6 элементов, которые расположены рядом друг с другом в периодической химической таблице. Каждый их элементов группы по праву считается благородным. Это связано со следующими химическими и физическими свойствами.
- Специалисты отмечают низкую концентрацию платиновых металлов. Количество месторождений невелико. Данная характеристика также относится к химическим элементам, которые традиционно считаются редкими и дорогостоящими.
- Представители вышеуказанной группы обладают свойствами следующих металлов: родий, осмий, палладий, рутений.
- В процессе изучения платиноидов было отменно сходство в атомном строении с элементами, указными выше.
Ученые, работающие в области химии, поделили все платиновые металлы на две группы, называемые триадами.
Разделение производится по весу.
- Группа №1. Это самые легкие представители. К ним относится палладий, рутений и родий.
- Группа №2. Оставшиеся 6 металлов – иридий, осмий и сама платина. Это уже тяжелые металлы.
Металлы и их свойства
У металлов вышеуказанной группы имеются свои обозначения. Список такой.
- Рутений – Ru.
- Родий – Rh.
- Палладий – Pd.
- Осмий – Os.
- Иридий – Ir.
- Платина – Pt.
Заметка: все обозначения расположены в определенном порядке, согласно атомному весу.
От наименьшего значения к большему. Все платиновые металлы обладают схожими характеристиками.
- Первое сходство заключается во внешнем виде. Практически все элементы, кроме осмия, имеют светлый оттенок (сочетание белого и серебристого цветов). Осмий отличается легким голубоватым тоном.
- Металлы имеют высокую устойчивость по отношению к множеству реагентов. При этом платиноиды являются эффективными катализаторами.
- С их помощью контролируют различные химические процессы, управляют скоростью окисления, а также следят за другими реакциями. Такое поведение металлов считается удивительным и парадоксальным.
Свойства
На поверхности не образуется окисление. Таким образом, наглядно демонстрируется инертность. По мнению специалистов, она особенно заметна у платины. При изучении представителей платиновой группы нельзя было обойти стороной температуру плавления. Самое низкое значение у палладия и составляет 1554 градуса.
Самое высокое значение у осмия. Его температура насчитывает 3 тысячи 27 градусов по Цельсию.
Следующее одинаковое свойства – тугоплавкость. Данная характеристика говорит о замечательной износостойкости. Несмотря на внешнее сходство, физические качества отличаются. В зависимости от этих показателей, при обработке используются специальные методики. Рутений и осмий – очень хрупкие металлы и требуют особо бережного отношения.
Высокая пластичность – показатель палладия и платины.
Где добываются?
Месторождения платиновых металлов обычно рассеяны на территории Канады и Южной Африки. В этих регионах получение полезного ископаемого происходит стандартным шахтным способом. Как показывает практика, большинство платиноидов добывается путем извлечения элементов из никелевых сульфидных минералов или же медных руд. В работе используют флотационную сепарацию.
В процессе обработки металла выполняется плавка полученного концентрата, в результате этого получается специальная смесь. Объем платиновых металлов – от 15 до 20% от сухого остатка.
В некоторых случаях процесс добычи и обработки может отличаться. Иногда на заводах используется гравитационное разделение. В этом случае количество необходимых химических элементов возрастает до 50%. Такой вариант обработки исключает выплавку. Несмотря на то что богатые залежи МПГ встречаются редко, некоторые месторождения также находятся на территории Канады, Китая, Австралии и Финляндии.
Существуют и другие источники, однако, доля их добычи насчитывает всего 0,3% от общей массы, добываемой на планете.
Где используются?
Платиноиды нашли свое применение в различных сферах. Универсальные свойства металлов данной группы активно используются на сегодняшний день. Чистая платина само по себе очень мягкая и податливая. В таком состоянии она очень восприимчива и различным повреждениям и дефектам.
Чтобы повысить твердость и износостойкость драгоценного металла, используются различные элементы. Платину сплавляют с другими химическими элементами.
Ювелирные украшения из платины высоко ценятся и стоят дороже золота. Особую популярность они обрели в Японии. Жители Страны восходящего солнца называют такие изделия «хаккин». Основной ювелирного сплава является платина и составляет 90% от общей массы. Оставшиеся 10% – это палладий.
С ним легко работать, включая пайку и другую обработку.
Также для увеличения твердости, драгоценный белый металл соединяют с рутением. Добавление этого элемента увеличивает стойкость к процессу окисления. МПГ нашли свое применение в изготовлении кованых изделий. В этом случае используется сплав, состоящий из меди, платины и палладия. Такой вариант более доступный по цене, по сравнению с составом из двух элементов: платины и палладия.
Специальные сплавы, которые делаются с использованием платиноидов, широко используются при изготовлении термопар. Это специальное устройство с широким спектром применения. Его основное предназначение заключается в изменении высоких температур (максимальное значение – до 1800 градусов по Цельсию выше нуля). Некоторые представители применяются в чистом виде.
Как правило, они выступают в качестве добавок к остальным металлам из платиновой группы. Палладий нашел свое применение в сфере производства электрического оборудования, а также в современных стоматологических сплавах.
Катализаторы
Более 40% всей полученной платины, которая изготавливается за границей, используется как катализатор. Это удивительное и полезное свойство было обозначено еще в первой части статьи. Практически весь металл (примерно 90%) нашел свое применение в сфере производства выхлопных систем для автомобилей.
Драгоценный материал, а также родий и палладий, выступает в качестве защитного покрытия для сотовых конструкций и других элементов. Слой металла защищает от процессов окисления, сохраняя оборудование целым и невредимым. Вступая в химическую реакцию, агрессивные компоненты преобразовываются в безопасные соединения и вещества.
Химические элементы могут выполнять задачу эффективного катализатора не только в качестве покрытия, но и в виде раскаленной сетки из металла. В этом случае происходит реакция между воздухом и ядовитым веществом – аммиаком. В результате получается азотная кислота и оксид азота. Для получения других веществ добавляют различные компоненты.
Еще одна сфера, которая не обходится без использования МПГ – добыча нефти. Это глобальная отрасль, которая указывает на ценность платиноидов и их важность в промышленности.
Другие варианты использования металлов такие.
- На территории России из палладия изготавливаются инвестиционные монеты. Делать это начали после того, как во времена СССР была выпущена монета из чистого палладия. Номинал – 25 рублей.
- Высоковольтное оборудование также не обходится без использования МПГ. При изготовлении электроники данного типа нужны износостойкие и надежные контакты, которые будут устойчивы к негативному воздействию со стороны. Несмотря на развитие новых технологий, в настоящее время нет действующей альтернативы платиноидам.
- В процессе изготовления инструментов и устройств для работы в сложных условиях также активно используются такие металлы. Чтобы трудиться в агрессивной среде, оборудование должно быть прочным, износостойким и долговечным. Именно эти характеристики оно получает от платиновых металлов.
- Чтобы значительно повысить стойкость титана к коррозии, к нему добавляют немного палладия. Также данный элемент платиновой группы часто подмешивают к стали.
- В области медицины активные соединения также активно используются. Данная практика применялась ранее и сохраняет актуальность на сегодняшний день.
- Не стоит забывать о платиновой фольге. Этот материал используется, чтобы защищать устройство химических реакторов.
- Сплав из серебра и палладия активно применяется в слаботочной электронике.
О том, как ещё используется этот драгоценный металл, смотрите в следующем видео.
Источник: vplate.ru