Найдите правильный ответ на вопрос ✅ «Почему бериллий и магний не являются щелочноземельными металлами? . » по предмету Химия, а если вы сомневаетесь в правильности ответов или ответ отсутствует, то попробуйте воспользоваться умным поиском на сайте и найти ответы на похожие вопросы.
Новые вопросы по химии
Придумайте необычные описания характеризующие воду.
Химия: Какие частицы входят в состав ядра атома? а). электроны б). протоны в). нейтроны г). ионы
По положению элемента #40 в табл Менделеева запишите электрон конфигур. Выделите ваоентные электронв и распредилите их по квантовым состоянием в стабильном и возбуж состояниях. Для валент электрон запишите квант числа.
CH3-CH2-CH2-Cl+KOH⇒?
Сожгли вещество, масса которого 13,8 грамм, при этом выделился оксид углерода (четырех валентный) объемом 23,52 литра, и вода массой 10,8 грамм. Плотность этого вещества по водороду 46. Установить молекулярную формулу
Источник: iotvet.com
Магний и щелочноземельные металлы
Почему магний не щелочноземельный металл
Ключевые слова конспекта: щелочноземельные металлы, элементы IIA-группы, земли, получение щелочноземельных металлов.
ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ IIA ГРУППЫ
К щёлочноземельным металлам относят кальций Са, стронций Sr, барий Ва, радий Ra – металлы IIА-группы. Название «щёлочноземельные» обусловлено тем, что гидроксиды этих металлов относятся к щелочам – растворимым в воде основаниям, а оксиды этих металлов с древних времён называли землями. Бериллий и магний к щёлочноземельным металлам не относятся.
Важнейшие параметры элементов IIA группы приведены в таблице:
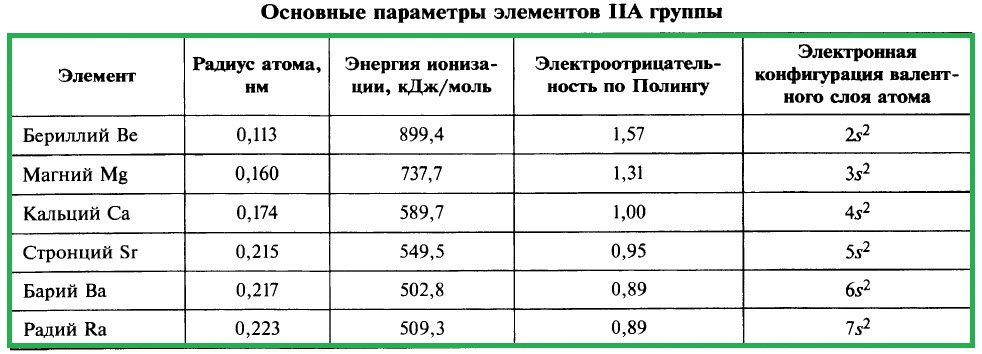
Электронная конфигурация валентного слоя атомов щёлочноземельных металлов в стационарном состоянии ns 2 . Щёлочноземельные металлы являются s-элементами. Во всех своих соединениях они имеют степень окисления +2.
Высшие оксиды щёлочноземельных металлов имеют состав МеО и проявляют основный характер. Высшие гидроксиды этих элементов Ме(ОН)2 являются типичными основаниями, их относят к щелочам, хотя их растворимость намного ниже, чем гидроксидов щелочных металлов. Водородные соединения щёлочноземельных металлов представляют собой твёрдые гидриды состава МеH2.
ЩЁЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ – ПРОСТЫЕ ВЕЩЕСТВА
При обычных условиях щёлочноземельные металлы – твёрдые вещества, имеют металлический блеск на свежем срезе (быстро покрываются желтоватой плёнкой на воздухе), лёгкие (кроме радия), при этом более твёрдые, чем щелочные металлы. Кальций не режется ножом, он довольно твёрдый, стронций и барий мягче. Барий похож по твёрдости на свинец, но в отличие от него при разрезании крошится на отдельные кристаллы.
При внесении щёлочноземельных металлов или их соединений в бесцветное пламя появляется его характерная окраска:
Магний и щелочноземельные металлы. Видеоурок 15. Химия 9 класс

При сгорании щёлочноземельных металлов на воздухе или в кислороде образуются оксиды:
При нагревании на воздухе или в кислороде кальций загорается, пламя при этом имеет красноватый цвет.

Щёлочноземельные металлы взаимодействуют с серой при нагревании. Образуются сульфиды:

При нагревании щёлочноземельные металлы реагируют с азотом с образованием нитридов (Са – при температуре красного каления):

При нагревании щёлочноземельные металлы взаимодействуют с водородом с образованием твёрдых гидридов:

Щёлочноземельные металлы легко взаимодействуют с водой с образованием щёлочи и водорода:
Кальций с холодной водой реагирует сравнительно медленно, но с горячей водой реакция идёт бурно.

Щёлочноземельные металлы активно реагируют с разбавленными кислотами с образованием соли и водорода, но при этом, как и в случае щелочных металлов, параллельно происходит взаимодействие щёлочноземельного металла с водой. По-другому происходит взаимодействие сконцентрированными растворами кислот или с самими кислотами, являющимися сильными окислителями (HNO3, H2SO4). Происходит восстановление азота в высшей степени окисления (в HNO3) или серы в высшей степени окисления (в H2SO4). Образуется соль, продукт восстановления соответственно азота или серы и воды:
Щёлочноземельные металлы активно взаимодействуют с растворами солей, но происходит, как и в случае щелочных металлов, не замещение металла, входящего в состав соли, а реакция щёлочноземельных металлов с водой раствора.

Кальций и стронций получают электролизом расплавов хлоридов:
Конспект урока по химии «Щелочноземельные металлы. Элементы IIA-группы». Выберите дальнейшее действие:
- Вернуться к Списку конспектов по химии
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии
Источник: uchitel.pro
Щелочноземельные металлы
В системе периодических элементов щелочноземельные металлы занимают отдельный столбик, второй слева. Иногда их так и называют — элементы второй группы.
Щелочноземельные металлы в периодической системе элементов
Почему эта группа металлов получила название щелочноземельные?
Оказывается, в древние времена землями назывались те соединения, которые плохо растворялись в воде. А так как при взаимодействии оксидов стронция, кальция и бария с водой образовывалась щелочь, то такие оксиды назвали щелочными землями, а металлы, соответственно, щелочноземельными.

Щелочноземельные металлы горят разным по цвету пламенем: так, например, пламя кальция и радия красного цвета, магния — насыщенно-белого, а стронция — малинового, бария — зеленого, бериллия — белого
Какие элементы входят в группу щелочноземельных металлов?
В список металлов этой группы входят бериллий, магний, кальций, стронций, барий и радий.
Все щелочноземельные металлы обладают общими характеристиками:
- Все металлы белого цвета с блестящей поверхностью.
- В отличие от щелочных металлов, они более твердые и ножом не режутся (исключение составляет стронций, который можно разрезать ножом).
- При контакте с воздухом они окисляются и теряют блеск.
- По сравнению со щелочными металлами активность щелочноземельных гораздо ниже.
- У металлов этой группы два валентных электрона, которые они легко теряют.
- Все щелочноземельные металлы (кроме бериллия) довольно активны по отношению к воде: из ее молекулы они вытесняют водород и образуют гидроксиды. При этом магний реагирует только на кипящую воду.
Нахождение в природе
Наиболее распространенным из щелочноземельных металлов является кальций. Остальные элементы этой группы располагаются в порядке уменьшения их количества на Земле следующим образом: магний, барий, стронций, бериллий и радий.
Источник: sitekid.ru