1. Степень окисления атомов в простом веществе равна нулю . (Cu 0 , H2 0 )
2. Сумма степеней окисления всех атомов в молекуле вещества равна нулю .
3. Степень окисления водорода в соединениях с неметаллами равна +1 .
4. Степень окисления водорода с металлами равна -1.
5. Степень окисления кислорода равна -2 (кроме OF2 и H2O2)
6. Окислители — атомы, ионы или молекулы, принимающие электроны, у окислителей степень окисления понижается .
7. Восстановители — атомы, ионы или молекулы, отдающие электроны, у восстановителей степень окисления повышается .
Таблица элементов с постоянной степенью окисления
| Элементы | Степень окисления в сложных веществах |
| Li, Na, K, Rb, Cs | +1 |
| Be, Mg, Ca, Sr, Ba, Zn | +2 |
| B, Al | +3 |
| F | -1 |
В соединениях из трех элементов степень окисления одного из элементов вычисляют, исходя из условия, что молекула электронейтральна.
ЕГЭ по химии — Что такое постоянная степень окисления?
Например, в молекуле фосфорной кислоты H3PO4 степень окисления водорода равна +1, кислорода -2, степень окисления фосфора обозначим за х.
Степень окисления фосфора рассчитываем по уравнению:
3 * (+1) + х + 4* (-2) = 0
Давайте порассуждаем вместе
1. Атом азота в азотной кислоте имеет степень окисления:
1) 0
2) +3
3) +5
4) -5
Ответ: Формула азотной кислоты HNO3, степень окисления водорода равна +1, кислорода -2, степень окисления азота обозначим за х и рассчитаем ее по уравнению: + 1 + х + 3* (-2) = 0
х = +5
2. Степень окисления -2 атом серы проявляет в каждом из соединений
1) CuSO4 и H2S
2) SO2 и Na2S
3) H2SO3 и SO3
4) CaS и FeS
Ответ: степень окисления -2 атом серы проявляет в бинарных соединениях с металлами (сульфидах) и водородом (H2S), поэтому правильный ответ CaS и FeS
3. Максимально возможную степень окисления атом хлора проявляет в соединении
1) HCl
2) HClO3
3) KClO4
4) Ba(ClO2)2
Ответ: атом хлора расположен в 7 группе, поэтому может иметь максимальную степень окисления +7. Такую степень окисления атом хлора проявляет в веществе KClO4. Проверим это. У калия степень окисления +1, у кислорода -2, у хлора х. Из уравнения: +1 +х + 4* (-2) = 0 находим х = +7
4. В соединениях NO2 и NH3 степени окисления азота соответственно равны:
1) +4 и -3
2) +2 и +3
3) +2 и -2
4) +5 и +3
Ответ: В оксиде азота (IV) у кислорода степень окисления -2, значит у азота степень окисления +4. В аммиаке у водорода степень окисления +1, значит у азота степень окисления -3.
Как определить степень окисления элемента в ионах? #shorts
5. Установите соответствие между схемами превращения веществ и изменением степени окисления хлора
Схемы превращений Изменение степени окисления хлора A) Cl2 + F2 = ClF3 1) -1 —> +5 Б) Cl2 + I2 = ICl3 2) +2 —> +4 В) ClO2 + H2 = HCl + H2O 3) 0 —> +3 4) 0 —> -1 5) +4 —> -1 6) +4 —> +1
Ответ:
А Б В 3 4 5
В молекуле хлора Cl2 степень окисления хлора равна 0
В молекуле ClF3 у фтора степень окисления -1, значит у хлора +3
В молекуле ICl3 у хлора степень окисления -1
В молекуле ClO2 у кислорода степень окисления -2, значит у хлора +4
В молекуле HCl у водорода +1, а у хлора -1
6. Установите соответствие между схемами превращения веществ и изменением степени окисления серы
Схемы превращений Изменение степени окисления серы A) H2S + O2 = H2O + SO2 1) -2 —> +4 Б) Cl2 + S = S2Cl2 2) +2 —> +4 В) H2SO3 + NO2 = NO + H2SO4 3) 0 —> +4 4) 0 —> +1 5) +4 —> +6 6) -2 —> 0
Ответ:
А Б В 1 4 5
В молекуле сероводорода у водорода степень окисления +1, а у серы -2
В молекуле SO2 у кислорода степень окисления -2, а у серы +4
В молекуле сернистой кислоты у водорода степень окисления +1, у кислорода -2, значит у серы +4
В молекуле серной кислоты у водорода степень окисления +1, у кислорода -2, значит у серы + 6
7. Установите соответствие между схемами превращения веществ и изменением степени окисления азота
Схемы превращений Изменение степени окисления азота A) PH3 + NO = H3PO4 + N2 1) -2 —> +5 Б) P + NO2 = P2O5 + NO 2) +3 —> +5 В) H3PO3 + N2H4 = H3PO2 + N2 + H2O 3) 0 —> +5 4) +2 —> 0 5) +4 —> +2 6) -2 —> 0
Ответ:
А Б В 4 5 6
В молекуле NO степень окисления у кислорода равна -2, а у азота +2
В молекуле азота N2 степень окисления азота равна 0
В молекуле NO2 степень окисления азота равна +4
В молекуле N2H4 степень окисления азота равна -2
8. В каких реакциях железо выступает в роли восстановителя?
1) Fe + S = FeS
2) 2FeCl3 + H2 = 2FeCl2 + 2HCl
3) 2Fe(OH)3 = Fe2O3 + 3H2O
4) 3Fe + 2O2 = Fe3O4
5) 2FeCl2 + Cl2 = 2FeCl3
Ответ: 1, 4, 5 , т.к. в этих реакциях железо отдает электроны и повышает свою степень окисления.
9. В каких реакциях сера не изменяет степень окисления?
10. В каком соединении фосфор проявляет степень окисления -3
1) P2O3
2) Na3PO4
3)Ca3P2
4) PCl3
Ответ: степень окисления -3 фосфор проявляет в бинарных соединениях с металлами, значит в фосфиде кальция Ca3P2 у кальцая степень окисления +2, а у фосфора -3.
- Главная
- Заказать работу
- Онлайн калькулятор стоимости работы
Работы для ВУЗов:
НАШИ УСЛУГИ
- Решение задач по сопромату
- Решение задач по физике
- Решение задач по математике
- Решение задач по химии
- Решение задач по теоретической механике
- Решение задач по теплотехнике
- Решение задач по ТАУ
- Решение задач по материаловедению
- Решение задач по гидравлике
- Решение задач по ТОЭ
- Решение задач по электронике
- Решение задач по теории вероятности
- Решение задач по программированию
- Решение задач по экономике
- Решение задач по БЖД
- Решение задач по метрологии
- Решение задач по статистике
- Решение задач по электроснабжению
- Решение задач и курсовых по электрическим машинам
- Решение задач по бухгалтерскому учету
- Курсовые по деталям машин
- Курсовые по теории машин и механизмов (ТММ)
- Чертежи по инженерной графике
- Курсовые по охране труда
- Решение задач по эконометрике
- Решение задач по строительной механике
- Решение задач по финансовой математике
- Решение задач по информатике
- Курсовые по налогам
- Курсовые по прикладной механике
- Курсовые по менеджменту
Источник: dx-dy.ru
Химия для чайников.
При изучении ионной и ковалентной полярной химической связи вы знакомились со сложными веществами, состоящими из двух химических элементов. Такие вещества называют би парными (от лат. би — «два») или двухэлементными.
Вспомним типичные бпнарные соединения, которые мы привели в качестве примера для рассмотрения механизмов образования ионной и ковалентноЙ полярной химической связи: NaHl — хлорид натрия и НСl — хлороводород. В первом случае связь ионная: атом натрия передал свой внешний электрон атому хлора и превратился при этом в ион с зарядом -1. а атом хлора принял электрон и превратился в ион с зарядом -1. Схематически процесс превращения атомов в ионы можно изобразить так:
В молекуле же НСl связь образуется за счет спаривания не-спаренных внешних электронов и образования общей электронной пары атомов водорода и хлора.
Правильнее представлять образование ковалентной связи в молекуле хлороводорода как перекрывание одноэлектронного s-облака атома водорода с одноэлектронным p-облаком атома хлора:
При химическом взаимодействии общая электронная пара смещена в сторону более электроотрицательного атома хлора:
Такие условные заряды называются степенью окисления. При определении этого понятия условно предполагают, что в ковалентных полярных соединениях связующие электроны полностью перешли к более электроотрицательному атому, а потому соединения состоят только из положительно и отрицательно заряженных ионов.
Степень окисления — это условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что все соединения (и ионные, и ковалентно-полярные) состоят только из ионов.
Степень окисления может иметь отрицательное, положительное или нулевое значения, которые обычно ставятся над символом элемента сверху, например:
Отрицательное значение степени окисления имеют те атомы, которые приняли электроны от других атомов пли к которым смещены общие электронные пары, то есть атомы более электроотрицательных элементов. Фтор всегда имеет степень окисления -1 во всех соединениях. Кислород, второй после фтора по значению элекгроотрицательности элемент, почти всегда имеет степень окисления -2, кроме соединений со фтором, например:
Положительное значение степени окисления имеют те атомы, которые отдают свои электроны другим атомам или от которых оттянуты общие электронные пары, то есть атомы менее электроотрицательных элементов. Металлы всегда имеют положительную степень окисления. У металлов главных подгрупп:
I группы во всех соединениях степень окисления равна +1,
II группы равна +2. III группы — +3, например:
В соединениях суммарная степень окисления всегда равна нулю. Зная это и степень окисления одного из элементов, всегда можно найти степень окисления другого элемента по формуле бинарного соединения. Например, найдем степень окисления хлора в соединении Сl2О2. Обозначим степень окисления -2
кислорода: Сl2О2. Следовательно, семь атомов кислорода будут иметь общий отрицательный заряд (-2) • 7 =14. Тогда общий заряд двух атомов хлора будет равен +14, а одного атома хлора:
(+14):2 = +7.
Аналогично, зная степени окисления элементов, можно составить формулу соединения, например карбида алюминия (соединения алюминия и углерода). Запишем знаки алюминия н углерода рядом АlС, причем сначала знак алюминия, так как это металл. Определим по таблице элементов Менделеева число внешних электронов: у Аl — 3 электрона, у С — 4. Атом алюминия отдаст свои 3 внешних электрона углероду и получит при этом степень окисления +3, равную заряду иона. Атом углерода, наоборот, примет недостающие до «заветной восьмерки» 4 электрона и получит при этом степень окисления -4.
Запишем эти значения в формулу: АlС, и найдем наименьшее общее кратное для них, оно равно 12. Затем рассчитаем индексы:
Знать степени окисления элементов необходимо и для того, чтобы уметь правильно называть химическое соединение.
Названия бинарных соединений состоят из двух слов — названий образующих их химических элементов. Первое слово обозначает электроотрицательную часть соединения — неметалл, его латинское название с суффиксом -ид стоит всегда в именительном падеже. Второе слово обозначает электроположительную часть — металл или менее электроотрицательный элемент, его название всегда стоит в родительном падеже. Если же электроположительный элемент проявляет разные степени окисления, то это отражают в названии, обозначив степень окисления римской цифрой, которая ставится в конце.
Чтобы химики разных стран понимали друг друга, потребовалось создание единой терминологии и номенклатуры веществ. Принципы химической номенклатуры были впервые разработаны французскими химиками А. Лавуазье, А.Фурктуа, Л.Гитоном и К.Бертолле в 1785г. В настоящее время Международный союз теоретической и прикладной химии (ИЮПАК) координирует деятельность ученых рядных стран и издает рекомендации по номенклятурс веществ и терминологии, используемой к химии.
Источник: chemistrykz.blogspot.com
Готовимся к углубленному изучению химии
Степень окисления- это условный заряд атомов химического элемента в соединении, вычисленный из предположения, что соединения состоят только из ионов.
Степени окисления могут иметь положительное, отрицательное или нулевое значение, причём знак ставится перед числом:-1, -2, +3, в отличии от заряда иона, где знак ставится после числа.
В молекулах алгебраическая сумма степеней окисления элементов с учётом числа их атомов равна 0.


1.Элемент в простом веществе имеет нулевую степень окисления;
2.Все металлы имеют положительную степень окисления;
3.Бор и кремний в соединениях имеют положительные степени окисления;
4.Водород имеет в соединениях степень окисления (+1).Исключая гидриды( соединения водорода с металлами главной подгруппы первой-второй групп, степень окисления -1, например Na + H — );
5.Кислород имеет степень окисления (-2),за исключением соединения кислорода со фтором O +2 F — 2 и в перекисях( Н2О2- степень окисления кислорода (-1);
6.Фтор имеет степень окисления (-1)
Степени окисления
Элементы
Li, Na, K, Rb, Cs, Ag, H (кроме гидридов)
Be, Mg, Ca, Sr, Zn, Cd, Ba
-в соединениях с водородом и металлами
— Процесс отдачи электронов атомом, называется окислением.
— Атом, отдающий электроны и повышающий свою степень окисления, окисляется и называется восстановителем.
— Процесс принятия электронов атомом, называется восстановлением.
— Атом, принимающий электроны и понижающий свою степень окисления, восстанавливается и называется окислителем.
Правила определения степени окисления атома в соединении:
I. Степень окисления свободных атомов и атомов в молекулах простых веществ равна нулю — Na 0 , P 4 0 , O 2 0
II. В сложном веществе алгебраическая сумма СО всех атомов с учётом их индексов равна нулю = 0, а в сложном ионе его заряду.
Например, H +1 N +5 O 3 -2 : (+1)*1+(+5)*1+(-2)*3 = 0
[S +6 O4 -2 ] 2- : (+6)*1+(-2)*4 = -2


SHAPE * MERGEFORMAT

УПРАЖНЕНИЯ
1. Определить степени окисления в соединении K2Cr2O 7 .
Решение : У двух химических элементов калия и кислорода степени окисления постоянны и равны соответственно +1 и -2. Число степеней окисления у кислорода равна (-2)·7=(-14), у калия (+1)·2=(+2). Число положительных степеней окисления равно числу отрицательных. Следовательно (-14)+(+2)=(-12). Значит у атома хрома число положительных степеней равно 12, но атомов 2, значит на один атом приходится (+12):2=(+6), записываем степени окисленя над элементами К + 2Cr +6 2O -2 7
_____________________________________________________________
2. Необходимо найти степени окисления элементов в аммиаке (NH3).
Решение : Мы уже знаем (см. 2), что ст. ок. водорода равна +1. Осталось найти эту характеристику для азота. Пусть х — искомая степень окисления. Составляем простейшее уравнение: х + 3*(+1) = 0. Решение очевидно: х = -3. Ответ: N -3 H3 +1 .
_____________________________________________________________
3. Укажите степени окисления всех атомов в молекуле H2SO4.
Решение : Степени окисления водорода и кислорода уже известны: H(+1) и O(-2). Составляем уравнение для определения степени окисления серы: 2*(+1) + х + 4*(-2) = 0. Решая данное уравнение, находим: х = +6. Ответ: H +1 2S +6 O -2 4.
_____________________________________________________________
4. Определите степени окисления всех элементов в (NH4)2SO4.
Решение : Степени окисления водорода и кислорода известны, серы и азота — нет. Классический пример задачи с двумя неизвестными! Будем рассматривать сульфат аммония не как единую «молекулу», а как объединение двух ионов: NH4 + и SO4 2- . Заряды ионов нам известны, в каждом из них содержится лишь один атом с неизвестной степенью окисления. Пользуясь опытом, приобретенным при решении предыдущих задач, легко находим степени окисления азота и серы. Ответ: (N -3 H4 +1 )2S +6 O4 -2 .
Вывод: если в молекуле содержится несколько атомов с неизвестными степенями окисления, попробуйте «разделить» молекулу на несколько частей.
_____________________________________________________________
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
1. Рассчитайте степени окисления всех элементов в молекуле Al(NO3)3.
2. Определите степени окисления всех атомов в ионе (AsO4) 3- .
3.
Определите степени окисления всех атомов в формуле фосфорной кислоты H 3 PO 4.
4. Определите степени окисления всех атомов в формуле иона аммония ( NH 4 ) + .
5. Определите степени окисления атомов в формулах веществ:
Br2, CaO , SiO2, H2CO3 , CuO , Cu2O , Н 2 , KNO3 , FeO , Fe , Fe2O3, Fe(OH)2, Fe2(SO4)3, N2, HClO4
6. Рассчитать степень окисления фосфора в ортофосфате кальция Са3(РО4)2.
7. Определим степень окисления элементов в соединениях: Мg2Р2О7, Fe2(SO4)3, Н3РО4, НСl, НСlO.
8. Какие степени окисления называются промежуточными.
9. Определите степени окисления и валентности:

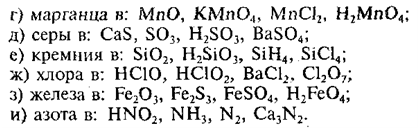
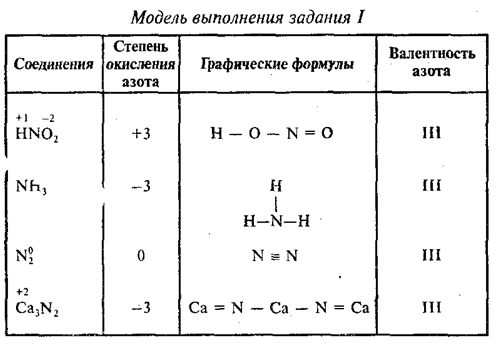
10. Чему равны высшие и низшие степени окисления следующих элементов:
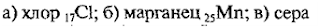
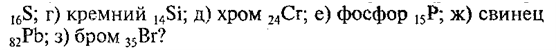
SHAPE * MERGEFORMAT
1. В каком соединении степень окисления Mn максимальна:
а) Mn О3
б) Н2 Mn О3
в) Na2MnO4
г) KMnO4
2. Укажите химические знаки элементов с переменной степенью окисления в соединениях:
г) F
3. Укажите формулы веществ, в которых степень окисления атома углерода равна -4:
а) СаС2
г) CO2
4. Отметьте формулы соединений с одинаковой степенью окисления азота:
а) Mg3N2
б) (NH4)2SO4
в) NH3
г) все ответы верны
5. Укажите формулы соединений, в которых степень окисления водорода равна +1:
а) все ответы верны
б) NH3
в) СН4
6. Отметьте формулы ионов, содержащих атомы со степенью окисления +4:
а) НСО3 —
б) Р2О7 4-
в) MnO 4 —
г) SiO3 —
7. Чему равна соответственно валентность и степень окисления атомов кислорода в молекуле СО:
а) II и -2
б) III и +2
в) III и -2
г) II и +2
8. В какой из молекул, формулы которых приведены ниже, есть две неподеленные пары валентных электронов:
Источник: himiy88.blogspot.com