1.1.2 С помощью сильного окислителя – концентрированной азотной кислоты – концевые группы альдоз (альдегидная и первичноспиртовая) одновременно окисляются в карбоксильные группы, образуя гликаровые кислоты (называемые также сахарными):
Получающаяся из D -галактозы галактаровая (слизевая) кислота трудно растворима в воде, что используется для обнаружения галактозы методом окисления ее азотной кислотой.
1.1.3 Избирательное окисление первичной спиртовой группы, если предварительно защитить склонную к окислению альдегидную группу (например, превращением альдозы в гликозид), то становится возможным избирательное окисление первичной спиртовой группы и образуются гликуроновые (уроновые) кислоты:
Уроновые кислоты при нагревании их солей с металлами (никель, магний) подвергаются декарбоксилированию. При этом из гексуроновых кислот образуются пентозы. В организме за счет ферментативной реакции декарбоксилирования D- глюкуроновой кислоты получается D- ксилоза:
Приведенная реакция показывает генетическую связь пентоз с гексозами, являющимися продуктами фотосинтеза. Пектиновые вещества плодов и ягод представляют собой продукты поликонденсации D- галактуроновой кислоты. Уроновые кислоты выполняют в организме важную функцию – они образуют с лекарственными веществами, их метаболитами, токсичными веществами водорастворимые гликозиды и выводят их из организма.
1.1.4 Окисление кетоз. Кетозы не окисляются слабыми окислителями. При действии сильных окислителей происходит расщепление молекул. Так, например, при окислении фруктозы получаются винная и щавелевая кислоты:
1.1.5 Реакция Толленса. Слабые окислители в щелочной среде (аммиачный раствор оксида серебра, соединения Сu 2+ ) превращают монозы в сложную смесь продуктов окисления и служат для качественного и количественного определения альдоз и кетоз. Подобно обычным альдегидам, альдозы легко дают реакцию “серебряного зеркала” с аммиачным раствором оксида серебра (реактив Толленса):
1.1.6 Окисление реактивом Фелинга. При нагревании реактива Фелинга (смесь равных обьемов водного раствора сульфата меди и щелочного раствора натрий-калиевой соли винной кислоты) в присутствии альдозы выпадает красный осадок Сu2О. Реакцию используют для количественного определения сахаров:
Кетозы тоже способны восстанавливать катионы металлов, так как они в щелочной среде изомеризуются в альдозы.
1.2 Восстановление. При восстановлении моноз образуются многоатомные спирты, называемые альдитами (глицитами). Эти кристаллические, легко растворимые в воде вещества обладают сладким вкусом и часто используются как заменители сахара (ксилит, сорбит):
Восстановление моносахаридов проводят водородом в присутствии металлических катализаторов (Pd, Ni). Шестиатомные спирты – глюцит (сорбит), дульцит и маннит – получаются при восстановлении соответственно глюкозы, галактозы и маннозы. Восстановление глюкозы в сорбит является одной из стадий промышленного синтеза аскорбиновой кислоты. При восстановлении альдоз получается лишь один полиол, кетоз – смесь двух полиолов. Например, при восстановлении D- фруктозы борогидридом натрия NaBН4 образуются D- глюцит (сорбит) и D- маннит:
| D -фруктоза | D -глюцит | D -маннит |
1.3 Присоединение синильной кислоты. Монозы присоединяют синильную кислоту, образуя нитрилы высших глюконовых кислот (Килиани, 1887):
Этим методом можно удлинять углеродную цепь и переходить от низших моносахаридов к высшим (см. способы получения моноз).
1.4 Действие гидроксиламина. Реакция с гидроксиламином используется для установления строения сахаров и для перехода от высших моносахаридов к низшим:
1.5 Действие фенилгидразина. Одной из наиболее важных реакций, которая позволяет выделять в чистом виде отдельные монозы, а также устанавливать тождество моноз различного происхождения, является взаимодействие моноз с фенилгидразином. Сначала фенилгидразин действует на монозы так же, как на простейшие альдегиды и кетоны, т. е. с выделением воды и образованием фенилгидразона:
Затем при нагревании полученного гидразона с фенилгидразином соседняя с карбонильной группой первичная или вторичная спиртовая группа окисляется в карбонильную, причем фенилгидразин восстанав-ливается до анилина и аммиака. Вновь образовавшаяся карбонильная группа (для кетоз – альдегидная, а для альдоз – кетонная) вступает в реакцию с третьей молекулой фенилгидразина и получается озазон монозы:
Из альдоз и кетоз могут получиться озазоны одинакового строения. Поскольку реакция образования озазона затрагивает только углероды С1 и С2 моносахаридов, то, следовательно, эпимерные альдозы и изомерные им кетозы дают один и тот же озазон. Озазоны представляют собой кристаллические вещества, трудно растворимые в воде, благодаря чему их легко выделить в кристаллическом виде из водных растворов моноз:
Озазоны при действии кислот гидролизуются в озоны:
При восстановлении озонов амальгамой натрия в слабокислой среде происходит избирательное восстановление альдегидной группы до первичной спиртовой группы. Этим методом можно осуществлять переход от альдоз к кетозам через озазоны и озоны:
| озон | кетогексоза |
1.6 Действие щелочей. В разбавленных растворах щелочей при комнатной температуре происходит изомеризация моносахаридов, т. е. получение из одного моносахарида равновесной смеси моноз, отличающихся конфигурацией первого и второго атомов углерода. Процесс изомеризации проходит через стадию образования промежуточного продукта – ендиола, который для глюкозы, маннозы и фруктозы является общим:
Происходящие при этих превращениях изменения конфигурации у второго углеродного атома альдоз носит название эпимеризации, а альдозы, отличающиеся лишь конфигурацией второго углеродного атома, называются эпимерами.
Способностью альдоз и кетоз к взаимному переходу друг в друга в слабощелочной среде обьясняются некоторые необычные свойства фруктозы, в частности – способность к положительным реакциям с реактивом Толленса и фелинговой жидкостью.
Превращение 6-фосфата- D- глюкопиранозы в 6-фосфат- D -фруктозы протекает в организме под действием фермента фосфоглюкоизомеразы и является одной из стадий катаболизма глюкозы.
Гидроксилы отличаются по реакционной способности: при С1 –гликозидный (наиболее реакционноспособный); при С6 – первичный; при С2-С4 – вторичные.
В зависимости от размера оксидного цикла гликозиды делятся на пиранозиды и фуранозиды. Ацетали глюкозы называют глюкозидами, рибозы – рибозидами, фруктозы – фруктозидами и т.п. (окончание «оза» монозы заменяется на «озид»). Растворы гликозидов не мутаротируют.
Удобным способом получения гликозидов является пропускание газообразного хлороводорода (катализатор) через раствор моносахарида в спиртах, например, этаноле, метаноле и т. д. При этом соответственно получаются этил- или метилгликозиды. В названии гликозидов указываются сначала наименования введенного радикала, затем конфигурация аномерного центра и название углеводного остатка с суффиксом «озид».
Вследствие таутомерии и обратимости реакции образования гликозида в растворе в равновесии в общем случае могут находиться таутомерные формы исходного моносахарида и соответственно 4 диастереомерных гликозида (a- и b- аномеры фуранозидов и пиранозидов).
Гликозиды легко гидрализуются разбавленными кислотами, но проявляют устойчивость к гидролизу в слабощелочной среде. Более напряженные пятичленные циклы фуранозидов расщепляются гидролитическим путем быстрее пиранозидов. Гидролиз гликозидов в кислой среде приводит к соответствующим спиртам и моносахаридам и представляет собой реакцию, обратную их образованию.
Для гидролитического расщепления гликозидов широко применяется ферментативный гидролиз, преимущество которого заключается в его специфичности. Например, фермент a- глюкозидаза из дрожжей расщепляет только a- глюкозидную связь. На этом основании ферментативный гидролиз часто применяется в целях установления конфигурации аномерного атома углерода. Гидролиз гликозидов лежит в основе гидролитического расщепления полисахаридов, осуществляемого в организме, а также используется во многих промышленных процессах.
Молекулу гликозида формально можно представить состоящей из двух частей – углеводной и агликоновой. В роли гидроксилсодержащих агликонов могут выступать и сами моносахариды. Гликозиды, образованные с ОН- содержащими агликонами, называют О- гликозидами. В свою очередь гликозиды, образованные с NH- содержащими соединениями (например, аминами), называют N- гликозидами. К ним принадлежат нуклеозиды, имеющие важное значение в химии нуклеиновых кислот.
Источник: studopedia.org
XIII Международная студенческая научная конференция Студенческий научный форум — 2021


Этот элемент является важной частью синтеза энергии в нашем организме. Рибоза входит в состав нашего генетического материала, а именно ДНК и РНК.
Еще одна важная функция рибозы-метаболизм клеток. Синтез АТФ способствует обеспечению энергией клеток организма.Чем больше рибозы, тем больше синтезируется АТФ и тем лучше мы себя чувствуем. АТФ обеспечивает высокое кровообращение и повышает мышечный тонус.
Рибоза содержится практически во всех продуктах питания. А особенно в говядине, рыбе, молочных продуктах, в мясе птицы.
Рисунок 3 Синтез цуринов и пиримидинов
Рибоза регулирует процессы синтезирования пуринов и пиримидинов:
Можно выделить следующие физические свойства рибозы: лёгкая растворимость и сладкий вкус
Рибоза представляет собой мелкие белые кристаллики , не имеющие запаха.
Рисунок 4 Получение рибозы
Её получают гидролизом мононуклеотидов:
Из химических свойств можно выделить следующие:
1)Рибоза как представитель моносахаридов может вступать в реакцию по альдегидной группе с аммиачным раствором оксида серебра (реакция «серебряного зеркала»).
2)Окисляется гидроксидом меди Cu ( OH )2.
3)Карбонильная группа восстанавливается в спиртовую.
4)Способность вступать в такие же реакции , как и спирты.
5)Реакция полуацетального гидроксила.
Рибоза используется как пищевая добавка, входящая в состав витаминов. Принимают при хронической усталости, улучшения состояния сердечно сосудистой системы, а так же для восстановления мышц.
Но принимать рибозы без рекомендации врача не стоит. Это влечёт за собой негативные последствия и побочные эффекты препарата. Особенно, если человек страдает заболеваниями сердца и диабетом.
Таким образом, рибоза необходима нашему организму во многих аспектах. От построения ДНК-цепей до синтезирования энергии. Без рибозы наши клетки перестанут делиться и образовывать новые ткани, а мы будем чувствовать усталость и апатию.
Источник: scienceforum.ru
Структура моносахаридов
Для изображения строения моносахаридов используют проекционные формулы Фишера. В формулах Фишера цепь углеродных атомов располагается в одну линию. Нумерация цепи начинается с атома углерода альдегидной группы (в случае альдоз) или с крайнего атома углерода, к которому ближе располагается кетогруппа (в случае кетоз). Атомы водорода и группы –ОН у асимметрических атомов «С» располагаются слева и справа от углеродной цепи.
В зависимости от пространственного расположения атомов «Н» и ОН-групп у 4-го атома углерода у пентоз и 5-го атома углерода у гексоз моносахариды относят к D- или L-ряду.
Моносахарид относят к D-ряду, если ОН-группа у этих атомов располагается справа от цепи:
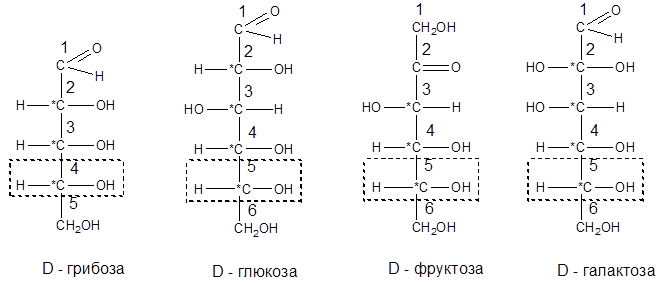
Рассмотренные выше структуры моносахаридов являются ациклическими. Однако моносахариды могут существовать также в циклических формах. Циклические формы образуются в результате взаимодействия карбонильной группы и одной из гидроксильных групп с образованием внутренних полуацеталей.
Альдегидная или кетонная группа гексоз и пентоз взаимодействует с гидроксильными группами у С-4 или С-5. В результате образуются пяти- или шестичленные циклы. Эти циклы структурно аналогичны кислородосодержащим гетероциклам пирану и фурану:
Поэтому циклические формы гексоз и пентоз соответственно называются пиранозными и фуранозными.
В растворах моносахаридов происходит миграция протона между гидроксо- и карбонильной группой, при этом устанавливается подвижное равновесие между ациклической и циклической формами.
Подвижное равновесие между взаимопревращающимися структурными изомерами (таутомерами) называется таутомерией.
Циклические формы принято изображать перспективными формулами Хеуо́рса.
Для перехода от формул Фишера к формулам Хеуорса нужно знать следующие правила:
1. Изображаем цикл в виде плоского многоугольника (при этом цикл находится в плоскости, перпендикулярной плоскости изображения). Нумерацию атомов углерода в цикле производим по часовой стрелке. (Символы атомов углерода обычно не записываются).
2. Атомы и группы атомов, которые в формуле Фишера находятся справа от цепи, в формуле Хеуорса располагаются под плоскостью цикла, и наоборот. Исключение составляет группа -СН2ОН у 5-го атома углерода в гексозах, которая в случае D-гексоз всегда располагается над плоскостью цикла.
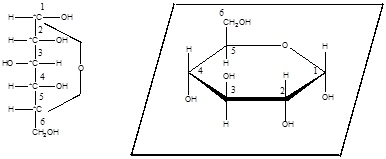

В циклических формах моносахаридов появляется еще один асимметрический атом углерода (С-1 у альдоз и С-2 у кетоз). Этот асимметрический атом углерода называется аномерным. Изомеры углеводов, отличающиеся расположением атомов и атомных групп у аномерного атома углерода, называются аномерами. Стереоизомер (пространственный изомер), в котором группа –ОН у аномерного атома «С» располагается под плоскостью цикла, называется α-аномером, а стереоизомер с противоположным расположением ОН-группы называется β-аномером:
Аномеры не могут непосредственно превращаться друг в друга. Переход от одного аномера к другому возможен только через промежуточное образование ациклической формы моносахарида.
Таким образом, в растворе глюкозы присутствуют различные таутомерные формы, находящиеся в динамическом равновесии:

Важнейшей кетогексозой является D-фруктоза (изомер D-глюкозы). Для циклических форм фруктозы характерны фуранозные структуры. Фуранозный цикл образуется в результате взаимодействия карбонильной (кетонной) группы со спиртовой группой при 5-м углеродном атоме.

Среди пентоз наиболее известны D-рибоза, у которой нет гидроксильной группы при втором углеродном атоме. Эти моносахариды входят в состав рибо- и дезоксирибонуклеиновых кислот (РНК и ДНК) в фуранозной форме.
Моносахариды представляют собой бесцветные кристаллические вещества, сладкие на вкус, хорошо растворимые в воде, нерастворимые в эфире, плохо растворимые в спирте. Сладость моносахаридов различна. Например, фруктоза слаще глюкозы в три раза.
Моносахариды – это соединения со смешанными функциями.
В растворах существует динамическое равновесие между несколькими таутомерными формами моносахаридов, поэтому в зависимости от условий и реагентов они могут реагировать в открытой или циклической форме. При этом равновесие смещается в сторону образования той формы, которая вступает во взаимодействие.
Химические свойства моносахаридов обусловлены наличием:
а) карбонильной группы в открытых формах моносахаридов;
б)спиртовых гидроксильных групп как в открытых, так и в циклических формах моносахаридов;
в) полуацетальной гидроксильной группы в циклических формах моносахаридов.
Рассмотрим химические свойства моносахаридов на примере важнейшего из них – глюкозы.
1. Восстановление (гидрирование) с образованием многоатомного спирта:
 |
В ходе этой реакции карбонильная группа –С– восстанавливается и образуется новая спиртовая группа – ОН.
2. Окисление
Глюкоза легко окисляется. В зависимости от характера окислителей получаются различные продукты.
1) Окисление под действием слабых (мягких) окислителей с образованием глюконовой кислоты.
К числу таких реакций относятся качественные реакции на глюкозу как альдегид: реакции с аммиачным раствором оксида серебра (I) Ag2O (реакция «серебряного зеркала») и реакция с гидроксидом меди (II) Cu(OH)2 в щелочной среде при нагревании:
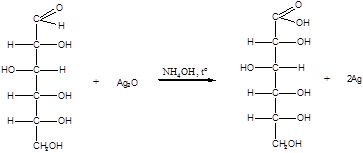
В ходе этих реакций альдегидная группа 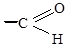 окисляется до карбоксильной группы
окисляется до карбоксильной группы 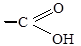 .
.
2) Окисление под действием сильных окислителей (например, азотной кислоты HNO3) c образованием двухосновной глюкаровой кислоты:
В ходе этой реакции и альдегидная группа 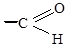 и первичная спиртовая группа – CH2OH окисляется до карбоксильных групп
и первичная спиртовая группа – CH2OH окисляется до карбоксильных групп 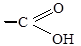 .
.
1. Взаимодействие с Cu(OH)2 на холоду с образованием глюконата меди (II) (качественная реакция на глюкозу как многоатомный спирт):
2. Взаимодействие с ангидридами или галогенангидридами кислот с образованием сложных эфиров:
3. Взаимодействие с галогеналканами с образованием простых эфиров:
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции HI.
4. Взаимодействие со спиртами с образованием гликозидов.
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения. В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы связаны остатки самых различных соединений.
III. Брожение (ферментация) моносахаридов
Брожение – это расщепление моносахаридов под влиянием биологических катализаторов – ферментов, вырабатываемых микроорганизмами. Разные микроорганизмы вызывают различные виды брожения. Название вида брожения определяется названием образующихся продуктов брожения.
Брожение – сложный многостадийный биохимический процесс. Ниже приводятся лишь суммарные уравнения различных типов брожения глюкозы.
1. Спиртовое брожение:
3. Молочнокислое брожение:

Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Прямо сейчас студенты читают про:
Формы защиты прав и законных интересов граждан организаций. Право на судебную защиту. Значение правосудия по гражданским делам ПРЕДМЕТ И СИСТЕМА КУРСА ГРАЖДАНСКОГО ПРОЦЕССУАЛЬНОГО ПРАВА Под формой защиты субъективных прав и охраняемых законом интересов граждан.
Структурные уровни организации материи. Микро-, макро- и мегамиры Материя. структура и системная организация материи. Системная организация как атрибут материи. Структура материи. Структурные уровни.
Полиция: виды, задачи, функции, система органов, организационные основы деятельности Полиция является составной частью довольно обширной системы органов Министерства внутренних дел Российской Федерации.
Формулы конфликтов Три формулы конфликтов (тип А, Б, В) приводит отечественный исследователь в области конфликтологии В.
Выделите в названиях лекарств известные частотные отрезки, объясните их значение. Напишите русское название препарата. № Названия лекарств Частотные отрезки Русское название Aethaper.
Источник: studopedia.ru