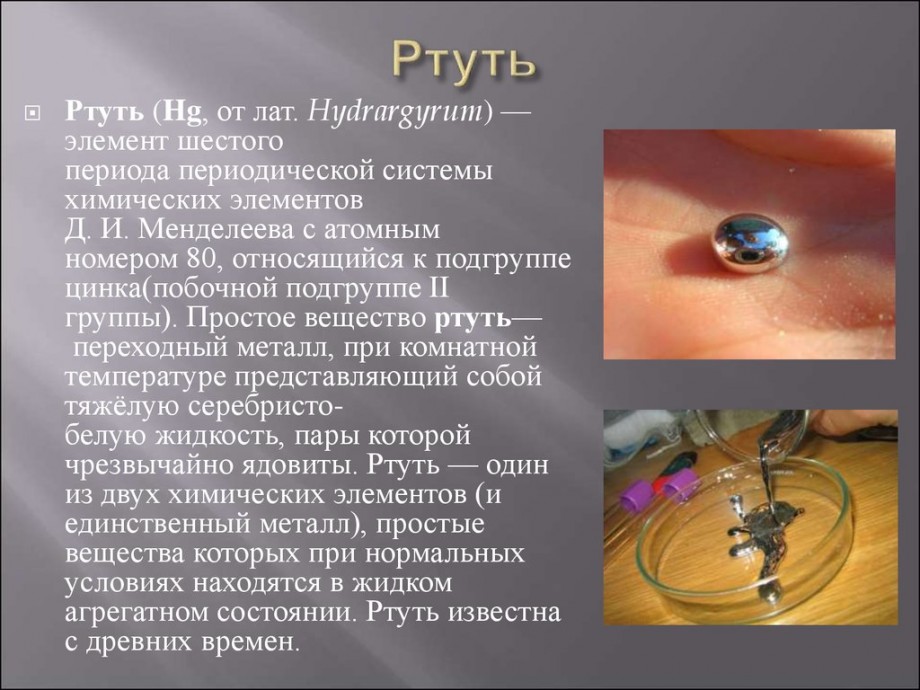
Ртуть (Hg, от лат. Hydrargyrum ) — элемент шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 80, относящийся к подгруппе цинка, 12-й группе (по устаревшей классификации — побочной подгруппе II группы). Простое вещество ртуть — переходный металл, при комнатной температуре представляющий собой тяжёлую серебристо-белую жидкость, пары которой чрезвычайно ядовиты, контаминант. Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии (второй такой элемент — бром).
- 1 История
- 1.1 Происхождение названия
- 2.1 Месторождения и добыча
- 7.1 Характерные степени окисления
- 7.2 Свойства металлической ртути
- 7.2.1 Отношение к простым веществам
- 7.2.2 Отношение к кислотам
- 7.2.3 Отношение к щелочам
- 7.2.4 Окисление ртути
- 7.2.5 Амальгамы
- 8.1 В медицине
- 8.2 В технике
- 8.3 В металлургии
- 8.4 В химической промышленности
- 8.5 В сельском хозяйстве
- 9.1 Гигиеническое нормирование концентраций ртути
- 9.2 Демеркуризация
- 9.3 Запрет использования содержащей ртуть продукции
История
Астрономический символ планеты Меркурий
«Ртуть — Металлическая Стерва»- Академия Сэма О’Нэллы (Озвучка Broccoli)
Ртуть — один из семи металлов, известных с древнейших времён. Нередко её находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом её основного минерала — киновари. Киноварная краска применялась на территории современной Турции с 8 тыс. лет до н. э., киноварные месторождения юго-восточных провинций современного Китая разрабатывались с 4 тыс. лет до н. э. В древнем Египте киноварь и металлическую ртуть использовали с 3-го тысячелетия до н. э., в древней Индии — с 1—2 тысячелетий до н. э. В Египте был найден сосуд с ртутью, датированный XV−XVI веками до н. э. В Египте, Месопотамии и Китае был известен способ получения ртути из киновари при помощи меди и уксуса. В VII веке до н. э. ассирийские ремесленники применяли ртуть для золочения металлических поверхностей (амальгамирование). Aмальгамирование было известно древним грекам и римлянам, они знали и о токсичности самой ртути и её соединений, в частности сулемы. Ртуть и киноварь упоминаются в «Естественной истории» Плиния Старшего. [4] [5] [6]
В надписях во дворце древнеперсидских царей Ахеменидов (VI—IV века до н. э.) в Сузах упоминается, что ртутную киноварь доставляли сюда с Зеравшанских гор и использовали в качестве краски [7] .
На протяжении многих столетий в Европе основным и единственным месторождением ртути был Альмаден в Испании [ источник не указан 3429 дней ] . В Новое время с ним стала конкурировать Идрия во владениях Габсбургов (современная Словения). Там же появилась первая лечебница для поражённых отравлением парами ртути рудокопов.
С XV века ртуть применяется в качестве лекарственного средства, в 1530 году её медицинское применение описал Парацельс. С XVI века ртуть применялась в Мексике для извлечения серебра из руды, а извлечение золота ртутью известно издревле [8] .
Химия. Что же мы знаем про ртуть? / Chemistry. What do we know about mercury?
Составной частью всех металлов ртуть стал считать арабский алхимик Джабир (Гебер) в IX веке [8] . Алхимики вслед полагали, что если жидкой ртути возвратить твёрдость при помощи серы или мышьяка, то получится золото. Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 году. Для представления элемента как у алхимиков, так и в настоящее время используется символ планеты Меркурий : название планеты алхимиками широко использовалось метонимией ртути (иногда как двойной меркурий). Твёрдая ртуть впервые была получена российскими учеными Ломоносовым и Брауном, которые 24 декабря 1759 года благодаря державшимся две недели сорокаградусным морозам [9] смогли заморозить ртуть и установить её металлические свойства в твёрдом состоянии: ковкость, электропроводность и др.; было показано, что ртуть и в жидком, и в твёрдом состоянии проводит электрический ток [10] .
Происхождение названия
Русское название ртути происходит от праслав. *rьtǫtь , связанного с лит. rìsti «катиться» [11] .
В 350 году Аристотель назвал ртуть «жидким серебром» (хютос аргюрон), в I веке н. э. Диоскорид называет её «серебряной водой» (хюдраргюрон). Латинское название hydrargyrum впервые встречается у Плиния, и химический знак Hg происходит от него [12] .
Из-за легкоподвижности капелек ртути на гладкой поверхности алхимики называли её меркурием в честь греко-римского бога Гермеса (Меркурия) — быстро перемещающегося вестника богов [8] .
Нахождение в природе
В разделе не хватает ссылок на источники (см. также рекомендации по поиску).
Информация должна быть проверяема, иначе она может быть удалена. Вы можете отредактировать статью, добавив ссылки на авторитетные источники в виде сносок. Эта отметка установлена 9 февраля 2014 года.
В обычных условиях киноварь и металлическая ртуть не растворимы в воде, но в присутствии некоторых веществ (Fe2(SO4)3, озон, пероксид водорода) растворимость в воде этих минералов достигает десятков мг/л. Особенно хорошо растворяется ртуть в сульфидах щелочных металлов с образованием, например, комплекса HgS•nNa2S. Ртуть легко сорбируется глинами, гидроксидами железа и марганца, глинистыми сланцами и углями [14] .
В природе известно около 20 минералов ртути, но главное промышленное значение имеет киноварь HgS (86,2 % Hg). В редких случаях предметом добычи является самородная ртуть, метациннабарит HgS и блёклая руда — шватцит (до 17 % Hg). На единственном месторождении Гуитцуко (Мексика) главным рудным минералом является ливингстонит HgSb4S7.
В зоне окисления ртутных месторождений образуются вторичные минералы ртути. К ним относятся, прежде всего, самородная ртуть, реже метациннабарит, отличающиеся от таких же первичных минералов большей чистотой состава. Относительно распространена каломель Hg2Cl2. На месторождении Терлингуа (Техас) распространены и другие гипергенные галоидные соединения — терлингуаит Hg2ClO, эглестонит Hg6Cl4O [15] (по другим данным Hg6OCl3(OH) [16] , Hg6HCl3O2 [17] ).
Месторождения и добыча

Словенский город Идрия — крупнейший в Европе центр добычи ртути с XV века
Одно из крупнейших в мире ртутных месторождений находится в Испании (Альмаден), которое наряду с рудниками Словении (Идрия), Италии, США и Мексике было закрыто из-за выработки или падения цен на ртуть. Цены на ртуть были весьма волатильны, в 2006 году они составляли $650 за стандартную в индустрии упаковку 76 фунтов (34 кг) [21] . В 2012 году ЮНЕСКО объявило промышленную инфраструктуру Альмадена и Идрии памятником Всемирного наследия человечества [22] .
Китай является крупнейшим в мире производителем ртути, на долю него в 2012 году приходилось более 72 % мирового объёма производства. Другими крупнейшими производителями ртути являются Кыргызстан, Чили, Россия и Перу. Наибольшими запасами ртути располагает Мексика [23] .
В Российской Империи добыча киновари в незначительных количествах начата в 1759 году на Ильдикайском месторождении в Забайкалье. В небольших количествах россыпная киноварь добывалась в Приамурье. В XIX веке разрабатывались месторождения Бирксуйского рудного поля (Южная Фергана) и Хпека (Южный Дагестан). В 1887 году вступило в строй Никитовское ртутное месторождение (в Украине), где до 1908 года годовое производство варьировалось в пределах 47,3-615,9 тонн, существенная часть ртути шла на экспорт. К XXI веку добыча руды и производство первичной ртути на Никитовском месторождении прекратились [24] .
К XXI веку в России, согласно Государственному балансу запасов полезных ископаемых, есть 24 месторождения ртутных руд низкого качества, в большинстве своём киноварных с запасами не более 2 тыс. тонн ртути. Четыре сравнительно крупных месторождения — Тамватнейское (14 тыс. т), Западнопалянское (10,1 тыс. т), Чаган- Узунское (14 тыс. т), «Звездочка» (3 тыс. т) [24] .
В бывшем СССР наибольшее производство ртути — в Киргизии (Хайдаркан — Айдаркен), с десятикратным отставанием за ней следует Таджикистан. Незначительные количества ртути получают попутно с цинком в Казахстане [24] .
В окружающей среде
Содержание ртути в ледниках(?) за 270 лет
В разделе не хватает ссылок на источники (см. также рекомендации по поиску).
Информация должна быть проверяема, иначе она может быть удалена. Вы можете отредактировать статью, добавив ссылки на авторитетные источники в виде сносок. Эта отметка установлена 9 февраля 2014 года.
До индустриальной революции осаждение ртути из атмосферы составляло около 4 нанограммов на 1 кубический дециметр льда. Природные источники, такие как вулканы, составляют примерно половину всех выбросов атмосферной ртути. Причиной появления остальной половины является деятельность человека. В ней основную долю составляют выбросы в результате сгорания угля (главным образом в тепловых электростанциях) — 65 %, добыча золота — 11 %, выплавка цветных металлов — 6,8 %, производство цемента — 6,4 %, утилизация мусора — 3 %, производство соды — 3 %, чугуна и стали — 1,4 %, ртути (в основном для батареек) — 1,1 %, остальное — 2 %.
Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1950-е годы [18] , что привело к более чем трём тысячам жертв, которые либо умерли, либо сильно пострадали от болезни Минамата.
Изотопы
Основная статья: Изотопы ртути
Природная ртуть состоит из смеси 7 стабильных изотопов: 196 Hg (распространённость 0,155 %), 198 Hg (10,04 %), 199 Hg (16,94 %), 200 Hg (23,14 %), 201 Hg (13,17 %), 202 Hg (29,74 %), 204 Hg (6,82 %) [25] . Искусственным путём получены радиоактивные изотопы ртути с массовыми числами 171—210 [26] . Из них наиболее устойчива ртуть-194 (период полураспада 444 года).
Прочие радиоактивные изотопы имеют период полураспада менее года.
Получение
[math]ce < HgS + O2 ->Hg + SO2 ^ >[/math] металлотермическим методом [27] : [math]ce < HgS + Fe ->FeS + Hg ^ >[/math] или обжигом киновари с известью [27] : [math]ce < 4HgS + CaO ->4Hg ^ + 3CaS + CaSO4 >[/math]
Метод основан на неустойчивости оксида ртути (II), который при нагревании разлагается. Пары ртути конденсируют и собирают. Этот способ применяли ещё алхимики древности [27] .
Полученная ртуть очень загрязнена. Сначала её фильтрованием через отверстие избавляют от механических примесей, затем мелкими каплями пропускают сквозь колонку, заполненную азотной кислотой, высушивают концентрированной серной кислотой и перегоняют в вакууме [27] .
Источник: xn--h1ajim.xn--p1ai
LiveInternetLiveInternet

В поисках пищи. 07.02.2012 —> Смотрели: 78 (8)
-Музыка
-Поиск по дневнику
-Подписка по e-mail
-Постоянные читатели
-Сообщества
Читатель сообществ (Всего в списке: 2) AbhaziaTrip О_Самом_Интересном
-Статистика
Создан: 21.10.2011
Записей: 5325
Комментариев: 1250
Написано: 11417
Меркурий-металл ртуть, между «живыми» и «мертвыми.» После ртути- радиоактивные элементы.
Меркурий-металл ртуть.Ртуть между «живыми» и «мертвыми.» После ртути радиоактивные элементы.
1.ртуть– химический элемент II группы периодической системы элементов, атомный номер 80, относительная атомная масса 200,6.
Источник http://www.ekowiki.ru/index.php?title=Ртуть
2.Реферат: Ртуть и другие. Действие химических элементов на организм человека
«Накопление химических элементов во внутренних органах человека приводит к развитию различных заболеваний. Из элементов больше всего в организме человека накапливаются кадмий, хром — в почках, медь — в желудочно-кишечном тракте, ртуть — в центральной нервной системе, цинк — в желудке, двигательном аппарате, мышьяк — в почках, печени, легких, сердечно-сосудистой системе, селен — в кишечнике, печени, почках, бериллий — в органах кроветворения, нервной системе. »
Источник http://www.bestreferat.ru/referat-1245.html
3.»Ртуть – один из немногих металлов, крупнейшие месторождения которых находятся на европейском материке. Наиболее крупными месторождениями ртути считаются Альмаден (Испания), Монте-Амьята (Италия) и Идрия (Югославия).»
Источник http://n-t.ru/ri/ps/pb080.htm
4.опасность ртуть разбитый градусник
«Если поступление ртути в организм происходит малыми дозами, но в течение длительного времени, наступает хроническое отравление. Для него характерны прежде всего повышенная утомляемость, слабость, сонливость, апатия, головные боли и головокружения. Как видно, эти симптомы очень легко спутать с проявлением других заболеваний или даже с недостатком витаминов. »
Источник http://www.partnerx.ru/199.html
5.»Ртуть считали основой металлов, близкой к золоту и поэтому называли меркурием (Mercurius), по имени ближайшей к солнцу (золоту) планеты Меркурий. С другой стороны, полагая, что ртуть представляет собой некое состояние серебра, древние люди именовали ее жидким серебром (откуда произошло лат. Hydrargirum). Подвижность ртути вызвала к жизни другое название — живое серебро (лат. Argentum vivum); немецкое слово Quecksilber происходит от нижнесаксонского Quick (живой) и Silber (серебро). Интересно, что болгарское обозначение ртути — «живак» и азербайджанское — «дживя» заимствованы, вероятно, от славян.»
Источник http://chemistry-chemists.com/N1_2012/S1/ChemistryAndChemists_1_2012-S1-8.html
6.»Название этого металла в последние годы чаще всего звучит в тревожном и тревожащем контексте. В подтверждение этого тезиса достаточно перечислить несколько заголовков из «Химии и жизни» семидесятых годов: «Ртуть отравляет воду», «Ртуть и уродства», «Ртутное отравление», «Ртуть всюду». И можно подумать, будто у нее, ртути, нет других свойств и качеств, кроме способности вредить всюду и всем. »
Источник http://xarhive.narod.ru/Online/chem/hg.html
школьникам студентам
Источник: www.liveinternet.ru
Ртуть как химический элемент название

1. Человечество использует ртуть вот уже более 3000 лет.
Ртуть — это удивительный, ни на что не похожий гибрид жидкости и металла, а также элемент с атомным номером 80.
2. Ртуть является одним из немногих химических элементов, обладающих массой интересных свойств и обширной сферой применения людьми за всю историю.
3. Ртуть — очень удивительное вещество, обладающее всеми основными свойствами металлов. Вот только форму предать ему проблематично.
4. Ртуть — единственный металл и второе (наряду с бромом) вещество, которое при комнатной температуре пребывает в жидком состоянии.
5. И металлом ртуть стала только лишь в 1759 году, когда Михаил Ломоносов и Иосиф Браун смогли доказать этот факт.
6. Ртуть — очень тяжелый металл, т. к. обладает огромной плотностью. Например, 1 литр ртути имеет массу около 13,6 килограммов.
7. На это же число плотность ртути выше плотности воды.
8.Впервые вес ртути в 1627 году измерил Роберт Бойль, но его цифры верны и сейчас. 1 литр ртути соответствует примерно 13,6 килограммам.

9.В природе ртуть может встречаться в чистом виде – вкраплениями небольших капель в других породах. Чаще всего ртуть добывали, обжигая ртутный минерал киноварь. Также присутствие ртути можно обнаружить в сульфидных минералах, глинистых сланцах и др.
10.Возможно изготовление сплавов ртути со всеми металлами, кроме железа и платины.

РУДА КИНОВАРЬ
11.Большая часть ртути, используемой людьми, добывается из руды, названной киноварью.
12.Чтобы получить чистую ртуть, киноварь нагревают в потоке воздуха. Кислород в воздухе объединяется с серой в руде, формируя газ двуокиси серы и оставляя ртуть.
13. Твердой ртуть становится только при температуре –39 градусов.
14.А повышение ее до +356 градусов заставляет ртуть закипать и превращаться в ядовитый пар.
15. Благодаря своей токсичности ртуть активно применялась древними химиками для того чтобы извлечь из руды золото, серебро, платину и другие металлы.
16.Такой способ под названием амальгация позже был забыт, к нему вернулись только в XVI столетии. Возможно, благодаря именно ему, добыча золота и серебра колонизаторами Южной Америки в свое время достигла колоссальных размеров.

17. Благодаря отличной электропроводимости ртуть широко применяется при изготовлении осветительных приборов и выключателей.
18. А ртутные соли обладают массой полезных свойств. Так, из хлористой соли делают антисептические средства, из фульмината — взрывчатые боеприпасы.
19. Благодаря своему цвету в античные времена этот металл даже отождествляли с живым серебром, о чем свидетельствует одно из её латинских названий: argentumvivum.
20.И это понятно, ведь находясь в своем естественном состоянии – жидком, она способна «бежать» быстрее воды.

21. Способность ртути равномерно расширяться при нагреве нашла широкое применение в разного рода термометрах.
22. А ранее, несмотря на свою токсичность, ртуть активно применяли лекари древности при лечении всевозможных заболеваний. На ее основе изготавливали медицинские препараты и снадобья для лечения различных кожных заболеваний.
23.Она входила в состав мочегонных и слабительных препаратов, использовалась в стоматологии.
24.А йоги древней Индии, согласно запискам Марко Поло, употребляли напиток на основе серы и ртути, который продлевал им жизнь и давал силы.

25.Также известны случая изготовления китайскими знахарями «пилюлю бессмертия» на основе данного металла.
26.В медицинской практике известны случаи использования ртути и при лечении заворота кишок. По мнению врачей тех времен, благодаря своим физическим свойствам «жидкое серебро» должно было проходить через кишки, распрямляя их. Но указанный способ не прижился, так как он имел весьма плачевные результаты – пациенты погибали от разрыва кишечника. От применения такого ртутного лекарства пришлось отказаться.
27. Особое место в использовании ртути в Средневековье является применение ее в мистических ритуалах. Распыляемый красный порошок киновари, по мнению шаманов и магов, должен был отпугивать злых духов.

28. Но, несмотря на приписываемые полезные свойства, ртуть обладает и разрушительными свойствами на человеческий организм. Так, по мнению ученых, жертвой ртутного «лечения» стал русский царь Иван Грозный. При эксгумации его останков современные специалисты установили, что государь русский умер в результате ртутной интоксикации, полученной им в ходе лечения сифилиса.
29.Губительным стало применение солей ртути и для Средневековых мастеров по изготовлению шляп. Постепенное отравление парами ртути становилось причиной слабоумия, получившего название болезни сумасшедшего шляпника. Этот факт нашел отражение в «Алисе в стране чудес» Льюиса Кэрролла. Автор отлично изобразил этот недуг в образе Сумасшедшего Шляпника.
30.А вот употребление ртути с целью самоубийства как раз наоборот, не увенчивались успехом. Известны факты, когда люди выпивали ее или делали внутривенные ртутные инъекции. И все они остались живыми.
31. Ведь металлическая ртуть не так ядовита, как принято считать. Наиболее опасны пары ртути и её растворимые соединения. Сама же металлическая ртуть не всасывается в желудочно-кишечном тракте и выводится из организма.

32. В древности люди больше полагались на магические свойства этого вещества. Например, жрецы Древнего Египта клали в деревянный или гранитный сосуд несколько граммов ртути и помещали его в горло мумии фараона — они считали, что после смерти это будет оберегать их правителя.
33.Рядовые египтяне также рассчитывали на помощь ртути, нося флакончик с ней в качестве амулета.
34.Многие верили и верят, что ртуть приносит удачу, поэтому и в наши дни талисманы из ртути не редкость.

35. Ртуть применяют для производства краски, которой открашивают корабли. Дело в том, что на подводной части судна могут образовываться колонии бактерий и микроорганизмов, которые разрушают обшивку. Краска на основе ртути препятствует этому разрушительному воздействию.
36. Известно, что ртуть содержится в морской воде. Недавно было установлено, что мелкие рыбы способны накапливать это вещество. При этом хищники, как рыбы, так и птицы, которые охотятся на мелкую рыбу, могут сохранять ртуть в организме в еще более высоких концентрациях. Например, если сельдь содержит 0,01 промилле ртути, то у акулы показатель превышает 1 промилле.
37. Случайно разбившийся градусник требует соблюдения безопасного алгоритма действий. Первое правило — вывести всех из помещения, закрыть дверь, распахнуть окно. Загрязненный парами ртути воздух не распространится по квартире.
38.Сама ликвидация начинается с подтягивания мелких капель друг к другу с помощью бумаги. Мелкие частицы собирают кисточкой, клейкой лентой. Оставшиеся капли втягивают грушей. Все погружают в банку.
39.Вооружившись фонариком, необходимо убедиться в полном отсутствии ртути. Нельзя убирать вещество веником, бытовым пылесосом. За счет нагревания, дробления капель испарение усиливается в сотни раз.
40.После механической уборки провести влажную. Протирать химическими чистящими средствами нельзя: при контакте с ртутью они образуют опасные соединения.

41. Ртуть нельзя перевозить в самолетах. Но не из-за её токсичности как может показаться на первый взгляд. Все дело в том, что ртуть, контактируя с алюминиевыми сплавами, делает их хрупкими. Поэтому, случайно разлив ртуть, можно повредить самолет.
42. В сельском хозяйстве высокотоксичные соединения ртути используют в качестве пестицидов.
43. Сегодня в медицине ртуть можно встретить только лишь в градусниках, измеряющих температуру тела. Но и в этой нише ее постепенно вытесняет электроника.

44. Кстати, наш организм всё-таки «отягощен» ртутью, но её количество ничтожно — 13 миллиграмм.
45. Ранее ртуть даже входила в некоторые препараты «слабительного» действия. Единственный минус такового — если организм «не отдаст свои переработки» будет сильнейшее ртутное отравление.

46. В современном мире ртуть нашла широчайшее применение в электронике, где компоненты на ее основе используются во всевозможных лампах и другой электротехнике.
47.Её применяют в медицине для производства некоторых лекарств.

48.Из ртути возможно выделение кислорода.

49. Ртуть также участвует в переработке нефти. Так, с помощью именно этого металла, можно регулировать оптимальную температуру для процесса, который играет главенствующую роль для нефти.
50. В настоящее время продолжает проводиться большая работа по изучению полезных свойств ртути с последующим её применением в механике и химической промышленности.

фото из интернета
Источник: obshe.net