По активности металлы можно разделить на три группы: активные, средней активности и неактивные. Для определения активности металлов используют ряд активности или ряд напряженности металлов (РНМ). Активными считаются металлы, расположенные в ряду до алюминия (иногда алюминий также относят к активным металлам); металлы средней активности – все металлы от алюминия и до водорода; неактивные металлы стоят в РНМ после водорода.
Активные металлы и металлы средней активности можно также разделить на несколько групп: щелочные, щелочноземельные, амфотерные и переходные.
Щелочные металлы — это элементы главной подгруппы I группы: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs, франций Fr.
Источник: maximumtest.ru
Химический элемент рубидий: характеристики, свойства, соединения

Цезий — самый активный металл на Земле!
В 1861 году недавно изобретенный физический метод исследования веществ – спектральный анализ – еще раз продемонстрировал свое могущество и надежность, как залог большого будущего в науке и технике. С его помощью был открыт уже второй неизвестный ранее химический элемент – рубидий. Затем, с открытием в 1869 году Д. И. Менделеевым периодического закона, рубидий вместе с другими элементами занял свое место в таблице, которая внесла порядок в химическую науку.
Дальнейшее изучение рубидия показало, что этот элемент обладает целым рядом интересных и ценных свойств. Мы рассмотрим здесь наиболее характерные и важные из них.
Общая характеристика химического элемента
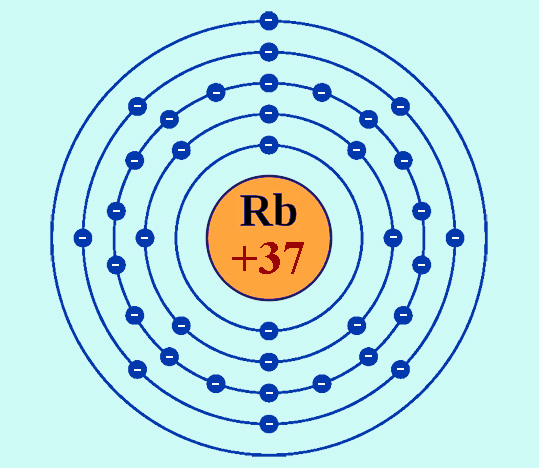
Рубидий имеет атомный номер 37, то есть в атомах его в состав ядер входит именно такое количество положительно заряженных частиц – протонов. Соответственно нейтральный атом обладает 37 электронами.
Символ элемента — Rb. В периодической системе рубидий классифицируется как элемент I группы, период – пятый (в короткопериодном варианте таблицы он относится к главной подгруппе I группы и расположен в шестом ряду). Является щелочным металлом, представляет собой мягкое, очень легкоплавкое кристаллическое вещество серебристо-белого цвета.
История обнаружения
Честь открытия химического элемента рубидий принадлежит двум немецким ученым – химику Роберту Бунзену и физику Густаву Кирхгофу, авторам спектроскопического метода изучения состава вещества. После того, как в 1860 году применение спектрального анализа привело к открытию цезия, ученые продолжили исследования, и уже в следующем году при изучении спектра минерала лепидолита ими были обнаружены две неотождествленные линии темно-красного цвета. Именно благодаря характерному оттенку наиболее сильных спектральных линий, по которым удалось установить существование неизвестного ранее элемента, он и получил свое название: слово rubidus переводится с латыни как «багровый, темно-красный».
Самые опасные щелочные металлы в мире
В 1863 году Бунзен впервые выделил из воды минерального источника металлический рубидий путем упаривания большого количества раствора, разделения солей калия, цезия и рубидия и, наконец, восстановления металла с использованием сажи. Позднее Н. Бекетов сумел восстановить рубидий из его гидроксида с помощью порошка алюминия.
Физическая характеристика элемента
Рубидий – легкий металл, он имеет плотность 1,53 г/см 3 (при нулевой температуре). Образует кристаллы с кубической объемно-центрированной решеткой. Плавится рубидий всего при 39 °C, то есть при комнатной температуре его консистенция уже близка к пастообразной. Металл кипит при 687 °C, пары его имеют зеленовато-синий оттенок.
Рубидий – парамагнетик. По проводимости он более чем в 8 раз превосходит ртуть при 0 °C и почти во столько же раз уступает серебру. Подобно другим щелочным металлам, рубидий отличает очень низкий порог фотоэффекта. Для возбуждения фототока в нем достаточно уже длинноволновых (то есть низкочастотных и несущих меньшую энергию) красных световых лучей. В этом отношении по чувствительности его превосходит лишь цезий.

Изотопы
Рубидий имеет атомный вес 85,468. В природе встречается в виде двух изотопов, различающихся количеством нейтронов в ядре: рубидий-85 составляет наибольшую долю (72,2%), и в значительно меньшем количестве – 27,8% – рубидий-87. Ядра их атомов, помимо 37 протонов, содержат соответственно по 48 и по 50 нейтронов. Более легкий изотоп стабилен, а рубидий-87 имеет огромный по длительности период полураспада – 49 миллиардов лет.
В настоящее время искусственным путем получено несколько десятков радиоактивных изотопов этого химического элемента: от сверхлегкого рубидия-71 до перегруженного нейтронами рубидия-102. Периоды полураспада искусственных изотопов варьируют от нескольких месяцев до 30 наносекунд.

Основные химические свойства
Как было отмечено выше, в ряду химических элементов рубидий (как натрий, калий, литий, цезий и франций) относится к щелочным металлам. Особенность электронной конфигурации их атомов, определяющая химические свойства – это наличие только одного электрона на внешнем энергетическом уровне. Этот электрон легко покидает атом, а ион металла при этом приобретает энергетически выгодную электронную конфигурацию стоящего перед ним в таблице Менделеева инертного элемента. Для рубидия это – конфигурация криптона.
Таким образом, рубидий, как и прочие щелочные металлы, имеет ярко выраженные восстановительные свойства и степень окисления +1. Щелочные свойства сильнее проявляются с увеличением атомного веса, поскольку при этом растет и радиус атома, и, соответственно, ослабляется связь внешнего электрона с ядром, что обусловливает повышение химической активности. Поэтому рубидий активнее лития, натрия и калия, а цезий, в свою очередь, активнее рубидия.
Суммируя все вышесказанное о рубидии, разбор элемента можно произвести, как на иллюстрации, представленной ниже.

Соединения, образуемые рубидием
На воздухе этот металл ввиду своей исключительной реакционной активности окисляется бурно, с воспламенением (пламя имеет фиолетово-розоватый цвет); в ходе реакции образуются надпероксид и пероксид рубидия, проявляющие свойства сильных окислителей:
Оксид образуется в том случае, если доступ кислорода к реакции ограничен:
Это вещество желтого цвета, реагирующее с водой, кислотами и кислотными оксидами. В первом случае образуется одна из наиболее сильных щелочей – гидроксид рубидия, в остальных – соли, например, сульфат рубидия Rb2SO4, большинство которых растворимы.

Еще более бурно, сопровождаясь взрывом (так как мгновенно воспламеняются и рубидий, и освобождаемый водород), протекает реакция металла с водой, в которой образуется гидроксид рубидия, чрезвычайно агрессивное соединение:
Рубидий – химический элемент, способный также непосредственно реагировать со многими неметаллами – с фосфором, водородом, углеродом, кремнием, с галогенами. Галогениды рубидия – RbF, RbCl, RbBr, RbI – хорошо растворимы в воде и в некоторых органических растворителях, например, в этаноле или в муравьиной кислоте. Взаимодействие металла с серой (растирание с серным порошком) происходит взрывообразно и приводит к образованию сульфида.

Существуют и малорастворимые соединения рубидия, такие как перхлорат RbClO4, они находят применение в аналитике для определения этого химического элемента.
Нахождение в природе
В составе полезных ископаемых рубидий повсеместно сопутствует калию. Наибольшей концентрацией рубидия отличаются лепидолиты – минералы, служащие также источником лития и цезия. Так что рубидий в небольших количествах всегда присутствует там, где обнаруживаются другие щелочные металлы.

Немного о применении рубидия
Краткую характеристику хим. элемента рубидия можно дополнить несколькими словами о том, в каких областях используется этот металл и его соединения.
Рубидий находит применение в производстве фотоэлементов, в лазерной технике, входит в состав некоторых специальных сплавов для ракетной техники. В химической промышленности соли рубидия используются благодаря высокой каталитической активности. Один из искусственных изотопов, рубидий-86, применяется в гамма-дефектоскопии и, кроме того, в фармацевтической промышленности для стерилизации лекарственных препаратов.
Еще один изотоп, рубидий-87, используют в геохронологии, где он служит для определения возраста древнейших горных пород благодаря очень большому периоду полураспада (рубидий-стронциевый метод).
Если несколько десятков лет назад считалось, что рубидий – химический элемент, область применения которого едва ли будет расширяться, то в настоящее время для этого металла появляются все новые перспективы, например, в катализе, в высокотемпературных турбоагрегатах, в специальной оптике и в других сферах. Так что в современных технологиях рубидий играет и будет продолжать играть важную роль.
Источник: fb.ru
Ряд активности металлов

Ряд активности металлов это последовательность в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов.
Металлы в ряду активности до водорода (литий Li, рубидий Rb, …, свинец Pb) и металлы в ряду активности после водорода (сурьма Sb, висмут Bi, …, золото Au).
Примером может служить расширенный (полный) ряд активности металлов:

Что такое ряд активности металлов и окислительно-восстановительные реакции
Отправным пунктом при изучении ряда активности металлов следует взять периодическую систему элементов.
Устанавливается, что активность металла определяется степенью лёгкости отдачи атомом электронов: чем легче атомы металла отдают электроны, тем металл является активнее.
Ряд активности металлов показывает их сравнительную активность в реакциях окисления или восстановления (сверху вниз восстановительная активность уменьшается) металл, находящийся в ряду напряжений левее (или выше) водорода, способен вытеснить водород из кислот.
Проверь хорошо ли Вы знаете науки
Ты получил <> снаружи >

О сравнительной активности металлов можно судить по их положению в периодической системе: внутри периодов при передвижении справа налево нарастает активность металлов, и самые активные металлы (литий, натрий, калий, рубидий, цезий и франций) стоят в начале периодов.
Рис. Трубка для опытов по вытеснению металлов водородом под давлением
В главных подгруппах при передвижении сверху вниз тоже нарастает активность металлов, в чём можно убедиться на примере тех же щелочных металлов.
История
Зависимость последовательности расположения металлов была известна с времен алхимиков, так как они с помощью (трансмутации) восстанавливали другие металлы из их растворов ( например медь, серебро).
В 1800 г. Алессандро Вольта сконструировал свой первый генератор электрического тока — «вольтов столб». Это изобретение доставило ему всемирную славу.
Он установил относительную активность: Zn, Pb, Sn, Fe, Cu, Ag, Au, в результате опытов выяснилось, что «сила» гальванического элемента становилась больше, чем дальше стояли друг от друга металлы в этом ряду (ряд напряжений).
В 1798 году Иоганн Вильгельм Риттер высказал гипотезу электрического тока в ряду окисления металлов вследствие протекания химической реакции.
Й. Берцелиус на основе электрохимической теории сродства построил классификацию элементов, разделив их на «металлоиды» (сейчас применяется термин «неметаллы») и «металлы» и поставив между ними водород.
Ряд Бекетова
Если металлы стоят в разных периодах и в разных группах, как, например , цинк и свинец, то на основе положения их в периодической системе быстро и правильно охарактеризовать их сравнительную активность довольно трудно.
Это можно выполнить на основе ряда активности металлов, установленного русским учёным Н. Н. Бекетовым и впервые названного им «вытеснительным рядом металлов».
Наиболее выдающимся трудом Н. Н. Бекетова являются его «Исследования над явлениями вытеснения одних элементов другими» (Харьков, 1865).
Исследования показали, что простые вещества (более легкие), могут вытеснять более тяжелые (отсюда и название вытеснительный ряд Бекетова, или просто ряд Бекетова).
Для наиболее важных металлов ряд активности металлов имеет следующий вид:

1. В этом ряду металлы расположены в определённой системе, а именно в порядке убывающей активности. Из двух металлов, стоящих рядом, легче отдают электроны атомы металла, стоящего левее.
2. Каждый металл этого ряда вытесняет все следующие за ним металлы из растворов их солей, иначе говоря, каждый металл окисляется ионами всех следующих за ним металлов, например :

При этом, как видно из уравнений, металл переходит в состояние иона, а ион — в состояние металла.
3. Если в ряду двигаться слева направо, т. е. от калия к золоту, то способность атомов отдавать электроны будет убывать, т. е. будет убывать восстановительная способность атомов и нарастать окислительная способность ионов металлов.
Таким образом, в приведённом ряду активности металлов атомы калия и натрия являются очень сильными восстановителями, а ионы серебра и золота — сильными окислителями.
4. Как следствие из изложенного вытекает, что водород из разбавленных кислот может вытеснять только металлы, которые в ряду стоят левее его.
Металлы же, стоящие вправо от водорода, наоборот, вытесняются водородом, находящимся под давлением, из растворов их солей умеренных концентраций:
Для определения места водорода в ряду активности металлов Н. Н. Бекетов производил такие опыты:
В колена изогнутой стеклянной трубки (рис.) помещались раздельно соли металла, кислота и цинк. Трубка запаивалась, потом наклонялась так, что цинк падал в кислоту и выделяющийся водород действовал под давлением на раствор соли.
По явлениям, происходящим в колене трубки с раствором соли, можно было судить о том, вытесняется ли металл водородом или нет.
На основании подобных опытов Н. Н. Бекетов пришёл к выводу, что в «вытеснительном ряду» водород должен занимать место после свинца, а за водородом идут медь, ртуть, серебро, золото и платиновые металлы.
5. Из двух металлов, образующих электроды гальванического элемента, отрицательным электродом, катодом, будет тот из них, который стоит левее в ряду, а положительным электродом, анодом, — тот, который стоит правее.
Зависимость окислительно восстановительных реакций в ряду активности металлов
Окислительно-восстановительная реакция в гальваническом элементе протекает тем энергичнее, чем эти металлы дальше отстоят друг от друга в ряду активности металлов.
Следует в заключение подчеркнуть, что ряд активности металлов нельзя рассматривать как абсолютную характеристику свойств металлов, действительную во всех случаях и при всяких условиях.
1) Так, например , в растворах цианистого калия он существенно отличается от обычного ряда, что видно из приводимого ниже сопоставления (при 10°):
а) Обычный ряд: Zn, Fe, Sn, Сu, Ag. Аu;
б) 0,6% раствор KCN: Zn, Сu, Sn, Ag, Аu, Fe;
в) 30% раствор KCN: Zn, Сu, Аu, Ag, Sn, Fe.
При изменившихся условиях активность, например , железа резко снижается, активность меди заметно повышается и т. д.
Пример взаимодействия хлороводорода с серебром
2) Хотя серебро в ряду активности стоит после водорода, но при нагревании металлического серебра в атмосфере хлористого водорода протекает обратимая реакция:
2Ag + 2HCl ⇄ 2AgCl + H2,
причём вытеснение водорода серебром сопровождается выделением тепла.
Если эту реакцию проводить в замкнутом сосуде под атмосферным давлением, то при 600° газовая смесь содержит по объёму 92,8 % НСl и 7,2 Н2, а при 700° соответственно 95% и 5%.
Подобным же образом протекает реакция при тех же условиях и с медью.
Несмотря на свой относительный характер и имеющиеся некоторые исключения, ряд активности металлов всё же очень важен в практическом отношении,
Так как в большинстве случаев он позволяет правильно ориентироваться в направлении окислительно-восстановительной реакции при взаимодействии металла с водным раствором того или иного электролита.
Часто задаваемые вопросы ответы о ряде активности металлов?
Что показывает ряд активности металлов?
Это ряд металлов химическая активность (электрохимический потенциал), которых располагается в порядке увеличения силы
Используется для оценки активности металлов в водных растворах, и для процессов, происходящих при электролизе.
Что такое ряд напряжений металлов?
Электрохимический ряд активности металлов (ряд напряжений, ряд стандартных электродных потенциалов).
Последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ0, отвечающих полуреакции восстановления катиона металла:
Men + : Men + + nē → Me.
Ряд напряжений характеризует сравнительную активность металлов в окислительно-восстановительных реакциях в водных растворах.
Как пользоваться рядом активности металлов?
Это ряд металлов, в котором их химическая активность уменьшается. Это чудесная шпаргалка, которой нужно уметь пользоваться: металлы, которые стоят до водорода, могут вытеснять водород из растворов кислот.
То есть литий Li, рубидий Rb, …, свинец Pb будут вытеснять водород из кислот ( например из школы взаимодействие цинка с серной кислотой при которой выделяется водород).
И металлы которые находятся после водорода (сурьма Sb, висмут Bi, …, золото Au) не выделяют водород из кислот.
Ряд активности металлов или ряд Бекетова используют для предварительного определения химической реакции между металлом и кислотой, которая записывается на бумаге.
Всегда нужно учитывать тот факт, что примеси других элементов ( например платина, золото и т.д.) могут не давать выделения водорода или наоборот.
Статья на тему Ряд активности металлов
- ← Предыдущая
- Следующая →
- Главная реакции восстановления окисления
Похожие страницы:
Вытеснительный ряд металлов Бекетова Рассматривая способы получения водорода, мы уже отмечали, что одни металлы легко вытесняют из воды водород, другие —.
Химические свойства металлов Основным химическим свойством металлов является способность их атомов легко отдавать свои валентные электроны и переходить в положительно.
Атомарный водород это химический элемент который неустойчив почти сразу переходит в обычный водород выделяя при этом некоторую температуру. Даже при.
Водород в природе Водород (Hydrogenium; ат. вес 1,008) в свободном состоянии встречается в природе лишь в незначительных количествах, главным образом.
Соединения фосфора с водородом и галогенами С водородом фосфор образует три соединения: РН3 — газообразный фосфористый водород, Р2Н4 — жидкий фосфористый.
Разложение пероксида водорода это процесс разделения молекулы пероксида водорода на воду и кислород, так как концентрированная перекись непрочное соединение, уже.
Понравилась статья поделись ей
Источник: znaesh-kak.com