в) Глюкоза, будучи не только альдегидом, но и многоатомным спиртом, реагирует с Cu(OH)₂ с образованием ярко-синего осадка:
| |
H — C — O — H H — C — O
| + Cu(OH)₂ ⇒ | >Cu²⁺ + 2 OH⁻
H — С — O — H H — С — O
| |
При нагревании образуется кирпично-красный осадок Cu₂O за счет окисления альдегидной группы:
t
— CHO + 2 Cu(OH)₂ > — COOH + Cu₂O↓
Очевидно, альдегид при нагревании также реагирует с Cu(OH)₂ с образованием осадка Cu₂O кирпично-красного цвета.
г) Глюкоза и альдегиды не реагируют непосредственно с щелочью. Однако в щелочной среде альдегиды на реакцию альдольной конденсации — с образованием альдегидоспирта (альдоля):
O O OH O
|| || KOH | ||
С₂H₅ — С — H + С₂H₅ — С — H > С₂H₅ — СH — СH — С — H
|
CH₃
Альдегиды, не имеющие α-водородных атомов, в щелочной среде вступают в реакцию диспропорционирования — реакцию Канниццаро. В этой реакции 2 молекулы альдегида превращаются в 1 молекулу спирта и 1 молекулу карбоновой кислоты:
Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Подготовка к ЕГЭ по Химии
O O O — H
|| KOH || |
2 С₆H₅ — C — H > C₆H₅ — C — O — H + C₆H₅ — С — H
|
H
Глюкоза в щелочном растворе изомеризуется во фруктозу, галактозу и другие моносахариды.
При нагревании в щелочной среде происходит деструкция глюкозы с образованием молочной, муравьиной кислот и других продуктов
д) Глюкоза не реагирует с водой. Альдегиды присоединяют воду с образованием спиртов с двумя гидроксильными группами при одном атоме углерода:
O OH
|| |
H — C — H + H₂O <> H — С — H (метандиол, метиленгликоль)
|
OH
Но это соединение очень неустойчиво и превращается обратно в формальдегид.
Источник: 0tvet.com
Задание с ответами: химия. ЕГЭ — 2018
Из предложенного перечня выберите два утверждения, характерные для глюкозы, в отличие от сахарозы.
1) реагирует с кислородом
2) реагирует с серной кислотой (конц.)
3) восстанавливается водородом
4) окисляется аммиачным раствором оксида серебра
5) реагирует с сульфатом натрия
Запишите в поле ответа номера выбранных утверждений.
Сведения для решения
Глюкоза — это альдегидоспирт, поэтому для нее характерны реакции окисления и присоединения, которые протекают по альдегидной группе. Окисляется глюкоза до глюконовой кислоты, восстанавливается водородом до шестиатомного спирта сорбита.
Как спирт глюкоза вступает в реакции замещения, образует сложные эфиры.
Правильный ответ: 34.
Правильный ответ: 34|43
Источник: vuz-24.ru
Взаимодействие углекислого газа с веществами и его химические свойства


Общие химические свойства углекислого газа: CO2 инертен, то есть химически не активен; при попадании в водный раствор легко вступает в реакции.
Большинство кислотных оксидов устойчивы к высоким температурам, но углекислота при их воздействии восстанавливается.
Взаимодействие с другими веществами:
1) Углекислота относится к кислотным оксидам, то есть в сочетании с водой образуется кислота. Однако угольная кислота неустойчива и распадается сразу. Эта реакция имеет обратимый характер:
Диоксид углерода + вода ↔ угольная кислота
2) При взаимодействии углекислого газа и соединений азота с водородом (аммиаком) в водном растворе происходит разложение до углеаммонийной соли.
Аммиак + углекислота = гидрокарбонат аммония

Полученное вещество часто используется в приготовлении хлеба и различных кондитерских изделий.
3) Ход некоторых реакций должен поддерживаться высокими температурами. Примером является производство мочевины при 130 °C и давлении 200 атм., схематически изображаемое так:
Аммиак + диоксид углерода → карбамид + вода
Также под воздействием температуры около 800 градусов протекает реакция образования оксида цинка:

Цинк + двуокись углерода → оксид цинка + оксид углерода
4) Возможно уравнение с гидроксидом бария, при котором выделяется средняя соль.
Гидроксид бария + углекислота = карбонат бария + оксид водорода.
Применяется для регулировки калориметров по теплоемкости. Также вещество используют в промышленности для производства красных кирпичей, синтетических тканей, фейерверков, гончарных изделий, плитки для ванн и туалетов.
5) Углекислый газ выделяется при реакциях горения.

Метан + кислород = углекислота + вода (в газообразном состоянии) + энергия
Этилен + кислород = диоксид углерода + оксид водорода + энергия
Этан + кислород = двуокись углерода + вода + энергия
Этанол + кислород = вода + углекислота + энергия
6) Газ не поддерживает горения, этот процесс возможен только с некоторыми активными металлами, например, магнием.
Магний + углекислота = углерод + оксид магния.
MgO активно применяется при производстве косметических средств. Вещество используют в пищевой промышленности как пищевую добавку.
7) Двуокись углерода реагирует с гидроксидами с получением солей, которые существуют в двух формах, как карбонаты и бикарбонаты. Например, углекислый газ и гидроксид натрия, согласно формуле, образуют гидрокарбонат Na:
диоксид углерода + гидроксид натрия → гидрокарбонат натрия.
Или же при большем количестве NaOH образуется карбонат Na с образованием воды:
Диоксид углерода + гидроксид натрия → карбонат натрия + вода
Кислотно-щелочные реакции углекислоты используются на протяжении веков для затвердевания известкового раствора, что может быть выражено простым уравнением:
Гидроксид кальция + двуокись углерода → карбонат кальция + оксид водорода

В зелёных растениях играет важную роль в процессе фотосинтеза:
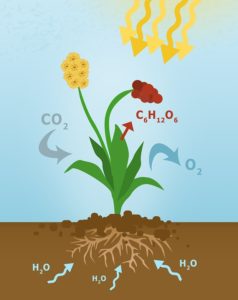
Диоксид углерода + вода → глюкоза + кислород.
9) Химические свойства углекислоты используются в промышленности при производстве соды, суть этого процесса можно выразить суммарным уравнением:
Хлорид натрия + Диоксид углерода + аммиак + вода → гидрокарбонат натрия + хлорид аммония
10) Фенолят Na разлагается при взаимодействии с углекислым газом, при этом малорастворимый фенол выпадает в осадок:
Фенолят натрия + двуокись углерода + оксид водорода = фенол + гидрокарбонат натрия
11) Пероксид натрия и углекислый газ, взаимодействуя, образуют среднюю соль карбоната Na с выделением кислорода.
Пероксид натрия + углекислота → карбонат натрия + кислород

Образование углекислоты происходит при растворении в воде кальцинированной соды (стиральной соды).
Гидрокарбонат натрия + вода → углекислота + вода + гидроксид натрия
При этой реакции (гидролиз по катиону) образуется сильнощелочная среда.
12) CO2 вступает в реакцию с гидроксидом калия, последний образуется путем электролиза хлористого калия.
Гидроксид калия + углекислота → карбонат калия + вода
13) Газ в силу своего строения не реагирует с благородными газами, то есть гелием, неоном, аргоном, криптоном, ксеноном, радоном, оганесоном.