Серебро является довольно популярным металлом как в быту, так и в промышленности. Розовое и самородное, матовое и другие виды серебра имеют свои особенности. Что это такое? Где применяется серебро?
Характеристики и свойства серебра как металла
Серебро — металл, который известен людям с древних времен. Археологи находили предметы из этого металла, которым уже более 6 тысяч лет. К тому же доказано, что самые первые в истории монеты были созданы именно из сплава серебра и золота. Латинское название этого металла argentum. Слово это означает «блестящий, белый».
Характеристики элемента
Серебро имеет сходство с палладием. Кстати, в периодической схеме он стоит следующим после него. А вот с рубидием у него меньше похожих свойств, несмотря на общий период. Это связано с тем, что они в разной степени заполнены электронами. Кроме того, по многим физическим и химическим свойствам серебро схоже с медью и золотом. В группе меди этот элемент имеет самые низкие температуры плавления и кипения. Кроме того, в данной группе у него наибольшие показатели электро- и теплопроводности. Свойства элемента во многом зависят от того, насколько чистый вид он имеет.
Как СЕРЕБРО Обгонит ЗОЛОТО? | Секрет Уоренна Баффетта
Распространение в природе
Серебро считают достаточно редким металлом, который находят в земной коре. Этот элемент встречается и самостоятельно, в качестве самородка, и в форме различных соединений. Примерами могут быть селенаты, сульфиды, галогениды и теллураты в составе различных минералов. Кроме того, достаточно часто серебро обнаруживают в метеоритах. Как ни странно, но оно входит в состав морской воды. Серебро в форме самородка — большая редкость. Намного чаще можно обнаружить медную и золотую руду, которая содержит в себе соединения серебра.
Самородное серебро формируется за счет того, что вода воздействует на сульфид натрия. То же касается и влияния водорода на это соединение. Металлический вид серебра — это кристаллы с гранями, имеющие беловатый оттенок, который чаще всего имеет черное покрытие (налет). Самородное серебро можно обнаружить в России, Канаде, Германии, Норвегии, Чили.
Различают минералы серебра. К примеру, кантпит имеет ромбическую структуру. Этот минерал устойчив к +178 градусам по Цельсию. В данном веществе содержится около 87 процентов серебра. Аргентит имеет кубическую структуру кристалла. Он устойчив к температурам выше 178 градуса. Этот минерал является основным источником, из которого добывается серебро. Чаще всего это соединение можно обнаружить возле медной руды, цинка и свинца.
Применение серебра
В пищевой промышленности из этого металла тоже выплавляют посуду. Кроме того, из него делают специальное оборудование для приготовления напитков и фруктовых соков.
Некоторые виды серебра используют для того, чтобы создавать зеркала. Кроме того, специальные бруски могут быть деталями в аккумуляторах.
Легенды, история, символика
Этот тяжелый металл часто олицетворяют с женским началом. Его сравнивают с Луной. Символ имеет холодный оттенок. В греческих и римских мифах серебро было знаком лунной богини Артемиды-Дианы. Кроме того, этот металл считается символом королев. Из-за того что серебро ассоциируется с луной и ее светом, то часто оно символизирует надежду.
Кроме того, он может указывать на мудрость. Совсем неудивительно, что греческих оракулов связывали с выражением «серебряные языки». Алхимики же считали, что серебро — символ первоначального, чистого состояния любых видов материи. Китайцы считают, что серебро ассоциируется с чистотой, девственностью, яркостью и женственностью. Христианская культура связывала серебро с красноречием, целомудрием.
Магические свойства серебра
В древние времена народы, которые проживали на территории Мексики, считали, что серебро — это грязь божественного происхождения, а также связывали металл с Луной. Чаще для украшений, конечно, использовали золото, однако серебряные изделия указывали на богатство, благополучие и высокое сословие. Часто серебро использовали для пожертвований, к примеру, из него делали иконы и статуи в храмах.
Многие народные верования считают, что этот металл защищает от злых духов и демонов. К примеру, в Риме жрецы закапывали статуи из этого металла вокруг города или страны, чтобы защититься от набегов других варварских народов. Из серебра делали пули, с которыми охотились на ведьм и другую нечисть во время инквизиций. Показательными были выступления, когда во время грозы серебряными пулями стреляли по тучам, якобы отогнать ведьм, которые вызывали эти напасти. Существуют и другие примеры того, как использовали магические свойства серебра.
Полезные качества металла
О таких свойствах металла знали очень давно. К примеру, в шестом веке до нашей эры царь Персии Кир Великий использовал исключительно серебряную посуду для того, чтобы транспортировать и хранить воду во время его походов. Большинство его воинов носили на шее кулоны из серебра либо имели нагрудник и налокотники с таким металлом. Они использовали их при ранениях, т.к. считалось, что если приложить пластину из серебра к ране, то это спасет от заражения инфекциями.
Показательным является пример с Александром Македонским. Он вместе со своим войском вошел на территорию Индии, где часто бушевали эпидемии, в том числе и желудочно-кишечные. Когда его войско начало использовать воду из рек, то военные подхватили подобные инфекции, что привело к болезням. Однако было замечено, что болели только обычные рядовые солдаты, а вот военачальники и старшие по званию не заразились. Многие думали, с чем это связано. Но ответ был очень прост. Обычные военные использовали оловянную посуду, а старшие по чину — серебряную. И этого было достаточно для того, чтобы обезвредить инфекции в воде.
Сейчас ученые доказали, что вода, настоянная на серебре, может не только обеззараживать воду, но и бороться со всеми видами бактерий, грибков и вирусов.
Ее можно использовать при болезнях пищеварительной, дыхательной системы, лечении язв, ран и прыщей. Такая вода также стимулирует регенерацию, поэтому можно делать компрессы из нее. Кроме того, она подойдет для омоложения и укрепления всего организма. Ею можно полоскать зубы, принимать ванны с подобной водой.
В качестве профилактических мер можно пить хотя бы по одному стакану в день. Это средство — природный антибиотик, так что лучше носить какое-либо украшение вместе с собой. Если положить серебро на лоб, то проходят усталость, головные боли и рези в глазах.
Серебро является драгоценным металлом и химическим элементом. Аргентум – 47 элемент в периодической таблице Менделеева. Выглядит серебряная руда как обычная порода. Металл мягкий, пластичный, имеет самую высокую электропроводимость и теплопроводность. Стоит отметить, что химическая активность при этом слабая. Благородный металл используется во многих сферах. Так, он пригодится в ювелирной, электронной, фото- и кинопромышленности. Благодаря бактерицидным свойствам минерал используется и в медицине. Стоит отметить, что самородок содержит множество полезных ископаемых.
Все о серебре

Серебро является довольно распространенным металлом. В ювелирном деле оно нередко сочетается с прозрачными искусственными камнями. Гибкость и пластичность серебра позволяет делать из него необычные и замысловатые изделия. Металл довольно разнообразный и применяется во многих жизненных сферах.



Что это такое?
Серебро является драгоценным металлом и химическим элементом. Аргентум – 47 элемент в периодической таблице Менделеева. Выглядит серебряная руда как обычная порода. Металл мягкий, пластичный, имеет самую высокую электропроводимость и теплопроводность. Стоит отметить, что химическая активность при этом слабая.
Благородный металл используется во многих сферах. Так, он пригодится в ювелирной, электронной, фото- и кинопромышленности. Благодаря бактерицидным свойствам минерал используется и в медицине.
Стоит отметить, что самородок содержит множество полезных ископаемых. Серебряная руда встречается редко, поэтому металл добывается из комплексных полиметаллических руд.



История открытия
Серебро имеет ценные свойства, поэтому о нем знали задолго до начала нашей эры. Установить точную дату невозможно. Первые упоминания встречаются у египтян, они делали из серебра посуду. Украшения из этого металла датируются 5000-3400 годами до н. э. Ранее людям было известно лишь о самородном серебре.
Множественные опыты позволили алхимикам открыть наличие металла в разных соединениях. Тогда появился смысл определить серебро как химический элемент. Потом ученые заинтересовались заживляющими и бактерицидными свойствами материала. В России металл впервые выплавил Лаврентий Нейгарт в 1687 году.

Состав и свойства
Серебро имеет белый металлический блеск. Твердость металла составляет 25 кгс/мм². Благодаря этому свойству материал столь прочный и износостойкий. Плотность аргентума составляет 10,5 грамма на 1 см3. Температура плавления довольно высока, достигает 962°С.
Металл способен выдерживать большие нагрузки. Это позволяет использовать его в качестве материала для многих агрегатов, даже космических ракет и подводных лодок. Серебро хорошо отражает свет, что расширяет сферу использования. А также металл отлично проводит тепло.
Если оставить серебряную ложку в чашке с горячим чаем, то можно обжечься.


Не менее интересны химические свойства вещества. Например, металл может раствориться в ртути и превратиться в амальгаму. Химический элемент не реагирует с кислородом, углеродом, водородом, кремнием и азотом. Однако серебро взаимодействует с другими веществами, которые имеют значение в быту.
- Чувствительность к сероводороду. Даже малое количество приводит к образованию сульфида серебра. Визуально на изделии виден черный налет. Соединения серы окружают людей повсеместно. Вещество есть в продуктах питания, строительных материалах и даже в человеческом поте.
- Реакция с галогенами, особенно с йодом. Стоит избегать контакта серебра с этим веществом.
- При нагревании аргентум адсорбирует газы. Речь идет о кислороде, аргоне, водороде и подобном. Жидкий металл поглощает в разы больше О2, чем твердый. При застывании можно заметить, как через верхнюю корочку пробивается кислород. Это похоже на небольшой серебряный вулкан.

Добыча
Любой металл первоначально нужно откуда-то взять. Нахождение в природе, в рудниках, является основным источником добычи серебра. При этом 2/3 от всего количества является побочным продуктом при производстве никеля, меди, свинца и цинка. А также серебро добывается при вторичной переработке. Однако эффективность процесса низкая из-за его сложности.


Каким бывает?
Всем известно, что золото может быть розовым и белым, а не только рыжим. Вот и ювелирное серебро бывает цветное. Благодаря этому металл выглядит по-разному в изделиях. Правда, экзотические цвета не сильно востребованы среди покупателей. Самородное серебро довольно благородное и привлекательное.
Металл делится на виды в зависимости от дополнительных материалов в составе сплава. Добавки напрямую сказываются на важных свойствах.
Так, некоторые виды серебра подходят для плетения цепочек и браслетов. Иногда специальные напыления играют сугубо декоративную роль и даже усложняют уход за изделием.

Стерлинговое
Такой вид аргентума определен в качестве эталона. В составе 92,5% этого металла и всего 7,5% меди. Добавка нужна для повышения прочности готового изделия. Сплав имеет натуральный белый оттенок.

Матовое
Удалить блеск можно при термической обработке в серной или соляной кислоте. Матовое серебро используется для создания ювелирных изделий.
Такой вид без блеска выглядит стильно и довольно дорого. Декоративные свойства вызывают особый интерес к матовому серебру.

Филигранное
Такой металл отличается пробой 960. В ювелирном деле серебро используется для тонких плетеных узоров.
Интересно, что всего 1 грамм металла нужно взять, чтобы сделать 2 км проволоки. Такие украшения требуют аккуратного использования.

Родированное
Такое серебро считается одним из дорогостоящих. Тонкий слой металла платиновой группы позволяет увеличить износостойкость и эластичность. Такое покрытие защищает украшение от окисления.
Ювелирные изделия из такого серебра можно чистить намного реже, чем другие.

Черненое
Такой интересный вид придумали в России еще в XVII веке. Углубления в изделии заполняются сплавом сульфидов меди, свинца и серебра. В итоге обработанные участки становятся черными, а все выступы остаются белыми.
Очищать изделия следует особо бережно, чтобы не разрушить напыление.

Оксидированное
Подвид черненого серебра. Для создания визуальных эффектов используется пленка из оксида серебра. В этом случае все впадинки могут иметь синий, серый, фиолетовый или черный оттенок.
Украшения требуют особой аккуратности при чистке.

Позолоченное
Внешне напоминает золото, однако стоит дешевле. Изделия следует использовать бережно, чтобы не стереть желтое напыление.
Нельзя допускать контакта позолоченного серебра с химическими веществами и даже водой. Запрещены любые агрессивные механические воздействия.

Применение
Область использования серебра так велика, что сложно перечислить все и сразу. При этом часто металл используется в малом количестве. Физические и химические свойства делают аргентум привлекательным для ювелирного дела. Эти же особенности позволяют использовать серебро при изготовлении технических приспособлений в медицине.
Для украшений и столовых приборов не применяют чистый металл. Пластичность и гибкость его просто не позволяют поступать таким образом. В сплав добавляют медь и подобные вещества для улучшения стойкости к деформации. Чем больше дополнительного материала, тем меньше гибкость.

Стоит отметить, что в любой сфере используется сплав серебра, а не чистый материал. В качестве меры используется проба. Трехзначное число показывает, сколько серебра в 1 кг конкретного сплава.
В России официально признаны несколько официальных вариантов пробы.
- 720. Желтоватый сплав используется для изготовления пружин, иголок и деталей, что подвергаются большим нагрузкам.
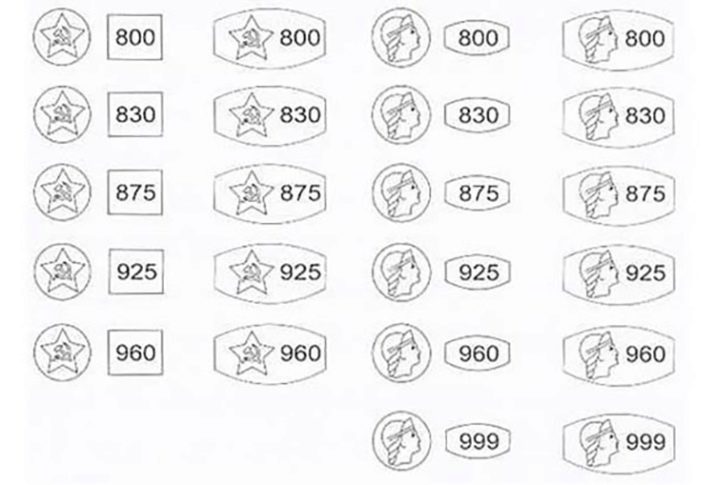
- 800. Металл с желтоватым оттенком применяется при создании украшений и столовых приборов.
- 830. Сфера применения такая же, как и у предыдущего варианта.
- 875. Используется в ювелирной промышленности. Украшения часто покрываются позолотой.
- 916. Ранее использовался для создания столовых приборов. Теперь же в ювелирном деле не применяется вовсе.
- 925. Стандартное стерлинговое серебро. Особо ценится при создании украшений благодаря тому, что практически не окисляется. Может использоваться при изготовлении столовых приборов.
- 960. Применяется сплав при создании изделий с рельефными композициями. Украшения легко деформируются.
- 999. Сырье для изготовления монет и слитков. А также применяется для электрооборудования, в ионизаторах и очистителях воздуха. Такой металл используют при изготовлении зеркал с максимальной точностью. Чистый аргентум можно найти в составе медицинских препаратов.
Сфера применения не ограничивается этим перечнем. Серебро может использоваться в пищевой промышленности. Из него делают аппараты для выжимания сока и изготовления других напитков. Бруски и порошок можно встретить в аккумуляторах.
Вообще, именно в промышленности используется наибольшее количество серебра. Особенно в электротехнике. Хлорид серебра применяется в качестве покрытия радарных поверхностей. Так, металл можно встретить при производстве:
- радиоэлектронных компонентов;
- свинцовых аккумуляторов;
- инфракрасной оптики;
- фильтров противогазов;
- некоторых детонаторов.

Интересные факты
- Последние годы принесли много интересных открытий. Все они позволили обнаружить новые возможности использования серебра в ювелирном деле, промышленности и медицине. В мире существует Институт серебра. Именно эта инстанция сообщает о перспективах использования металла.
- Ученые из Калифорнии вывели новый метод использования серебра для изготовления твердого металла. Вещество будет объединять лучшие качества этой группы элементов со стеклом. Итоговый материал можно применять для изготовления медицинских имплантатов. Ученые уверены, что новинка существенно лучше, чем имеющиеся аналоги.
- Наличие серебра уменьшает риск заражения инфекцией. Это обусловлено уникальными антибактериальными свойствами. Конечно, металл-стекло еще недостаточно исследован. Но сам факт создания такого материала весьма любопытный.
- Из серебра изготавливают необычные наночастицы. Они используются в качестве сенсоров, которые позволяют обнаружить болезнетворные бактерии. Респираторная маска с серебром позволяет уничтожить множество микроорганизмов. Этим общество также обязано науке.

Еще больше интересных фактов о серебре смотрите в следующем видео.
На вопрос о серебре, драгоценный это металл или нет, стоит ответить абсолютно утвердительно. Этот благородный металл очень ценился еще в древности. В те далекие времена серебряные ювелирные изделия обладали баснословно высокой стоимостью. Для примера — у древних римлян в качестве символа максимальной роскоши и достатка выступала солонка, выполненная из этого материала. В течение нескольких веков ценность серебра значительно превышала стоимость золота. Серебро — тяжелый металл, обладающий атомным (молярным) весом около 108 дальтонов (грамм на моль) и плотностью 10,5 грамма на кубический сантиметр.
Серебро

Серебро — Ag, минерал класса самородных элементов, кристаллизуется в кубической сингонии, кубически-гексоктаэдрический вид симметрии. Встречается в аргенитах (сульфид) и роговом серебре (хлорид серебра), добывается также как побочный товар очистки купрума и свинца. Серебро было одним из первых металлов, освоенных человеком. Является великолепным проводником тепла и электричества. Главным производителем серебра является Мексика, хотя серебряные руды разбросаны по всему миру.
СТРУКТУРА

Кристаллическая структура серебра
Сингония кубическая; гексаоктаэдрический в. с. ЗL 4 4L6 3 6L 2 9РС. Кристаллическая структура. Гранецентрированный куб. Облик кристаллов. Правильно образованные кристаллы очень редки. Встречающиеся формы:,. Двойники по (111). Агрегаты. Встречается иногда в виде типичных “вязаных” перистых дендритов, тонких неправильных пластин и листочков. Характерны также моховидные, волосовидные и проводочные формы. Наиболее распространены зерна неправильной формы и более крупные сплошные скопления – самородки.
СВОЙСТВА

Цвет серебряно-белый, часто с жёлтой, коричневой или черной побежалостью. Серебро с поверхности довольно быстро окисляется на воздухе и тем быстрее, чем больше примесей оно содержит, при этом цвет поверхности изменяется до чёрного с отливом различных оттенков. Блеск металлический до матового, цвет черты серебряно-белый, блестящий. Твердость 2,5 —3. Плотность 9,6 —12. Спайность отсутствует, излом раковистый. Весьма пластичное, гибкое, ковкое. Обладает максимальной среди металлов тепло- и электропроводностью. Является диамагнетиком. Под паяльной трубкой легко плавится. С НСI реагирует, образуя белый творожистый осадок (АgCl). Реакция с Н2S дает чёрное окрашивание.
ЗАПАСЫ И ДОБЫЧА

Серебро на акантите, 2.3 x 1.8 x 1.1 см, Перу, шахта Учукчакуа
По СССР крупные месторождения не известны. Самородки серебра в прежнее время находили в Турьинских рудниках на Северном Урале, в ряде свинцово-цинковых месторождений Алтая, Казахстана, Восточной Сибири и в других местах.
Из иностранных месторождений большой известностью пользовались месторождения: Конгсберг(Норвегия), где самородное серебро встречалось до глубины 900 м, Кобальт(Канада), Шнееберг(Германия).
Добыча серебросодержащих руд может производиться подземным или открытым способом. Сначала при помощи специальных приборов геологоразведчики проверяют шахты под землей на предмет содержания полезных ископаемых и драгоценных металлов. После обнаружения богатых серебром участков в соответствующих местах делают отверстия, в которые закладывают взрывчатку. Поднятые взрывом на поверхность шахты осколки серебросодержащей руды измельчают промышленным способом. Из руды драгоценный металл извлекают методами амальгации и цианирования.
ПРОИСХОЖДЕНИЕ

Серебро, ширина 1 см, Марокко, шахта Имитер
Образование самородного серебра в природе во многом аналогично образованию меди. Оно вместе с другими серебросодержащими минералами встречается в гидротермальных жильных месторождениях в ассоциации с аргентитом (Ag2S) и кальцитом (месторождение Конгсберг в Норвегии), иногда в ассоциации со сложными сернистыми, мышьяковистыми, сурьмянистыми соединениями разных металлов, в том числе никеля и кобальта.
В экзогенных условиях оно, так же как и самородная медь, встречается в зонах окисления месторождений сернистых и мышьяково-сурьмянистых руд, являясь продуктом их разложения и восстановления из поверхностных растворов различными органическими соединениями. Образующееся в этих условиях самородное серебро нередко имеет вид дендритов, пластинок, моховидных, проволочных, волосовидных форм и др. Экспериментально доказано, что тончайшие нитевидные и дендритовые образования, иногда в виде красивых узоров, образуются на кусочках угля из раствора, особенно в присутствии растворимых органических соединений.
В поверхностных условиях самородное серебро менее устойчиво, чем золото. Оно часто покрывается пленками и примазками черного цвета. В местностях с жарким, сухим климатом с поверхности нередко переходит в устойчивые галоидные соединения (AgCl и др.).
ПРИМЕНЕНИЕ

Серебро применяется главным образом в сплавах с медью для выделки серебряных изделий, монет и др. Чистое серебро употребляется для филигранных работ, изготовления тиглей для плавления щелочей, для серебрения, для получения химических соединений и других целей. Главная масса серебра (около 80%) добывается не в самородном виде, а в качестве побочного продукта из богатых серебром свинцово-цинковых, золотых и медных месторождений.
Области применения серебра постоянно расширяются, и его применение — это не только сплавы, но и химические соединения. Определённое количество серебра постоянно расходуется для производства серебряно-цинковых и серебряно-кадмиевых аккумуляторных батарей, обладающих очень высокой энергоплотностью и массовой энергоёмкостью и способных при малом внутреннем сопротивлении выдавать в нагрузку очень большие токи.
Содержание серебра в рудах цветных металлов составляет 10—100 грамм на тонну, в золото-серебряных рудах 200—1000 грамм на тонну. Серебряные руды разбросаны по всему миру, но лидерами по его добыче являются Мексика и Перу, за которыми с небольшим отрывом следуют Китай, Чили и Австралия. В России этот металл добывают из серебряно-свинцовых руд Урала, Алтая, Северного Кавказа. Физические и химические свойства. Физические свойства.
Основные сведения о серебре, как химическом элементе
Серебро в химии имеет обозначение Ag (от латинского слова Argentum, восходит к греческому «белый, блестящий»). Это элемент 11 группы (по устаревшей классификации — побочной подгруппы первой группы) пятого периода периодической системы химических элементов Д.И. Менделеева. Атомный номер 47. Относительная атомная масса 107,87 г/моль.
Рисунок 1. Структура серебра и его внешний вид.
Серебро имеет структуру в виде кристаллов неправильной формы. Часто в ней попадаются зерна разных размеров. Они связаны решетчатым каркасом в виде гранецентрированного куба (атомы расположены на каждой вершине куба и в центре граней).
В природе металл встречается в виде самородков (содержат 95 —99% серебра и примеси золота, платины, меди и других металлов) и в составе примерно 60 минералов. В таблице 1 приведены минералы, которые встречаются чаще остальных.
| Название минерала | Дополнительные компоненты | Содержание серебра, % |
| электрум | золото | 20-28 |
| аргентит | сера | 87 |
| гессит | теллур | 63 |
| науманит | селен | 73 |
| дискразит | сурьма | до 74 |
| кераргирит | хлор | 75 |
| прустит | сера и мышьяк | 65 |
Таблица 1. Содержание серебра в разных минералах.
Также в качестве примеси серебро обнаружено во всех медных и свинцовых рудах. Именно из них получают до 80% всего добываемого серебра. Содержание серебра в рудах цветных металлов составляет 10—100 грамм на тонну, в золото-серебряных рудах 200—1000 грамм на тонну.
Серебряные руды разбросаны по всему миру, но лидерами по его добыче являются Мексика и Перу, за которыми с небольшим отрывом следуют Китай, Чили и Австралия. В России этот металл добывают из серебряно-свинцовых руд Урала, Алтая, Северного Кавказа.
Физические и химические свойства
Физические свойства
Таблица 1. Основные физические свойства серебра.
Химические свойства серебра обусловлены положением в таблице Д.И. Менделеева. Особенность строения атома серебра заключается в наличии одного электрона на пятой орбитали. Электронная формула: 1s22s22p63s23p63d104s24p64d105s1.
Может проявлять степени окисления: -2, -1, +1, +2, +3, наиболее стабильная +1. Валентности: I, II, III. Входит в группу благородных металлов и в электрохимическом ряду напряжений находится после водорода, поэтому не взаимодействует с некоторыми веществами.
Серебро не взаимодействует:
- с растворами разбавленных соляной и серной кислот, щелочами;
- с водой: растворимость серебра в воде — 0,04 мкг/л;
- с кислородом, углеродом, хлором в обычных условиях, азотом и кремнием.
1. С неметаллами:
а) сера в обычных условиях:
2 A g + S → A g 2 S сульфид серебра I.
б) галогены при нагревании с образованием галогенидов серебра I:
2 A g + B r 2 → t ° 2 A g B r бромид серебра I.
в) кислород при повышении давления и температуры до 170 °С образует на поверхности серебра пленку:
4 A g + O 2 → t ° 2 A g 2 O.
г) селен, теллур, фосфор, мышьяк и углерод при нагревании с образованием бинарных соединений типа: A g 2 S e селенид серебра, A g 3 P фосфид серебра, A g 4 C карбид серебра и т.п.
P + 3 A g → t ° A g 3 P.
а) в газообразном виде:
- с сероводородом на воздухе с образованием на поверхности металла темного налета: 4 A g + O 2 + 2 H 2 S → A g 2 S + 2 H 2 O;
- с хлороводородом при нагревании: 2 A g + 2 H C l → t ° A g C l + H 2.
б) H N O 3, горячая H 2 S O 4 конц, HCl в присутствии свободного кислорода:
- 3 A g + 4 H N O 3 р а з б → 3 A g N O 3 н и т р а т с е р е б р а I и л и л я п и с + N O + H 2 O;
- A g + 2 H N O 3 к о н ц → A g N O 3 + N O 2 ↑ + H 2 O;
- 2 A g + 2 H 2 S O 4 к о н ц → t ° A g 2 S O 4 + S O 2 ↑ + H 2 O;
- 4 A g + 4 H C l + O 2 → 4 A g C l + 2 H 2 O.
в) концентрированные HCl и HBr, медленно:
- 2 A g + 4 Н С l → 2 H [ A g C l 2 ] + Н 2;
- 2 A g + 4 Н В r → 2 H [ A g B r 2 ] + Н 2.
3. С цианидами в присутствии кислорода воздуха с образованием дицианоаргентатов (I):
4 A g + 8 N a C N + O 2 + 2 H 2 O → 4 N a [ A g ( C N ) 2 ] д и ц и а н о а р г е н т а т н а т р и я + 4 N a O H.
4. С хлоридом железа (травление):
A g + F e C l 3 → A g C l + F e C l 2.
5. Со ртутью серебро образует жидкий сплав — амальгаму.
Способы получения
1. Пирометаллургический способ позволяет получать серебро как побочный продукт при переработке свинцово-цинковых руд. Проходит в несколько стадий:
- руду смешивают с жидким цинком → интерметаллиды цинка с серебром A g 2 Z n 3, A g 2 Z n 5 всплывают серебристым слоем на поверхности жидкого свинца;
- серебристый слой снимают, цинк удаляют перегонкой;
- свинец из остатка удаляют реакцией с кислородом: он выводится в виде оксида свинца (IV);
- далее серебро очищается электролитически.
2. Цианидное выщелачивание позволяет выделять серебро из тех руд, где оно содержится в малых количествах. Метод включает следующие стадии:
- обработка серебросодержащей руды раствором цианида натрия → серебро переходит в анионный комплекс N a [ A g ( C N ) 2 ];
- фильтрование через цинковую пыль, в ходе которого цинк вытесняет серебро: 2 N a [ A g ( C N ) 2 ] + Z n → N a 2 [ Z n ( C N ) 4 ] + 2 A g ↓;
- обработка серебряного осадка серной кислотой для удаления примесей;
- далее полученный остаток промывают, фильтруют, выпаривают и сплавляют в слитки.
3. При переработке медных руд серебро извлекают из анодного шлама методом электролитического рафинирования меди.
4. Амальгамный метод извлечения серебра уже не используется, но интересен с точки зрения истории:
- руда смешивается со ртутью → амальгама серебра;
- ртуть удаляют отгонкой → сырое серебро;
- сырой металл подвергают электролитическому очищению (аффинажу) в р-ре A g N O 3 с осаждением серебра высокой степени чистоты (99,9%) на катоде.
Сферы применения
- Ювелирное дело: изготовление украшений и посуды, декоративных изделий.
- Чеканка монет, медалей и других наград.
С середины XX века примерно 70% добываемого серебра расходуется промышленностью:
Химические свойства серебра. Серебро — сравнительно мягкий и пластичный металл, из 1 г его можно вытянуть металлическую нить длиной 2 км! Серебро тяжёлый металл, имеет низкую теплопроводность и электропроводность. Температура плавления относительно невысок, всего 962° С. Серебро охотно образует сплавы с другими металлами, которые придают ему новые свойства, например, при добавлении меди получается более твердый сплав — биллон. При нормальных условиях серебро не подвержено окислению, однако имеет способность поглощать кислород. Твердое серебро при нагреве способно растворить в пять раз больший объем кислорода!
Серебро

Серебро – химический элемент, благородный металл, известный с древнейших времен, распространен в природе гораздо меньше, чем медь. Серебряные наночастицы применяют в растениеводстве в качестве биологически активных веществ, стимулирующих рост и развитие растений.


серебряный кристалл

Чистый (>99.95%) искусственный серебряный кристалл, полученный путем электролиза с видимой дендритной структурой.
Латинское название – Argentum – дано этому металлу в связи с его цветом и является производным от греческого «аргос», то есть «белый, блестящий». Русское название «серебро» происходит от слова «серп» и связано непосредственно с луной (серп луны). Блеск самородков серебра, окрашенных в светло-желтый цвет, похож на сияние ночного светила. Более того, в алхимии в качестве символа серебра используется знак луны.
Наиболее древние ювелирные серебряные изделия были обнаружены в захоронениях, относящихся ко второй эпохе Герзе, то есть 3900 – 3600 лет до нашей эры.
Серебряные самородки находят очень редко, гораздо реже золотых. Именно поэтомудо конца I тысячелетия до нашей эры серебро ценилось выше золота. Ситуацию изменило открытие способа выделения чистого серебра из свинцовых руд.
Благодаря ковкости и пластичности серебро широко применяется в ювелирном деле во всех странах мира. Высокая электро- и теплопроводность сделала этот материал незаменимым в технике. Химические соединения серебра разлагаются на свету, что используется в фотографии.
Современные исследования подтверждают широкий спектр противомикробного действия серебра, отмечают отсутствие устойчивости к нему у многих патогенных организмов, низкую токсичность и гипоаллергенность. Благодаря этим свойствам материал широко используется при создании медицинских препаратов антисептического, противовоспалительного и бактерицидного действия.
В последнее десятилетие активно изучается действие наночастиц серебра на рост и развитие растений. Многочисленные исследования подтверждают положительное воздействие элемента на ростовые процессы.

Руда серебра

Физические и химические свойства
Серебро(Argentum) Ag– химический элемент побочной подгруппы первой группы периодической системы. Характеризуется ярко выраженным физиологическим воздействием на живые организмы, устойчивостью к воздействию кислорода воздуха в нормальных условиях. Атомный номер – 47. Атомная масса – 107,87.Плотность – 10,49 г/см3. Температура плавления – 960, 5°C. Температура кипения – 2210°C.
Серебро – белый, блестящий металл, в тонких пленках и проходящем свете – голубого цвета. На открытом воздухе, под действием сероводорода, серебро окисляется, покрываясь темным налетом сульфида серебра. Характеризуется наивысшей электро- и теплопроводностью среди прочих металлов периодической системы и лучшей отражательной способностью, в частности в инфракрасном и видимом свете. Растворимость серебра в воде – 0,04 мкг/л. В водных растворах ионы серебра образуют долго сохраняющие стабильность гидратированные ионы.
При повышении температуры и давления на поверхности серебра образуется одновалентный оксид серебра (Ag2O). Суспензия этого соединения обладает антисептическими свойствами. При температуре 200°CAg2 Oразлагается. Кроме указанного, устойчивым является и двухвалентный оксид серебра – AgO.
Серебро проявляет устойчивость к воздействию кислот. Разбавленная серная, соляная кислота и смесь концентрированной азотной и соляной кислот (царская водка) на него действия не оказывают в связи с образованием на поверхности металла защитной пленки из хлорида серебра (AgCl).
Хлорид серебра (AgCl) образуется в виде белого творожистого осадка нерастворимого в воде и кислотах при взаимодействии серебра с хлорид-ионами. На свету он постепенно темненнт и разлагается с выделением металлического серебра. Такими же свойствами обладают йодид и бромид серебра, но они имеют желтоватый цвет. Фторид серебра в воде растворяется.
Горячая концентрированная серная кислота (H2SO4) способна растворять серебро, образуя сульфат серебра(Ag2SO4).
Азотная кислота (HNO3) растворяет серебро с образованием нитрата серебра (ляпис)–AgNO3.Это бесцветные кристаллы хорошо растворимые в воде. Применяется ляпис в производстве фотоматериалов, в гальванотехнике, в медицине и растениеводстве.
Химические соединения серебра термодинамически малоустойчивы. При этом углерод-и азотосодержащие соединения одновалентного серебра разлагаются со взрывом.
Ag (95 – 98%) спримесьюAu, Hg,Sb,Bi, Cu, As,Pl
серебряно-белый часто с темным налетом
светло-желтый до серебряно-белого и зеленоватого
свинцово-серый до железно-черного
серая со слабым блеском
ярко-красный (цвет киновари), темнеет
кирпичная до ярко-красной
черный до темно-серого
смоляной до матового, у кристаллов алмазный
серый, бесцветный, с бурым (зеленым) оттенком, на свету темнеет до черного
сероватый до железно-черного
полуметаллический до алмазного
железно-черный до стально-серого в тонких осколках кроваво-красный
металлический, алмазовидный, матовый
железно-черный, в очень тонких осколках темно-красный
Физические свойства важнейших минералов серебра
Содержание в природе
Серебро – редкий металл, по среднему содержанию в земной коре находится на 69 месте среди остальных элементов периодической системы.
- в гранитах – 0,037х10 -4;
- в гранитоидах – 0,050х10 -4;
- в липаритах – 0,049х10 -4;
- андезитах – 0,080х10 -4;
- базальтах – 0,110х10 -4;
- габбро – 0,110х10 -4;
- ультроосновных породах – 0,600х10 -4;
- в среднем для пород Японии – 0,08 х10 -4.
- в магматических:
ультраосновных – 0,05х10 -4;
основных – 0,1х10 -4;
средних – 0,07х10 -4;
кислых – 0,05х10 -4;
в глинах, сланцах – 0,1х10 -4;
песчаниках – 0,44х10 -4;
карбонатных – 0,02х10 -4;
- в среднем по литосфере – 0,07х10 -4;
- в метеоритах-хондритах – 0,094х10 54;
- в железных метеоритах – 5х10 -4.
Содержание серебра в различных соединениях
В настоящее время большую часть серебра получают из его соединений. Самая важная серебряная руда – аргенит (серебряный блеск). Одновременно в качестве примеси серебро обнаруживается во всех медных и свинцовых рудах. Именно из них получают до 80% всего добываемого серебра. В России этот металл добывают из серебряно-свинцовых руд Урала, Алтая, Северного Кавказа.
Известно более 60 серебосодержащих минералов, которые делятся на 6 групп:
самородное серебро, содержит 95 – 99% серебра с примесью золота, платины, меди и других металлов;
сплавы серебра золотом (электрум) – 20 – 28 % серебра;
простые сульфиды серебра (аргентит) – 87 % серебра;
теллуриды и селениды серебра – гессит (63%), науманит (73%);
антемониды и арсениды – дискразит (до 74%);
галогениды и сульфаты – кераргирит (75%);
сложные сульфиды (тиосоли) – пираргирит(60%), прустит (65%).
Содержание серебра в почвах
Коллоидное серебро
Чистое серебро малорастворимо в воде. Ядовитость растворимых соединений серебра – факт общеизвестный. Тогда как все типы наночастиц серебра характеризуются низкой или нулевой токсичностью.
Проблему снабжения животных и растительных организмов необходимой дозой серебра в настоящее время решают с помощью коллоидных систем, содержащих наночастицы серебра. Данные о действии коллоидных наночастиц серебра на живые организмы, в том числе и растения весьма противоречивы. В целом это связано с недостаточной изученностью вопроса. Однако, в целом наука склоняется к положительному влиянию минимальных доз серебра на рост и развитие растений и животных, как и других микроэлементов.
Коллоидная система
Любая коллоидная система состоит из сверхмалых частиц находящихся во взвешенном состоянии в той или иной среде, например воде. Размер частиц в коллоиде составляет от 0,1 до 0,00 1 микрона. При размерах частиц менее 0,1 микрона – система будет представлять собой истинный раствор,при размерах более 100 нм –суспензию.
Коллоидная система обладает тремя свойствами:
- Состоит из разнородных компонентов.
- Является многофазной.
- Частицы не растворяются в растворе или суспензии.
Физико-химические свойства коллоидного серебра
Физико-химические свойства коллоидных наночастиц серебра определяютсяих агрегативной и седиментационной(способностью противостоять силе тяжести) устойчивостью, а также возможностью их окисления кислородом окружающего воздуха.
Устойчивость коллоидной системы в данном случае зависит от исходной концентрации ионов серебра в растворе.
Размеры наночастиц серебра варьируют в пределах от 3 до 100 нм. Физические свойства серебра в нанодиапазоне отличаются от свойств серебра. Например, уменьшение размеров частиц приводит к снижению температуры плавления.
Наночастицы серебра обладают большой удельной площадью поверхности, что увеличивает область контакта элемента с патогенными организмами и улучшает его бактерицидное действие. Одновременно увеличивается скорость адсорбции клеткой и транспортировка через клеточную мембрану.
Биологические эффекты наночастиц серебра
Горчица сарепская(Brassica juncea)– при проращивании семянна базальной питательной среде при использовании наночастиц серебра установлен положительный эффект, выражающийся в увеличении длинны, диаметра, числа листьев и побегов, а так же в повышение урожайности.
Рапс(Brassica napus) – привоздействии наночастицами серебра на ранних стадиях онтогенеза существенно наращивает массу корней и стеблей. Одновременно отмечается снижение энергии прорастания и всхожести семян.
Босвелия(Boswellia ovalifoliolata) – обработка семянускоряется прорастание и рост саженцев.
Спаржа лекарственная(Asparagus officinalis) – обработка семян ускоряется их прорастание и дальнейшее развитие растений. Одновременно отмечается повышение содержания аскорбиновой кислоты и хлорофилла в обработанных проростках.
Боб садовый(Vicia faba) – при добавлении в питательную средунаночастиц серебра отмечается снижение всхожести, замедление образования клубеньков (уменьшается численность бактерий симбиотов Rhizobium leguminosarum), замедление роста побегов, уменьшение длины корней.
Томаты(Solanum lycopersicum) – при добавлении в гидропонную среду наночастиц серебра всхожести не снижают, но уменьшают длину побегов и корней. Отмечается снижение активности фотосинтеза.
Редька посевная(Raphanus sativus) – при выращивании на гидропонной среде с добавлением наночастиц серебра всхожесть семян остается неизменной, длина корней и побегов уменьшается, снижается активность фотосинтеза.
Латук посевной(Lactucasativa) – отрицательное воздействие не наблюдается. Содержание серебра в съедобных частях растений составляет менее 1% от общего количества, внесенного в почву.
Знак влияния наночастиц на растения может зависеть от дозы внесения. При проращивании семян Риса посевного (Oryza sativa)на среде содержащей наночастиц серебра 30 мг/мл рост корней усиливается. При повышении концентрации до 60 мг/ мл проростки замедляли рост по сравнению с контролем. Одновременн, при увеличении дозы, отмечается уменьшение численности ризосферных организмов, поскольку бактериальные клеточные стенки повреждаются наночастицами серебра.
Подавление роста в зависимости от дозы и времени воздействия наблюдается у Ряски малой(Lemma minor), а прибольших концентрациях проявляются признаки окислительного стресса и изменения в структуре хлоропластов.
Фасоль золотистая(Phaseolusradiates) и Сорго зерновое (Sorghum bicolor)показывают большее подавление роста при выращивании на питательной среде с добавлением наночастиц серебра, чем на почве с аналогичными добавками.
Проведенные исследования на Многокореннике обыкновенном (Spirodela polyrhiza)по влиянию размеров наночастиц на токсические эффекты показали, что мелкие ( 6 нм) наночастицы более токсичны, чем крупные ( 20 – 100 нм).
Ячмень при обработке семяннаносеребром увеличивает длину корней проростков. Салат – уменьшает.
Влияние наночастиц серебра на морфологическое и физиологическое состояние растений зависит от их вида и формы. В частности, десятигранные наночастицы серебра значительно влияют на удлинение корней Резуховидки (Arabidopsis). Одновременно наночастицы сферической формы не оказывают на рост корней никакого эффекта.
В публикациях часто обнаруживаются противоречивые, часто противоположные данные о влиянии наночастиц серебра на растения. Это объясняется различиями в условиях экспериментов и недостаточнойизученностью вопроса, поскольку активные исследования влияния наночастиц серебра на растения ведутся не более 10 лет.
Серебро — Ag, минерал класса самородных элементов, кристаллизуется в кубической сингонии, кубически-гексоктаэдрический вид симметрии. Встречается в аргенитах (сульфид) и роговом серебре (хлорид серебра ), добывается также как побочный товар очистки купрума и свинца. Серебро было одним из первых металлов, освоенных человеком. Является великолепным проводником тепла и электричества. Главным производителем серебра является Мексика, хотя серебряные руды разбросаны по всему миру.
- https://zen.yandex.ru/media/uvelircentr/harakteristiki-i-svoistva-serebra-kak-metalla-5c3f64a0d8b60a00a9d5e4de
- https://vplate.ru/metally-i-splavy/vse-o-serebre/
- https://mineralpro.ru/minerals/silver/
- https://wika.tutoronline.ru/himiya/class/11/osnovnye-svedeniya-o-serebre-kak-himicheskom-elemente
- https://www.pesticidy.ru/active_nutrient/Silver