Заявляемое техническое решение относится к области электротехники, связанной с разработкой электролизеров, и может быть использовано при изготовлении платинированных титановых анодов электролизеров для аппаратов получения гипохлорита натрия и «Искусственная почка».
Известны различные методы нанесения платины на подложки: химический, электрохимический, контактного платинирования. Однако проведение платинирования титана по известному способу из платинохлористоводородной кислоты путем восстановления формалином не приводило к высаживанию платины на поверхность подложки. Так же опробование способа контактного платинирования из хлорплатината аммония в присутствии хлористого аммония при температуре 353 K в течение одного часа показало, что платиновое покрытие на поверхности титановой подложки отсутствует. Эти способы не применимы для нанесения платины на титан.
Одним из наиболее распространенных и близким по технической сущности к заявляемому решению является способ электрохимического платинирования из фосфатных электролитов, включающий электрохимическое нанесение платины из раствора, г/л: платинохлористоводородная кислота 5 8; двухзамещенный фосфорнокислый аммоний 26 45; двухзамещенный фосфорнокислый натрий 120 — 240, при плотности тока 0,1 0,5 А/дм 2 . Однако основным недостатком такого способа является низкая активность анода в реакции выделения гипохлорита натрия. Также использование электролизера в аппарате «Искусственная почка» с анодами приводит к генерации нитрат-ионов в диализирующем растворе и к снижению его pH, что вызывает накопление нитрат-ионов в организме больного и понижает pH его крови.
SUNLIGHT / Серебро 925 пробы
Для решения поставленной задачи заявляется способ платинирования титанового анода для электрохимических процессов, отличающийся от известного тем, что платинирование проводят химическим способом в течение 5 25 ч из водно-спиртового раствора следующего состава, мас.
тетрахлороплатоат калия 0,076 0,358
этиловый спирт 17,2 35,6
остальное вода.
Необходимо отметить, что поверхность платины, нанесенной по предлагаемому способу, определенная потенциодинамическим методом, составляет 60 80 см 2 на один сантиметр квадратный геометрической поверхности электрода. В то время как поверхность платины, нанесенной по известному способу, составляет 10 15 см 2 /см 2 . Таким образом удалось решить вопрос повышения активности анода, снизить количество нитрат-ионов и повысить pH раствора.
Согласно заявляемому способу платинирования были изготовлены несколько вариантов анодов, полученных из растворов различных составов и с различным временем платинирования.
Испытания электролизера в качестве электролизера аппарата «Искусственная почка» проводили при следующих параметрах:
раствор NaCl 9 г/л
концентрация мочевины 0,6 г/л
скорость потока раствора 0,25 л/мин
электролизер с суммарной площадью однополюсных электродов 0,1 м 2
межэлектродное расстояние 1 мм
pH раствора на входе электролизера 7,2
температура раствора 309 К.
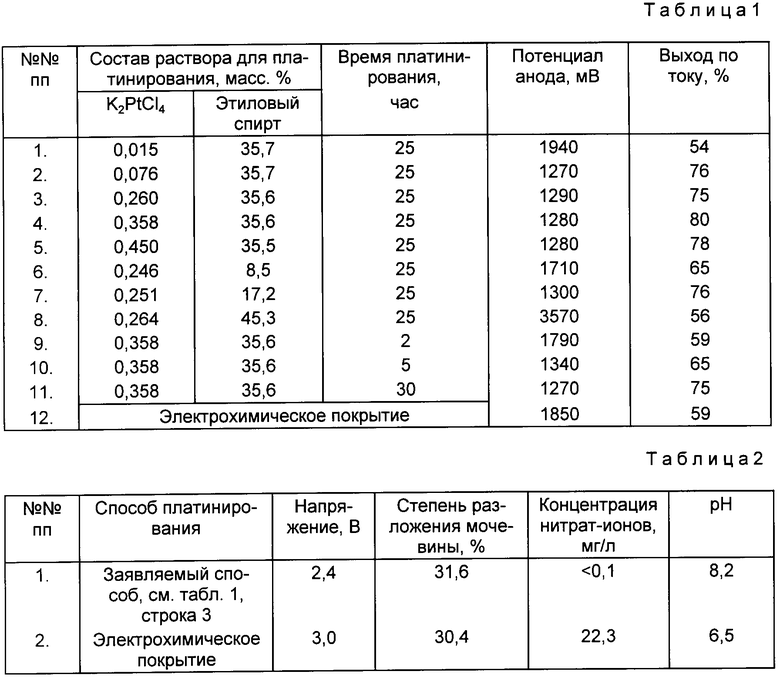
Экспериментальные данные по испытанию анодов для получения гипохлорита натрия представлены в табл. 1. Результаты испытаний электролизера диализирующего раствора представлены в табл. 2. Для сравнения в таблицах приведены результаты испытаний анода и электролизера из анодов, изготовленных по прототипу.
Как видно из табл. 1 (строки 2, 3, 4, 7, 10), аноды, платинированные по заявляемому способу, обладают повышенной активностью. Испытания электролизера с анодами по заявляемому способу в аппарате «Искусственная почка» (см. табл. 2) показывают, что аноды обладают повышенной активностью, при этом в диализирующем растворе отсутствуют нитрат-ионы и повышается его pH.
Уменьшение (табл. 1, строка 6) и увеличение (табл. 1, строка 8) содержания этилового спирта выше указанных пределов приводит к снижению активности.
Оптимальное время платинирования (табл. 1, строки 4, 10) составляет 5 — 25 ч. Уменьшение времени (табл. 1, строка 9) платинирования приводит к уменьшению активности, увеличение (табл. 1, строка 11) приводит к значительному снижению производительности труда при процессе платинирования.
Использование метода платинирования титановых анодов по заявляемому способу позволит снизить затраты электроэнергии на производство гипохлорита натрия на 30 40% а также позволит производить анализ со значительным снижением нитрат-ионов в организме больного и не снижать pH его крови.
Похожие патенты RU2096528C1
- Громыко В.А.
- Кривобок Н.М.
- Владимиров И.В.
- Хозяшев С.И.
- Хозяшев С.И.
- Ашихин Виктор Владимирович
- Лебедь Андрей Борисович
- Краюхин Сергей Александрович
- Воронцов Вадим Валентинович
- Юнь Антонин Александрович
- Ковригин Дмитрий Николаевич
- Чиркова Светлана Салаватовна
- Скопин Дмитрий Юрьевич
- Шполтакова Ирина Александровна
- Щипанов И.В.
- Новоселов А.П.
- Сонькин Владимир Семенович
- Муралеев Адиль Ринатович
- Сидин Евгений Геннадьевич
- Маганов Дмитрий Дмитриевич
- Гельман Дмитрий Евгеньевич
- Носков Сергей Григорьевич
- Стрелков Сергей Иванович
- Лещинский Герман Михайлович
- Шутов Олег Александрович
- Базаев Николай Александрович
- Хозяшев С.И.
- Нефедкин С.И.
- Коровин Н.В.
Иллюстрации к изобретению RU 2 096 528 C1
Реферат патента 1997 года СПОСОБ ПЛАТИНИРОВАНИЯ АНОДА ДЛЯ ЭЛЕКТРОХИМИЧЕСКИХ ПРОЦЕССОВ
Изобретение относится к области электротехники, связанной с разработкой электролизеров, и может быть использовано при изготовлении платинированных титановых анодов электролизеров для аппаратов получения гипохлорита натрия и «Искусственная почка». Способ платинирования анодов на основе титана для электролиза растворов путем химического нанесения заключается в том, что платинирование проводят в растворе, содержащем 0,076 — 0,358% тетрахлороплатоата калия, 17,2 — 35,6% этилового спирта, остальное — вода и выдерживают в течение 5 — 25 ч. 2 табл.
Формула изобретения RU 2 096 528 C1
Способ платинирования титанового анода для электрохимических процессов путем нанесения платины из платиносодержащего раствора, отличающийся тем, что платинирование проводят в растворе, содержащем следующие компоненты, мас.
Тетрахлороплатоат калия 0,076 0,358
Этиловый спирт 17,2 35,6
Вода Остальное
и выдерживают в течение 5 25 ч.
Источник: patenton.ru
Покрытия металлами платиновой группы
Шесть металлов платиновой группы по своим основным свойствам могут быть отнесены к двум подгруппам.
Первая подгруппа включает «легкие» платиновые металлы с плотностью в пределах 12—12,4; к этой подгруппе относятся рутений, родий и палладий. Ко второй подгруппе «тяжелых» платиновых металлов относятся осмий, иридий и платина с плотностью в пределах 21,4—22,6.
В настоящее время из всех шести платиновых металлов сколько-нибудь значительное промышленное применение в гальванотехнике получил родий. По имеющимся данным, годовая потребность родия в США для целей покрытия составляет 155 кг стоимостью в один миллион долларов. Платина и палладий в принципе могут получить важное значение в гальванотехнике, но в настоящее время нет такой области применения, которая могла бы в широких масштабах использовать эти металлы из-за их высокой стоимости. Положение может существенно измениться, когда платинированный титан найдет широкое применение для катодной защиты судов от коррозии в морской воде, а также трубопроводов (нефтепроводов).
Рутений, иридий и осмий в настоящее время не имеют практического применения в гальванотехнике вследствие редкого распространения их в земной коре, высокой стоимости и весьма ограниченного спроса на покрытия этими металлами из-за технологических трудностей процесса и неудовлетворительных свойств покрытий.
По сравнению с электроосаждением серебра и золота электроосаждение платиновых металлов связано с большими трудностями. Платиновые металлы в водных растворах проявляют большую склонность к комплексообразованию, причем некоторые комплексы столь прочны, что не могут быть использованы в качестве основных компонентов (солей) для электроосаждения соответствующих металлов. Так, например, платиновые металлы не могут быть выделены на катоде из растворов их комплексных цианистых солей. Кроме того, некоторые соли платиновых металлов, из которых электроосаждение возможно, например, платинохлористоводородной кислоты, склонны к гидролизу и для ведения процесса с удовлетворительным выходом по току необходимо тщательно регулировать кислотность. Тем не менее трудности в большей или меньшей степени преодолены, и в настоящее время имеются методы электроосаждения всех платиновых металлов, за исключением осмия.
Вследствие высокой стоимости платиновых металлов неудивительно, что вначале внимание было сосредоточено на электроосаждении тончайших покрытий (доли микрона) с максимальным блеском. Однако в годы второй мировой войны к родиевым покрытиям предъявлялись более серьезные требования — они должны были сопротивляться коррозии и защищать поверхность изделий от механического износа. Поэтому возникла необходимость наносить покрытия больших толщин.
Тонкие покрытия из металлов платиновой группы неизбежно имеют поры (часто они имеются и в покрытиях значительной толщины) и при наличии электролита (в простейшем случае влажного воздуха) работает коротко замкнутый гальванический элемент, который ускоряет коррозию основного металла. В целях ослабления этого эффекта основной металл предварительно покрывают никелем или серебром. Гальваническая пара обезвреживается в случае применения нескольких металлов, например титана и тантала в качестве прослоек, которые, являясь анодами, обусловливают образование защитной окисной пленки. Аналогичные явления наблюдаются на платинированном титане, который является анодом при электрохимической (катодной) защите сосудов. Если не превзойдено критическое напряжение, то титановый анод, оголенный в местах пор, или других дефектов покрытия, практически сохраняет срок своей службы.
За редким исключением платиновые аноды не растворяются в электролитах, применяемых для электроосаждения платиновых металлов. Чаще применяют нерастворимые платиновые аноды, а металл, выделяющийся на изделиях и уносящийся выгружаемыми изделиями, периодически пополняется соответствующими солями. При этом, однако, накапливается анион вводимой соли и тем самым сокращается срок службы электролита. Так как периодическая замена постепенно загрязняющегося электролита свежим удорожает процесс, то было установлено, что более целесообразно периодически добавлять соли, например, динитродиамин-платины при платинировании. При таком методе электролит может работать неограниченно долго.
- Родирование
- Палладирование
- Платинирование
- Покрытия рутением и иридием
Защитные покрытия металлов
- Подготовка поверхности
- Электролитическое и химическое полирование металлов
- Электрохимическое выделение и растворение металлов и сплавов
- Макро- и микрорассеивающая способность электролитов. Выравнивание поверхности
- Цинкование
- Кадмирование
- Лужение
- Свинцевание горячее и электролитическое
- Алюминирование
- Меднение
- Никелирование
- Хромирование
- Гальванические покрытия драгоценными металлами
- Гальваническое покрытие легких металлов и сплавов
- Химическое оксидирование металлов и сплавов
- Фосфатирование
- Обезвреживание сточных вод
- Металлургия
Источник: www.stroitelstvo-new.ru
Платинирование металлов

Медные и латунные предметы покрываются тонким слоем платины в следующем растворе, нагретом до кипения: 1 часть нашатырной платины (хлороплатината аммония), 8 частей нашатыря и 40 частей воды.
После платинирования предметы чистят мелом.
Для той же цели предметы можно натирать смесью, состоящей из равных частей нашатырной платины и винного камня.
Стальные и железные предметы можно платинировать, покрывая их раствором хлорной платины в эфире.
Для платинирования мелких галантерейных вещей может служить доведенный до кипения раствор 10 частей хлорной платины и 200 частей поваренной соли в 1000 частях воды, к которому добавляют немного едкого натрия до щелочной реакции. В этом растворе можно платинировать также и с цинковым контактом, т.е. приводя металлическую поверхность в соприкосновение с цинковой палочкой.
Источник: electro-shema.ru