Оглавление диссертации кандидат химических наук Леглер, Елена Викторовна
Глава 1. Литературный обзор.
1.1. Аминокислоты как биохимические лиганды.
1.1.1. Функциональные группы аминокислот как металлсвя-зывающие центры.
1.1.2. ИК-спектроскопические исследования аминокислот и их комплексов.
1.1.2а. ИК-спектроскопическое изучение аминокислот.
1.1.26. ИК-спектроскопические исследования аминокислотных комплексов металлов.
1.1.3. Некоторые трифункциональные аминокислоты, их особенности и биологическая роль.
1.1 .Зв. Глутаминовая кислота.
1.2. Комплексные соединения серебра с аминокислотами.
1.3. Исследование комплексообразования серебра с аминокислотами в растворах.
1.4. Некоторые медицинские аспекты использования препаратов серебра.
Глава 2. Экспериментальная часть.
2.1. Исходные вещества и методы анализа синтезированных соединений.
2.2. Методы исследования комплексных соединений.
Глава 3. Синтез и исследование комплексных соединений серебра с трифункциональными аминокислотами — глутаминовой кислотой, триптофаном, аргинином и гистидином.
Лекция: Химия — Аминокислоты
3.1. Методики синтеза аминокарбоксилатов серебра.
3.2. Определение стехиометрического состава комплексов и их термогравиметрическое исследование.
3.3. ИК-спектроскопическое изучение синтезированных соединений.
3.4. Изучение комплексных соединений методами растворимости и рН-метрии.
Глава 4. рН-метрическое исследование равновесий комплексообразования серебра с трифункциональными аминокислотами в водных растворах.
4.1. рН-метрия как метод исследования равновесий комплексообразования в водных растворах.
4.2. Изучение равновесия комплексообразования серебра с глута-миновой кислотой.
4.3. Изучение равновесия комплексообразования серебра с триптофаном.
4.4. Изучение равновесия комплексообразования серебра с аргинином.
4.5. Изучение равновесия комплексообразования серебра с гисти-дином.
Глава 5. Исследование биологической активности комплексных соединений серебра с аминокислотами.
5.1. Определение острой токсичности соединений серебра с аминокислотами.
5.2. Определение антимикробной активности соединений серебра с аминокислотами.
Рекомендованный список диссертаций по специальности «Физическая химия», 02.00.04 шифр ВАК
Термодинамика процессов комплексообразования ионов кальция с аминокислотами в водном растворе 2011 год, кандидат химических наук Курочкин, Владимир Юрьевич
Синтез и исследование комплексных соединений платины (IV) с аминокислотами, аденином и цитозином 2007 год, кандидат химических наук Андреева, Ольга Ивановна
Биологические свойства координационных соединений серебра и триптофана 2009 год, кандидат биологических наук Суфиев, Туй Давлатович
Координационная химия d- и f-элементов с полидентатными лигандами: синтез, строение и свойства 2007 год, доктор химических наук Буков, Николай Николаевич
Комплексные соединения никеля (II), палладия (II) с аминокислотами и АТФ 2002 год, кандидат химических наук Тинаева, Нина Константиновна
Введение диссертации (часть автореферата) на тему «Исследование комплексообразования серебра (1) с трифункциональными аминокислотами»
Актуальность работы. Возрастающая потребность в высокоэффективных лекарственных препаратах требует проведения широких научных исследований по целенаправленному синтезу новых биологически активных веществ.
Аминокислоты. 1 часть. 11 класс.
В связи с широкой распространённостью инфекционно-воспалительных заболеваний особенно велика потребность в препаратах противовоспалительного и противомикробного действия. В последнее время большое внимание уделяется координационным соединениям благородных металлов с аминокислотами, которые могут быть использованы в качестве антибактериальных средств.
Однако недостатками изученных соединений являются узкий спектр биологического действия и высокая токсичность. Комплексные соединения серебра с аминокислотами в этом аспекте практически не исследованы. В то же время положительная биологическая роль серебра, его бактерицидное действие и адаптированность аминокислот к живому организму позволяют надеяться на высокий лечебный (в частности, антимикробный) эффект и низкую токсичность соответствующих комплексных соединений. Поэтому исследования в этой области необходимы и важны.
Следует отметить, что внимание, которое уделяется таким комплексам, и особенно комплексам с трифункциональными аминокислотами, определяется также и теоретическим интересом в связи с выяснением влияния на состав и строение образующихся комплексов полифункционального строения аминокислот. Возможность различных способов координации трифункциональных аминокислот обусловливает многообразие образующихся комплексов различного строения и свойств, которые также будут зависеть от взаимного расположения функциональных групп в аминокислоте.
Эти основания определяют актуальность настоящего исследования комплексообразования серебра с трифункциональными аминокислотами -глутаминовой кислотой, триптофаном, аргинином и гистидином.
Работа выполнена в соответствии с планами НИР Института по проекту «Теоретические и экспериментальные исследования реакций комплексообразования и окислительно-восстановительных превращений благородных, редких и цветных металлов в важных для гидрометаллургии средах» (Гос. per. № 01.960.004621).
Цель работы. Систематическое исследование комплексообразования серебра с рядом аминокислот, содержащих три различные функциональные группы, в биологически важных нейтральных водных растворах с использованием препаративного и физико-химических методов исследования и биологические испытания синтезированных комплексов.
Научная новизна работы
Синтезированы и изучены методами элементного анализа, ИК-спектроскопии, дериватографии, рентгенофазового анализа, растворимости, рН-метрии, антимикробных тестов четыре новых комплексных соединения серебра (1) с трифункциональными аминокислотами — глутаминовой кислотой, триптофаном, аргинином, гистидином; изучен состав комплексов в твёрдом состоянии и в растворе, в том числе в гетерогенной системе «жидкость-твёрдое», подтверждено наличие в составе синтезированных полиядерных комплексов серебра с триптофаном, аргинином и гистидином гидроксильной группы.
Найдено цепочечно-разветвлённое полимерное строение комплекса с глутаминат-ионом [Ag2Glu]n, линейно-цепочечное полимерное строение [Ag3Trp2OH] п с триптофанат-ионом в качестве N—О-мостиков и гидроксо-мостиками.
Обнаружено хелатообразование донорными атомами азота в комплексах в твёрдом состоянии [Ag2LOH] анионов аргинина и гистидина наряду с мостиковой N-G-координацией. В растворах для комплексов [AgL] хелатообразование проявляется в виде эффекта упрочнения и аномального усиления кислотных свойств азота аминогруппы гуанндиновой группировки аргинина и азота а-аминогруппы гистидина.
На основании результатов рН-метрического титрования при 298 К и ионной силе 0.5 моль/л получены пробные значения констант равновесия ступенчатого образования комплексов [AgL] и [AgL2], показана необходимость учёта протонирования аминокоординированных аргинина и гистидина в комплексах серебра (I).
Обнаружено аномальное упрочнение комплекса серебра с триптофаном [AgL2] для объяснения которого, а также аналогичных отрицательных ступенчатых эффектов в процессах последовательного комплексообра-зования с бифункциональными аминокислотами, предложена гипотеза о внешнесферной квазибидентатной координации аминокоординированных аминокислотных остатков в модели линейных комплексов с координационным числом 2.
Выполнено исследование антимикробной активности и токсичности соединений серебра с аминокислотами и обсуждено их действие с учётом данных о формах существования данных комплексов в нейтральных водных растворах.
Практическая ценность работы
Разработаны методики синтеза новых комплексных соединений серебра с глутаминовой кислотой [Ag2Glu]n, триптофаном [Ag3Trp2OH]n, аргинином и гис-тидином [Ag2LOH]. В Красноярской государственной медицинской академии на кафедрах микробиологии и фармакологии проведены исследования данных соединений на антимикробную активность и токсичность. На основании полученных результатов и соответствующих Актов испытаний они рекомендованы в качестве субстанций лекарственных антибактериальных средств. Полученные результаты расширяют знания в области координационной химии сведениями о комплексообразовании серебра (1) с трифункциональными аминокислотами. На защиту выносятся: физико-химическое изучение состава, строения и свойств комплексов серебра (1) с аминокислотами, содержащими три различные функциональные группы; идентификация сопряжённых кислотно-основных и хелатных комплексных форм серебра (1) с трифункциональными аминокислотами в биологически важных нейтральных водных растворах и термодинамические оценки констант равновесия их образования; биологические испытания синтезированных соединений.
Апробация работы и публикации
Основные результаты работы представлены на Международных и Всероссийских научных конференциях «Молодёжь и химия» (Красноярск, 1999, 2000), XXXVIII Международной научной студенческой конференции «Студент и научно-технический прогресс» (Новосибирск, 2000), Научной конференции «Физико-химия и технология неорганических материалов» (Красноярск, 2000), а также на конференциях молодых учёных ИХХТ СО РАН и КНЦ (2001). По теме диссертации опубликовано 5 статей, 5 тезисов докладов конференций.
Структура и объём диссертации
Диссертация состоит из введения, литературного обзора, пяти глав экспериментальной части, посвященных описанию методик экспериментов, обсуждению результатов исследований, выводов, списка используе
Источник: www.dissercat.com
Аминокислоты
Аминокислоты – это сложные органические соединения, которые в своей молекуле одновременно содержат аминогруппу и карбоксильную группу.
Аминокислоты представляют собой твердые кристаллические вещества, характеризующиеся высокими температурами плавления и разлагающиеся при нагревании. Они хорошо растворяются в воде. Данные свойства объясняются возможностью существование аминокислот в виде внутренних солей (рис. 1).
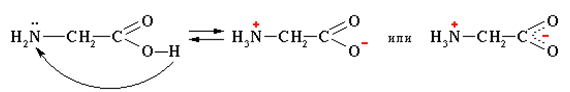
Рис. 1. Внутренняя соль аминоуксусной кислоты.
Получение аминокислот
Исходными соединениями для получения аминокислот часто служат карбоновые кислоты, в молекулу которых вводится аминогруппа. Например, получение их из галогензамещенных кислот
Кроме этого исходным сырьем для получения аминокислот могут служить альдегиды (1), непредельные кислоты (2) и нитросоединения (3):
Химические свойства аминокислот
Аминокислота как гетерофункциональные соединения вступают в большинство реакций, характерных для карбоновых кислот и аминов. Наличие в молекулах аминокислот двух различных функциональных групп приводит к появлению ряда специфических свойств.
Аминокислоты – амфотерные соединения. Они реагируют как с кислотами, так и с основаниями:
Водные растворы аминокислот имеют нейтральную, щелочную и кислотную среду в зависимости от количества функциональных групп. Например, глутаминовая кислота образует кислый раствор, поскольку в её составе две карбоксильные группы и одна аминогруппа, а лизин – щелочной раствор, т.к. в её составе одна карбоксильная группа и две аминогруппы.
Две молекулы аминокислоты могут взаимодействовать друг с другом. При этом происходит отщепление молекулы воды и образуется продукт, в котором фрагменты молекулы связаны между собой пептидной связью (-CO-NH-). Например:
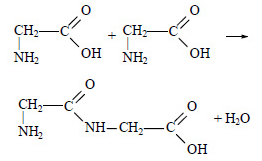
Полученное соединение называют дипептидом. Вещества, построенные из многих остатков аминокислот, называются полипептидами. Пептиды гидролизуются под действием кислот и оснований.
Применение аминокислот
Аминокислоты, необходимые для построения организма, как человек, так и животные получают из белков пищи.
γ-Аминомасляная кислота используется в медицине (аминалон / гаммалон) при психических заболеваниях; на её основе создан целый ряд ноотропных препаратов, т.е. оказывающих влияние на процессы мышления.
ε-Аминокапроновая кислота также используется в медицине (кровоостанавливающее средство), а кроме того представляет собой крупнотоннажный промышленный продукт, использующийся для получения синтетического полиамидного волокна – капрона.
Антраниловая кислота используется для синтеза красителей, например синего индиго, а также участвует в биосинтезе гетероциклических соединений.
Примеры решения задач
| Задание | Напишите уравнения реакций аланина с: а) гидроксидом натрия; б) гидроксидом аммония; в) соляной кислотой. За счет каких групп внутренняя соль проявляет кислотные и основные свойства? |
| Ответ | Аминокислоты часто изображают как соединения, содержащие аминогруппу и карбоксильную группу, однако с такой структурой не согласуются некоторые их физические и химические свойства. Строение аминокислот соответствует биполярному иону: |
Запишем формулу аланина как внутренней соли:
Исходя из этой структурной формулы, напишем уравнения реакций:
Внутренняя соль аминокислоты реагирует с основаниями как кислота, с кислотами – как основание. Кислотная группа – N + H3, основная – COO — .
| Задание | При действии на раствор 9,63 г неизвестной моноаминокарбоновой кислоты избытком азотистой кислоты было получено 2,01 л азота при 748 мм. рт. ст. и 20 o С. Определите молекулярную формулу этого соединения. Может ли эта кислоты быть одной из природных аминокислот? Если да, то какая это кислота? В состав молекулы этой кислоты не входит бензольное кольцо. |
| Решение | Напишем уравнение реакции: |
Найдем количество вещества азота при н.у., применяя уравнение Клапейрона-Менделеева. Для этого температуру и давление выражаем в единицах СИ:
T = 273 + 20 = 293 K;
P = 101,325 × 748 / 760 = 99,7 кПа;
n(N2) = 99,7 × 2,01 / 8,31 × 293 = 0,082 моль.
По уравнению реакции находим количество вещества аминокислоты и её молярную массу.
Определим аминокислоту. Составим уравнение и найдем x:
14x + 16 + 45 = 117;
Из природных кислот такому составу может отвечать валин.
Источник: ru.solverbook.com
Аминокислоты. Свойства аминокислот.
Аминокислоты, белки и пептиды являются примерами соединений, описанных далее. Многие биологически активные молекулы включают несколько химически различных функциональных групп, которые могут взаимодействовать между собой и с функциональными группа друг друга.
Аминокислоты.
Аминокислоты – органические бифункциональные соединения, в состав которых входит карбоксильная группа –СООН, а аминогруппа — NH2.
Разделяют α и β — аминокислоты:

В природе встречаются в основном α-кислоты. В состав белков входят 19 аминокислот и ода иминокислота (С5Н9NO2):


Самая простая аминокислота – глицин. Остальные аминокислоты можно разделить на следующие основные группы:
1) гомологи глицина – аланин, валин, лейцин, изолейцин.
2) серосодержащие аминокислоты – цистеин, метионин.
3) ароматические аминокислоты – фенилаланин, тирозин, триптофан.
4) аминокислоты с кислотным радикалом – аспарагиовая и глутаминовая кислота.
5) аминокислоты с алифатической гидрокси-группой – серин, треонин.
6) аминокислоты с амидной группой – аспарагин, глутамин.
7) аминокислоты с основным радикалом – гистидин, лизин, аргинин.
Изомерия аминокислот .
Во всех аминокислотах (кроме глицина) атом углерода связан с 4-мя разными заместителями, поэтому все аминокислоты могут существовать в виде 2-х изомеров (энантиомеров). Если L и D – энантиомеры.

Физические свойства аминокислот.
Аминокислоты представляют собой твердые кристаллические вещества, хорошо растворимые в воде и мало растворимые в неполярных растворителях.
Получение аминокислот.
1. Замещение атома галогена на аминогруппу в галогензамещеных кислотах:

Химические свойства аминокислот.
Аминокислоты – это амфотерные соединения, т.к. содержат в своём составе 2 противоположные функциональные группы – аминогруппу и гидроксильную группу. Поэтому реагируют и с кислотами и с щелочами:

Кислотно-основные превращение можно представить в виде:

Реагирует с азотистой кислотой:

Реагируют со спиртами в присутствие газообразного HCl:

Качественные реакции аминокислот.
Окисление нингидрином с образованием продуктов, окрашенных в сине-фиолетовый цвет. Иминокислота пролин дает с нингидрином желтый цвет.

2. При нагревании с концентрированной азотной кислотой протекает нитрование бензольного кольца и образуются соединения желтого цвета.
Источник: www.calc.ru