В чистую пробирку вводят 2 капли раствора нитрата серебра и прибавляют каплю аммиака. Образующийся бурый осадок гидроксида серебра растворяют, добавляя избыток (1—2 капли) раствора аммиака. Затем прибавляют каплю раствора формальдегида и медленно подогревают содержимое пробирки над пламенем горелки. При осторожном нагревании содержимое пробирки буреет и на ее стенках может выделиться серебро в виде блестящего зеркального налета (комплексный ион металла восстанавливается до металлического серебра). Альдегид окисляется до кислоты, которая образует аммониевую соль. Химизм процесса:
Сформулируйте вывод по работе.
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Самое популярное на сайте:
Концепции происхождения человека Человек, его место и роль в едином социоприродном комплексе. 1. Концепции происхождения человека. 2. Сходства и различия человека и.
Предмет и метод образовательного права Общая характеристика образовательного права и образовательной системы Предмет и метод образовательного права Учебная программа по.
49. Сложные эфиры (часть 3)
Формы и виды страхования Выделяют следующие формы страхования: 1) добровольное 2) обязательное Обязательнымhttps://studopedia.ru/5_61391_opit—okislenie-aldegidov-ammiachnim-rastvorom-oksida-serebra-reaktsiya-serebryanogo-zerkala.html» target=»_blank»]studopedia.ru[/mask_link]
12*. Для полного гидролиза 22,2 г смеси двух сложных эфиров потребовалось 168 г 10%-ного раствора гидроксида калия. При добавлении к такому же количеству смеси избытка аммиачного раствора оксида серебра выделилось 21,6 г осадка. Определите строение сложны
Одна из кислот, образующих эфир, — муравьиная,т.к. реагирует с оксидом серебра.

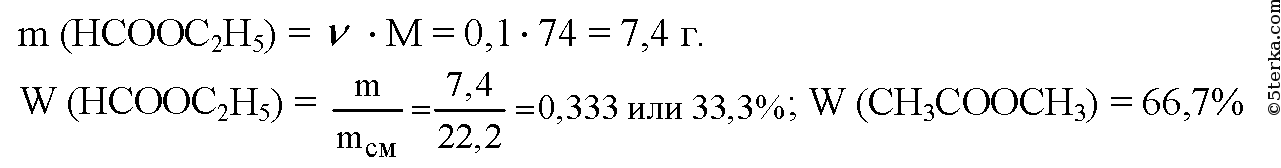
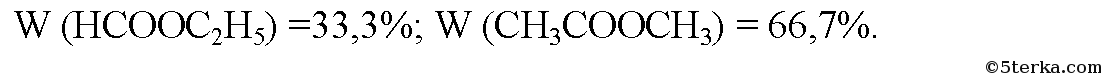
Источник:

Решебник по химии за 10 класс (О.С.Габриелян, 2002 год),
задача №12
к главе «Глава 4. Кислородсодержащие соединения. § 21. Сложные эфиры. Жиры».
Источник: 5terka.com
Глюкоза способна образовывать простые и сложные эфиры. Наиболее легко происходит замещение полуацетального (гликозидного) гидроксила:
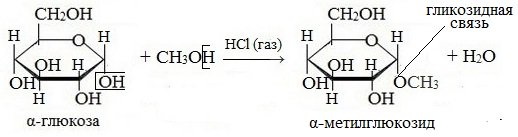
Простые эфиры получили название гликозидов.
В более жестких условиях (например, с CH3-I ) возможно алкилирование и по другим оставшимся гидроксильным группам.
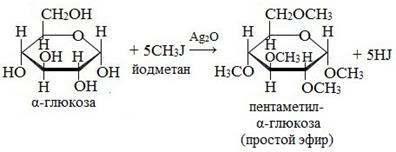
Моносахариды способны образовывать сложные эфиры с карбоновыми кислотами (реакция проходит с ангидридами, а не с самими кислотами) и с минеральными кислотами.
Опыты по химии. Получение сложного эфира

Реакция горения глюкозы.
Фруктоза
Это структурный изомер глюкозы — кетоноспирт:
OH OH OH OH O OH
Кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза. В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы обусловлены наличием кетонной и пяти гидроксильных групп. Так же, как и глюкоза, реагирует с гидроксидом меди (ярко-синий раствор) без нагревания; образует простые и сложные эфиры, горит. При гидрировании фруктозы также получается СОРБИТ. С бромной водой, Сu(OH)2 при нагревании, аммиачным раствором оксида серебра – не реагирует.
Реакция восстановления:
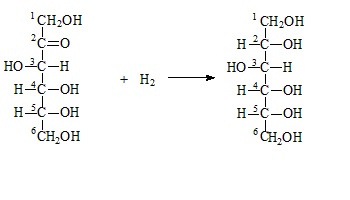
Реакция многоатомных спиртов:
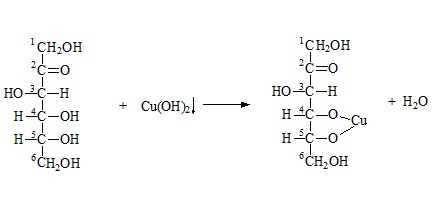
Образование сложных эфиров:
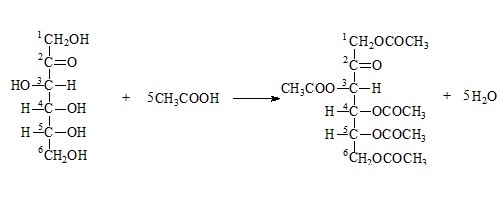
Дисахариды
Дисахариды – это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой).
1. Сахароза (свекловичный или тростниковый сахар) С12Н22О11
Физические свойства и нахождение в природе
1. Она представляет собой бесцветные кристаллы сладкого вкуса, хорошо растворима в воде.
2. Температура плавления сахарозы 160 °C.
3. При застывании расплавленной сахарозы образуется аморфная прозрачная масса – карамель.
4. Содержится во многих растениях: в соке березы, клена, в моркови, дыне, а также в сахарной свекле и сахарном тростнике.
Строение
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом.
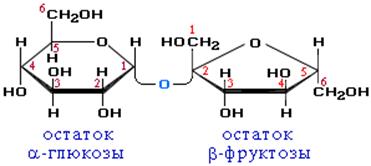
Химические свойства
В молекуле сахарозы гликозидный атом углерода глюкозы СВЯЗАН, поэтому она не образует ОТКЫТУЮ (альдегидную) форму. (альдегидная группа α-глюкозы, входящей в состав сахарозы, участвует в образовании связи с β-фруктозой)
Вследствие этого сахароза не вступает в реакции альдегидной группы – с аммиачным раствором оксида серебра с гидроксидом меди при нагревании. Подобные дисахариды называют невосстанавливающими, т.е. не способными окисляться.
Сахароза реагирует с Сu(OH)2 без нагревания (ярко-синий раствор), с Са(ОН)2 (образуется сахарат кальция).
Сахароза подвергается гидролизу подкисленной водой:
Из числа изомеров сахарозы, имеющих молекулярную формулу С12Н22О11, можно выделить мальтозу и лактозу.
При гидролизе различные дисахариды расщепляются на составляющие их моносахариды за счёт разрыва связей между ними (гликозидных связей):
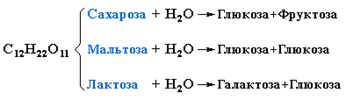
Таким образом, реакция гидролиза дисахаридов является обратной процессу их образования из моносахаридов.
Применение сахарозы
· В кондитерской промышленности;
· Получение искусственного мёда
Мальтоза
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
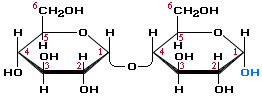
Мальтоза – является восстанавливающим дисахаридом и вступает в реакции, характерные для альдегидов.
2. К восстанавливающим сахаром относятся также целлобиоза
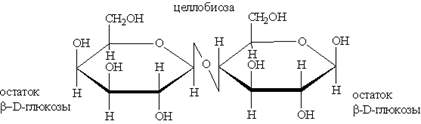
и лактоза

Эти дисахариды так же могут гидролизоваться.
Полисахариды.
Полисахариды — это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные представители — крахмал и целлюлоза — построены из остатков одного моносахарида — глюкозы. Крахмал и целлюлоза имеют одинаковую молекулярную формулу (C6H10O5)n, но совершенно различные свойства. Это объясняется особенностями их пространственного строения.
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы (выделена цветом):

Крахмал.
Крахмалом называется смесь двух полисахаридов, построенных из остатков циклической α-глюкозы.
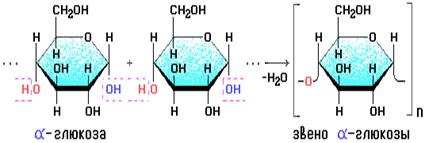
В его состав входят:
· амилоза (внутренняя часть крахмального зерна) – 10-20%
· амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200-1000 остатков α-глюкозы (средняя Mr=160 000) и имеет неразветвленное строение.

Макромолекула амилозы представляет собой спираль, каждый виток которой состоит из 6 звеньев α-глюкозы.

Свойства крахмала:
1. Гидролиз крахмала: при кипячении в кислой среде крахмал последовательно гидролизуется.
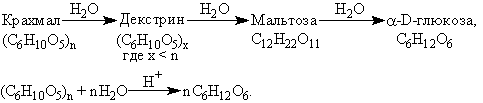
2. Крахмал не дает реакцию “серебряного зеркала” и не восстанавливает гидроксид меди (II).
Дата добавления: 2021-06-02 ; просмотров: 887 ; Мы поможем в написании вашей работы!
Источник: studopedia.net