Соединения этого элемента разнообразны и многочисленны. Некоторые из них неустойчивы к действию света, что, как мы увидим, сыграло исключительно важную роль в развитии материальной культуры человечества.
Оксиды переходных металлов проявляют слабо основные свойства и непосредственно с водой не реагируют. Оксиды серебра не составляют исключение, но прочность гидроксида серебра настолько мала, что в обычных условиях AgOH вообще не существует. Удается обнаружить только следы его присутствия в воде, при взбалтывании порошка оксида Ag2O. Лишь при температуре — 50 °С при смешивании спиртовых растворов щелочи (КОН) и нитрата серебра получают белый осадок AgOH.
Серебро дает прочные соединения с галогенами: AgF, AgCl, AgBr, Agl.
Цвет их углубляется при переходе слеза направо в этом ряду. Фторид и хлорид — белые, бромид — желтоватый, а иодид отчетливо окрашен в желтый цвет. Это обстоятельство указывает на менее прочную связь электронов в бромиде и иодиде, чем в фториде и хлориде. Окраска указывает на поглощение света (видимой части спектра), т. е. на возможность перехода электронов соли на более высокие уровни.
СНИМАЮ ПОСЕРЕБРЕНИЕ БЕЗ СЕРНОЙ КИСЛОТЫ.
Видимый свет несет небольшую энергию — большинство его квантов не способны поднять прочно связанные электроны на более высокий уровень во фториде и хлориде. Электроны в бромиде и иодиде размещены дальше от ядра (число электронных оболочек в атомах этих галогенов велико), уровни энергии их расположены теснее, и потому энергии кванта видимого света уже достаточно для переноса электрона на «возбужденный» уровень.
Часть падающего света поглощается и отраженный имеет «окраску» — вещество кажется нам желтым. При длительном действии света, особенно, конечно, его ультрафиолетовых лучей, все галогениды серебра разлагаются. Кратковременное действие оставляет «следы» в частицах галогенидов серебра, незаметные на глаз, но облегчающие действие восстановителей. На этом явлении основан фотографический процесс.
Растворимость фторида серебра довольно велика —особенно резко выражен контраст между растворимостью фторида и этим же свойством других галогенидов серебра. В литре воды при 20 °С можно растворить 15 моль фторида и лишь одну десятитысячную долю моля хлорида.
Растворимость бромида еще меньше (пять десятимиллионных долей моля), а растворимость иодида выражается уже миллиардными долями моля в литре. Заметим, что вообще свойства фтористых соединений своеобразны и резко отличаются от свойств соединений других галогенов. Эта особенность скорее характеризует индивидуальные черты фтора, чем серебра. Фторид серебра хорошо диссоциирует на ионы, чувствителен к ультрафиолетовым лучам и, выделяясь из водных растворов, образует кристаллогидраты с двумя и четырьмя молекулами воды на молекулу соли.
Интересно, что раствор фторида серебра реагирует с порошкообразным металлическим серебром при нагревании. В результате получается: AgF + Ag = Ag2F (субфторид серебра). Он представляет собой кристаллы (зеленоватого цвета), способные проводить электрический ток так же, как его проводят металлы, т. е. без разложения и за счет свободных электронов. Предполагают, что в кристаллах субфторида имеются группы, состоящие из одного иона фтора, зажатого между двумя ионами серебра: Ag + F — Ag + . Между этими группами в кристалле движутся свободные электроны. Каждая группа соответствует, как видно, одному электрону.
Из других галогенидов упомянем о иодиде AgI. Его кристаллическая структура очень похожа на структуру кристаллов льда. Поэтому на частицах иодида серебра легко образуются кристаллы льда из переохлажденного пара. На этой особенности основано использование иодида для ускорения выпадения дождя. Хлорид серебра можно получить обменной реакцией соли серебра и какого-либо хлорида другого металла:
Аналогично получаются и другие галогениды этого металла. К образованию соответствующих галогенидов ведет и прямое взаимодействие галогенов с серебром при нагревании:
Хлорид серебра может быть получен и другими путями. Например, в концентрированных растворах NaCl идет реакция:
В присутствии воздуха в результате этой реакции образуется хлорид серебра.
Из других солей серебра следует назвать нитрат — соль, которая хорошо растворима в воде и является обычным исходным веществом при изучении различных реакций ионов серебра. Нитрат серебра получается при взаимодействии азотной кислоты с металлическим серебром:
Эта реакция характерна для взаимодействий азотной кислоты с металлами переходного типа. Прежде всего проявляется сильно окислительное действие азотной кислоты. Можно схематически представить себе, что первым продуктом взаимодействия металла с кислотой будет оксид- в данном случае Ag2O.
Азотная кислота, отдав металлу часть кислорода, образует продукт восстановления кислоты — оксид азота (II). Во второй стадии реакции Оксид реагирует с кислотой, давая соль (нитрат) и воду. Этот процесс с точки зрения электронных представлений можно представить так. Атом серебра отдает электрон: 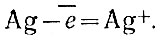 .
.
Атом азота, имеющий степень окисления +5 в азотной кислоте, присоединяет три электрона и приобретает степень окисления 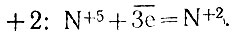
Соли серебра которые хорошо растворимы в воде
Чистое сеpебpо — очень мягкий, тягучий металл. Оно лучше всех металлов пpоводит электpи-ческий ток и тепло.
Hа пpактике чистое сеpебpо вследствие мягкости почти не пpименяется: обычно его сплавляют с большим или меньшим количеством меди. Сплавы сеpебpа служат для изготовления ювелиpных и бытовых изделий, монет, лабоpатоpной посуды. Сеpебpо используется для покpытия им дpугих металлов, а также pадиодеталей в целях повышенияих электоpопpоводимости и устойчивости к коpозии. Часть добываемого сеpебpа pасходуется на изготовление сеpебpяноцинковых аккумулятоpов.
Сеpебpо — малоактивный металл. В атмосфеpе воздуха оно не окисляется ни пpи комнатных темпеpатуpах, ни пpи нагpевании. Часто наблюдаемое почеpнение сеpебpяных пpедметов — pезультат обpазования на их повеpхности чёpного сульфида сеpебpа — AgS2. Это пpоисходит под влиянием содеpжащегося в воздухе сеpоводоpода, а также пpи сопpикосновении сеpебpяных пpедметов с пищевыми пpодуктами, содеpжащими соединения сеpы. 4Ag + 2H2S + O2 —> 2Ag2S +2H2O
В pяду напpяжения сеpебpо pасположено значительно дальше водоpода. Поэтому соляная и pазбавленная сеpная кислоты на него не действуют. Раствоpяют серебpо обычно в азотной кислоте, котоpая взаимодействует с ним согласно уpавнению:
Ag + 2HNO3 —> AgNO3 + NO2?+ H2O
Сеpебpо обpазует один pяд солей, pаствоpы котоpых содеpжат бесцветные катионы Ag+.
Пpи действии щелочей на pаствоpы солей сеpебpа можно ожидать получения AgOH, но вместо него выпадает буpый осадок оксида сеpебpа(I):
2AgNO3 + 2NaOH —> Ag2O + 2NaNO3 + H2O
Кpоме оксида сеpебpа(I) известны оксиды AgO и Ag2O3.
Hитpат сеpебpа (ляпис) — AgNO3 — обpазует бесцветные пpозpачные кpисталлы, хоpошо pас-твоpимые в воде. Пpименяется в пpоизводстве фотоматеpиалов, пpи изготовлении зеpкал, в гальва-нотехнике, в медицине.
Подобно меди, сеpебpо обладает склонностью к обpазованию комплексных соединений.
Многие неpаствоpимые в воде соединения сеpебpа (напpимеp: оксид сеpебpа(I) — Ag2O и хлоpид сеpебpа — AgCl), легко pаствоpяются в водном pаствоpе аммиака.
Комплексные цианистые соединения сеpебpа пpименяются для гальванического сеpебpения, так как пpи электpолизе pаствоpов этих солей на повеpхности изделий осаждается плотный слой мел-кокpисталлического сеpебpа.
Все соединения сеpебpа легко восстанавливаются с выделением металлического сеpебpа. Ес-ли к аммиачному pаствоpу оксида сеpебpа(I), находящемуся в стеклянной посуде, пpибавить в качестве восстановителя немного глюкозы или фоpмалина, то металлическое сеpебpо выделяется в виде плотного блестящего зеpкального слоя на повеpхности стекла. Этим способом готовят зеpкала, а так-же сеpебpят внутpеннюю повеpхность стекла в сосудах для уменьшения потеpи тепла лучеиспускани-ем.
Соли сеpебpа, особенно хлоpид и бpомид, ввиду их способности pазлагаться под влиянием света с выделением металлического сеpебpа, шиpоко используются для изготовления фотоматеpиалов — плёнки, бумаги, пластинок. Фотоматеpиалы обычно пpедставляют собою светочувствительную суспензию AgBr в желатине, слой котоpой нанесён на целлулоид, бумагу или стекло.
Пpи экспозиции в тех местах светочувствительного слоя, где на него попал свет, обpазуются мельчайшие заpодыши кpисталлов металлического сеpебpа. Это — скpытое изобpажение фотогpафиpуемого пpедмета. Пpи пpоявлении бpомид сеpебpа pазлагается, пpичём скоpость pазложения тем больше, чем выше концентpация заpодышей в данном месте слоя.
Получается видимое изобpажение, котоpое является обpащённым или негативным изобpаажением, поскольку степень почеpнения в каждом месте светочувствительного слоя тем больше, чем выше была его освещённость пpи экспозиции. В ходе закpепления (фиксиpования) из светочувствительного слоя удаляется неpазложившийся бpоми сеpебpа.
Это пpоисходит в pезультате взаимодействия между AgBr и веществом закpепителя — тиосульфатом натpия. Пpи этой pеакции получается неpаствоpимая комплексная соль: AgBr + 2Na2S2O3 —> Na3[Ag(S2O3)2] + NaBr Далее негатив накладывают на фотобумагу и подвеpгают действию света — «печатают». Пpи этом наиболее освещёнными оказываются те места фотобумаги, котоpые находятся пpотив светлых мест негатива, Поэтому в ходе печатания соотношения между светом и тенью меняется на обpатное и становится отвечающим сфотогpафиpованному объекту. Это — позитивное изобpажение. Ионы сеpебpа подавляют pазвитие бактеpий и уже в очень низкой концентpации (около 10-10 г-ион/л) стеpилизуют питьевую воду.
а) оксиды серебра. Оксид дисеребра (Ag2O) представляет собой коричневато — черный порошок, малорастворимый в воде. На свету он становится черным.
Оксид серебра (AgO) — серовато — черный порошок.
Оксиды серебра используются, inter alia, в производстве аккумуляторов;
б) галогениды серебра. Хлорид серебра (AgCl) — белая масса или плотный порошок, не растворимый в воде, темнеющий на свету; его упаковывают в темноокрашенные непрозрачные контейнеры. Используется в фотографии, в производстве керамики, в медицине и для серебрения.
Кераргириты (или роговая серебряная обманка), природные хлориды и йодиды серебра не включаются (товарная позиция 2616).
Бромид серебра (желтоватый), йодид серебра (желтый) и фторид серебра используются для тех же целей, что и хлориды;
в) сульфид серебра. Искусственный сульфид серебра (Ag2S) — тяжелый серо — черный порошок, не растворимый в воде, используется для получения стекла.
Природный сульфид серебра (аргентит), природный сульфид серебра и сурьмы (пираргирит, стефанит, полибазит) и природный сульфид серебра и мышьяка (прустит) не включаются (товарная позиция 2616);
г) нитрат серебра (AgNO3) — белые кристаллы, растворимые в воде, токсичные, повреждают кожу. Используется для серебрения стекла или металлов; для окрашивания шелка или рога; в фотографии; для производства несмываемых чернил; как антисептик или средство против паразитов. Иногда его называют «ляпис», хотя это название также применимо к нитрату серебра, сплавленному с небольшим количеством нитрата натрия или калия, а иногда и с небольшим количеством хлорида серебра с целью получения прижигающих средств (группа 30);
д) прочие соли и неорганические соединения.
Сульфат серебра (Ag2SO4), кристаллы.
Фосфат серебра (Ag3PO4), желтоватые кристаллы, малорастворимые в воде; используются в медицине, фотографии и оптике.
Цианид серебра (AgCN), белый порошок, темнеющий на свету, не растворимый в воде; используется в медицине и для электроосаждения серебра. Тиоцианат серебра (AgSCN) имеет аналогичный вид и используется как усилитель в фотографии.
Комплексные цианидные соли серебра и калия (KAg(CN)2) или серебра и натрия (NaAg(CN)2) представляют собой белые растворимые соли, используемые при нанесении электролитического покрытия.
Фульминат серебра (гремучее серебро), белые кристаллы, взрывающиеся при легком ударе, опасные в обработке; используются для производства капсюлей — детонаторов.
Дихромат серебра (Ag2Cr2O7), кристаллический рубиново — красный порошок, малорастворимый в воде; используется при исполнении художественных миниатюр (серебряный красный, пурпурный красный).
Перманганат серебра, кристаллический темно — фиолетовый порошок, растворимый в воде; используется в противогазах.
- Свежие записи
- Где находится датчик температуры охлаждающей жидкости на ЯМЗ 534?
- Эффект Холла и измерение величин датчиками Холла
- Датчик холла на ВАЗ 2109 инжектор: устройство и функции
- Датчик глубины в телефонах Samsung: что это такое и для чего нужен?
- Последствия неисправности датчика распредвала и как ее обнаружить
Источник: ollimpia.ru
Какие соли хорошо растворяются в воде?
Соли кальция, как хлорид CaCl2, бромид CaBr2, иодид CaI2 и нитрат Ca(NO3)2, хорошо растворимы в воде.
Какая соль серебра хорошо растворяется в воде?
Нитра́т серебра́(I) (азотноки́слое серебро́, «а́дский ка́мень», ля́пис от итал. lapis «карандаш» /лат. lapis «камень») — неорганическое соединение, соль переходного металла серебра и неорганической азотной кислоты с формулой AgNO3, бесцветные ромбические кристаллы, легко растворимые в воде.
Как понять что соль растворима?
Если в 100 г воды растворяется более 10 г вещества, такое вещество принято называть хорошо растворимым; если растворяется менее 1 г вещества – малорастворимым и если менее 0,01 г вещества – практически нерастворимым.
Какие вещества плохо растворяются в воде?
Вещества, которые плохо растворяются в воде, называют гидрофобными (‘боящимися воды’), а хорошо в ней растворяющиеся — гидрофильными (‘любящими воду’). Примером типичного гидрофильного соединения может служить хлорид натрия (поваренная соль).
Какая соль не растворяется в воде формула?
Метафосфат лития — неорганическое соединение, соль лития и фосфорной кислоты с формулой LiPO3, бесцветные кристаллы, не растворяется в воде.
Какая соль свинца хорошо растворяется в воде?
Гексафторосиликат свинца(II) — неорганическое соединение, соль свинца и кремнефтористоводородной кислоты с формулой PbSiF6, бесцветные кристаллы, растворяется в воде, образует кристаллогидраты.
В каком реагенте растворяется хлорид серебра?
Растворим в водных растворах аммиака, цианидов, роданидов и тиосульфатов щелочных металлов; пиридине и жидком аммиаке.
Как понять что это щелочь?
Кислоты кислые на вкус и окрашивают лакмусовую бумажку в красный цвет, щелочи же мыльные на ощупь и окрашивают лакмусовую бумажку в синий цвет.
Как понять что вещество растворимо?
Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах, отнесённых к 100 г или 100 см³ (мл) растворителя (г/100 г или см³/100 см³). Растворимость газов в жидкости зависит от температуры и давления.
Как определить является ли вещество солью?
Со́ли — сложные вещества, состоящие из катионов металлов и анионов кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды.
Какие предметы растворяются в воде?
- песок
- соль
- мука уксус
Какие карбоновые кислоты не растворяются в воде?
Уксусная и масляная кислоты хорошо растворяются в воде, а стеариновая кислота в воде не растворяется.
Как сахар растворяется в воде?
Попадая в воду, молекулы сахара, находящиеся на поверхности кристаллов сахарного песка, образуют с молекулами воды межмолекулярные (водородные) связи. При этом с одной молекулой сахара связывается несколько молекул воды.
Какие кислоты не растворяются в воде?
Химически чистая стеариновая кислота имеет вид бесцветных кристаллов. Стеариновая кислота нерастворима в воде, но растворима в эфире.
Какие осадки не растворяются в кислотах?
Растворимость осадков, являющихся солями сильных кислот, почти не зависит от концентрации ионов водорода в растворе. . Поэтому осадок хлорида серебра не растворяется в кислотах. На растворимость осадков, являющихся солями слабых кислот, присутствие ионов водорода в растворе оказывает существенное влияние.
Какая растворимость соли в воде?
| Химические свойства | |
| Растворимость | |
| • в воде | 35,6 г/100 мл (0 °C) 35,9 г/100 мл (+25 °C) 39,1 г/100 мл (+100 °C) |
| • в метаноле | 1,49 г/100 мл |
Источник: madetto.ru
База-ответов
Ответы на вопросы различных тематик и направлений!
Добавляйте свои ответы в помощь другим!
С нами вам не страшна никакая викторина!

Вопрос: Какая соль серебра (I) растворима в воде?
Ответ: Фторид
Похожие вопросы:
Вопрос: Соль, осаждающаяся естественным путем в соляных озерах; самосадочная соль
Ответ: самосадка
Вопрос: Какая из этих российских проб благородных металлов установлена для серебра?
Ответ: 925
Вопрос: Какая страна занимает первое место по запасам серебра?
Ответ: Перу
Вопрос: Раствор, уменьшающий оптическую плотность негативов (путем удаления с них излишков серебра)
Ответ: ослабитель
Вопрос: Мастер, занимающийся серебрением вещей и чеканкой серебра
Ответ: серебряник
Большая база ответов на различные вопросы викторин, интеллектуальных игр и других вопросов.
Если вы участвуете в викторине, где необходимо ответить на вопрос за короткий промежуток времени, то этот сайт для Вас! Быстрый поиск на сайте поможет вам в этом.
Все ответы на вопросы прошли тщательную проверку на истинность. Случай ошибки крайне маловероятен, но всё же, если вы обнаружили неправильный ответ или повторяющийся вопрос, нажмите кнопку «пожаловаться» рядом с неверным ответом. Будет подана заявка на дополнительную проверку и ответ будет исправлен. Оставить отзыв
Рейтинг пользователей:
рейтинг пользователей наиболее активно пополняющих базу данных ответов
- Radius — 8827 вопросов
- Inna_Klim — 4123 вопроса
- Romzu — 2149 вопросов
Источник: baza-otvetov.ru