Правильный ответ на вопрос «Растворенный сульфат меди будет взаимодействовать с: а. серебром, б. соляной кислотой, в. магнием, г. оксидом железа, д. оксидом калия . » по предмету Химия. Развернутая система поиска нашего сайта обязательно приведёт вас к нужной информации. Как вариант — оцените ответы на похожие вопросы. Но если вдруг и это не помогло — задавайте свой вопрос знающим оппонентам, которые быстро дадут на него ответ!
Новые вопросы по химии
При сжигании этана образовался углекислый газ объемом 32 л. Какие объемы исходных газов было использовано? (н. у.)
Запишите уравнения химических реакций, характеризующие свойства: а) MgO и SO3; б) Mg (OH) 2 и H2SO4. Уравнения реакций с участием электролитов запишите также в ионной форме.
Осуществите превращения Cu—CuO—CuSo4—Cu (OH) 2—CuCl2
Ксилол 100% консентрация, чем разбавить чтоб получить 40%
Запишите схемы образования химических связей для веществ состав которых отображают формулами kcl и cl2
МЕДНЕНИЕ СТАЛЬНЫХ ДЕТАЛЕЙ ЗА 2 СЕКУНДЫ!!!
Главная » Химия » Растворенный сульфат меди будет взаимодействовать с: а. серебром, б. соляной кислотой, в. магнием, г. оксидом железа, д. оксидом калия
Источник: abiturient.pro
Задания 32. Характерные химические свойства неорганических веществ

С какими из перечисленных ниже веществ будет взаимодействовать раствор сульфата меди (II)?
1) гидроксид калия (раствор)
3) нитрат бария (раствор)
4) оксид алюминия
5) оксид углерода (IV)
6) соляная кислота
7) фосфат натрия (раствор)
Ответ: 1237
Пояснение:
Сульфат меди (II) CuSO4 – растворимая в воде соль синего цвета, взаимодействует с растворимыми основаниями, кислотами и солями с образованием осадков или газов. Кроме того, сульфат меди вступает с металлами, стоящими в электрохимическом ряду напряжений металлов до меди, т.е. с теми, которые способны заместить медь в соли. Следовательно, из предложенного списка сульфат меди реагирует
— с гидроксидом калия KOH с образованием синего осадка Cu(OH)2:
— железом, так как оно стоит перед медью в электрохимическом ряду напряжений металлов. В результате реакции выделяется медь, железо окисляется до степени окисления +2:
— нитратом бария с образованием не растворимого в воде белого осадка — сульфата бария BaSO4:
— фосфатом натрия с образованием не растворимого в воде голубого осадка – фосфата меди (II):
ACE94D
Какие гидроксиды не взаимодействуют со щелочами?
Ответ:134
Пояснение:
Амфотерные гидроксиды – сложные вещества, в зависимости от условий проявляющие либо кислотные, либо основные свойства, т.е. амфотерные гидроксиды реагируют с кислотами и щелочами.
АФФИНАЖ САМЫЙ ДОСТУПНЫЙ СПОСОБ ИЗВЛЕЧЕНИЕ СЕРЕБРА СМОЖЕТ ЛЮБОЙ НОВИЧОК.
Среди представленных ответов амфотерными гидроксидами являются гидроксид хрома (III) и гидроксид цинка.
Fe(OH)2, Ca(OH)2 и Mg(OH)2 – основные гидроксиды, не взаимодействуют с веществами, обладающими основными свойствами (Mg, Ca – элементы главной подгруппы II группы, Fe 2+ — обладает основными свойствами).
ACE94D
Какие гидроксиды не взаимодействуют со щелочами?
Ответ:134
Пояснение:
Амфотерные гидроксиды – сложные вещества, в зависимости от условий проявляющие либо кислотные, либо основные свойства, т.е. амфотерные гидроксиды реагируют с кислотами и щелочами.
Среди представленных ответов амфотерными гидроксидами являются гидроксид хрома (III) и гидроксид цинка.
Fe(OH)2, Ca(OH)2 и Mg(OH)2 – основные гидроксиды, не взаимодействуют с веществами, обладающими основными свойствами (Mg, Ca – элементы главной подгруппы II группы, Fe 2+ — обладает основными свойствами).
F33AAC
При обычной температуре магний не взаимодействует с
1) водой в присутствии кислорода
2) растворами щелочей
Ответ: 125
Пояснение:
В присутствии кислорода Mg окисляется до MgO, т.е. металл становится покрытым оксидной пленкой. Оксид магния MgO превращается в гидроксид Mg(OH)2 в горячей воде:
Сульфид магния MgS образуется непосредственно из простых веществ при температуре 800 o C:
Mg + S = MgS (t = 800 o C)
С разбавленными и концентрированными растворами HNO3 и H2SO4 Mg реагирует при комнатной температуре. Поскольку Mg – металл, стоящий в ряду активностей металлов до водорода, в зависимости от концентрации азотной кислоты азот восстанавливается до различных степеней окисления:
С концентрированной серной кислотой активный металл Mg реагирует, в результате сера +6 восстанавливается до -2:
Реакция Mg с разбавленным раствором серной кислоты:
Mg является основным металлом, поэтому не реагирует с основаниями, т.е. с NaOH реакция не проходит.
C5C6B5
При комнатной температуре хром взаимодействует с
Ответ: 13
Пояснение:
В электрохимическом ряду напряжений металлов хром находится до водорода, поэтому он вытесняет водород из растворов неокисляющих кислот:
Концентрированные азотная и серная кислоты пассивируют хром. Хром может растворяться в них лишь при сильном нагревании, образуя соли хрома (III) и продукты восстановления кислоты:
В измельченном раскаленном состоянии хром реагирует с водой, образуя оксид хрома (III) и водород:
С азотом хром реагирует при температуре выше 1000 o C с образованием нитридов:
С водородом не взаимодействует
4DF082
Установите соответствие между реагирующими веществами и продуктами их взаимодействия.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ
Ответ: А-1, Б-4, В-3, Г-6
Пояснение:
А) MgO + SO2 = MgSO3 – реакция соединения (из двух сложных веществ образуется одно более сложное)
Реакция между основным (MgO) и кислотным (SO2) оксидом протекает с образованием средней соли — сульфита магния MgSO3. Оксид серы (IV) соответствует сернистой кислоте H2SO3, поэтому в реакциях с щелочами или основными оксидами образуются соли сернистой кислоты с кислотным остатком SO3 2- — сульфиты.
Б) MgO + SO3 = MgSO4 – реакция соединения (из двух сложных веществ образуется одно более сложное)
Реакция между основным (MgO) и кислотным (SO3) оксидом протекает с образованием средней соли — сульфата магния MgSO4. Оксид серы (VI) соответствует серной кислоте H2SO4, поэтому в реакциях с щелочами или основными оксидами образуются соли серной кислоты с кислотным остатком SO4 2- — сульфаты.
В) MgO + H2SO3 = MgSO3 + H2O– реакция обмена (два сложных вещества – реагенты – обмениваются своими составными частями)
Реакция между основным оксидом (MgO) и сернистой кислотой (H2SO3) протекает с образованием средней соли — сульфита магния MgSO3 – и воды. При взаимодействии сернистой кислоты H2SO3 с щелочами или основными оксидами образуются соли сернистой кислоты с кислотным остатком SO3 2- — сульфиты.
Г) MgO + H2SO4 = MgSO4 + H2O – реакция обмена (два сложных вещества – реагенты – обмениваются своими составными частями)
Реакция между основным оксидом (MgO) и серной кислотой (H2SO4) протекает с образованием средней соли — сульфата магния MgSO4 – и воды. При взаимодействии серной кислоты H2SO4 с щелочами или основными оксидами образуются соли серной кислоты с кислотным остатком SO4 2- — сульфаты.
B40780
Установите соответствие между названием оксида и формулами веществ, с которыми он может взаимодействовать.
НАЗВАНИЕ ОКСИДА
ФОРМУЛЫ ВЕЩЕСТВ
Источник: scienceforyou.ru
5. К раствору, содержащему 40 г сульфата меди(II), прибавили 12 г железных стружек. Рассчитайте, останется ли в растворе сульфат меди(II) после того, как закончится реакция.
5. К раствору, содержащему 40 г сульфата меди(II), прибавили 12 г железных стружек. Рассчитайте, останется ли в растворе сульфат меди(II) после того, как закончится реакция.
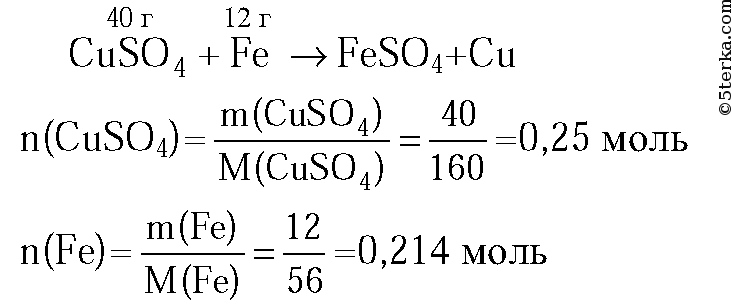
Т.к. CuSO4 находится в избытке, то после окончания реакции он останется в растворе.
Источник:

Решебник по химии за 9 класс (А.М.Радецкий, 2011 год),
задача №5
к главе «Тема I. Электролитическая диссоциация. Работа 4. Расчеты по уравнениям реакций, если одно из реагирующих веществ дано в избытке».
Источник: 5terka.com