Что произойдет в результате действия амииачного раствора оксида серебра на ацетилен (C2H2 + [Ag(NH3)2]OH = ?)? Приведите основные физические параметры вышеуказанного алкина, расскажите о его химических свойствах и способах получения.
Xumuk Админ. ответил 6 лет назад
При пропускании ацетилена через аммиачный раствор оксида серебра (C2H2 + [Ag(NH3)2]OH = ?) или хлорида меди (I) легко образуются ацетилениды серебра и меди, которые выпадают из раствора в осадок:
![]()
![]()
![]()
Как решать ОРГАНИЧЕСКИЕ ЦЕПОЧКИ? Основные типы химических реакций
Ацетилен (этин) представляет собой газ без цвета и запаха, обладает слабым наркотическим свойством. В промышленности ацетилен получают из метана путем высокотемпературного крекинга. Сырьем служит природный газ, который в основном состоит из метана. Другим промышленным способом является получение ацетилена из каменного угля.
Для ацетилена характерны реакции присоединения (галогенирование, гидрогалогенирование, гидратация), окисления и восстановления. Кроме этого алкины проявляют кислотные свойства, т.е. способны образовывать соли – ацетилениды. В результате тримеризации ацетилена – пропускание его над активированным углем при — образуется бензол:
Источник: ru.solverbook.com
Тема 3.4. Ацетиленовые углеводороды (алкины)
Алкины – это углеводороды, содержащие в своей структуре тройную связь. Общая формула ацетиленовых углеводородов СnH2n-2. Атомы углерода при тройной связи находятся в состоянии sp-гибридизации.
Номенклатура. По рациональной номенклатуре производные ацетилена рассматриваются как его замещенные, называются радикалы с прибавлением слова «ацетилен».
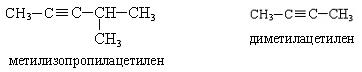
По систематической номенклатуре названия ацетиленовых углеводородов даются от соответствующих предельных углеводородов с заменой окончания на «-ин», нумерацию начинают с того конца, где ближе тройная связь:
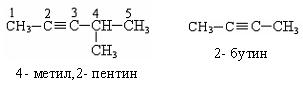
Способы получения. Существует несколько способов получения алкинов.
1. Электрокрекинг метана:
Реакцию проводят электродуговым способом, пропуская метан между электродами с временем контакта 0,1 – 0,01 секунды, чтобы ацетилен не разложился.
Качественные реакции в органической химии | ХИМИЯ ЕГЭ | Лия Менделеева
2. Синтез из углерода и водорода в вольтовой дуге:
3. Окислительный крекинг метана:
4. Синтез из карбида кальция (ацетиленида кальция):
Исходным веществом является СаСО3, разложением которого получается СаО, а затем карбид кальция:
б) СаО+ 3С → СаС2 + СО
5. Синтез из альдегидов:
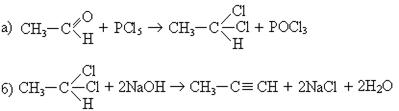
6. Синтез производных ацетилена через амид:
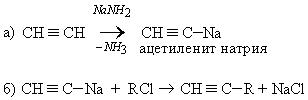
Химические свойства. Атомы углерода по тройной связивалкинах находятсяв состоянии sp-гибридизации и имеют две π-связи:
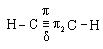
Типичными реакциями ацетиленовых углеводородов, к которым располагает электронная структура ацетилена, являются реакции электрофильного присоединения (АdЕ).
Другим направлением химически реакционной способности являются реакции нуклеофильного присоединения (АdN), возможность протекания которых объясняется большим вкладом s-орбитали в гибридное облако при sp-гибридизации, которое по форме приближается к сфере, а значит, электроны p-связи сильнее притягиваются ядром и не очень доступны для электрофильных частиц.
Кроме того, ацетиленовые углеводороды вступают в реакции замещения, окисления и полимеризации.
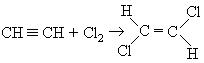
Реакция идет в транс-положение.
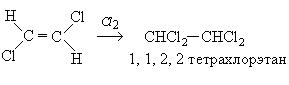
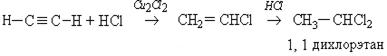
Гидрогалогенирование несимметричных производных ацетилена происходит в соответствии с правилом Морковникова:
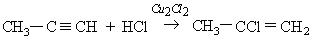
3. Гидрогенизация. В присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород с образованием алкенов, а затем алканов:
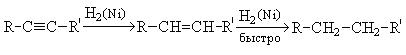
При использовании менее активного катализатора [Pd/CaCO3/Pb(CH3COO)2] гидрирование останавливается на стадии образования алкенов.
4. Гидратация (реакция Кучерова). Присоединение воды происходит в присутствии катализатора, соли ртути (II) и идет через образование неустойчивого непредельного спирта, который изомеризуется в уксусный альдегид:
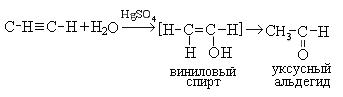
Процесс изомеризации находится в соответствии с правилом Эдьтекова, согласно которому структура гидроксила при двойной связи нестабильна и всегда изомеризуется в структуру, содержащую карбонильную группу. Этот переход называется еще кето-енольной таутометрией. При гидратации производных ацетилена образуются кетоны:
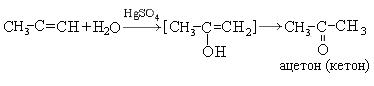
5. Реакция с карбоновыми кислотами:
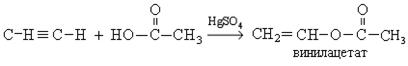
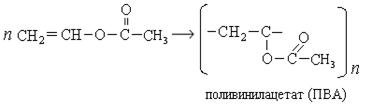
Поливинилацетат используется для изготовления водо-эмульсионных красок, клея, лака.
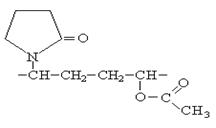
Сополимер винилацетата с винилпиролидоном является основным компонентом лака для волос.
Переэтерификация поливинилацетата метанолом позволяет получить поливиниловый спирт:
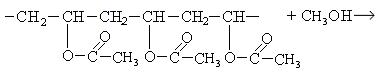
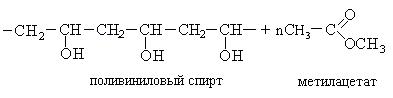
Используется поливиниловый спирт в больших количествах для повышения сохранности фруктов. Образующаяся пленка от поливинилового спирта легко растворяется в воде.
1. Реакция со спиртами:
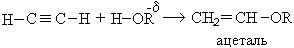
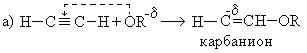
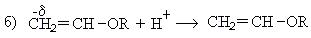
При взаимодействии ацетилена бутанолом получается винилбутиловый эфир, последующая полимеризация которого дает бальзам Шестаковского, используемый как лекарственное средство:
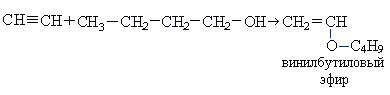
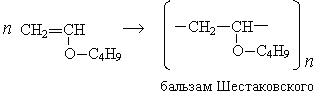
2. Взаимодействие с синильной кислотой:
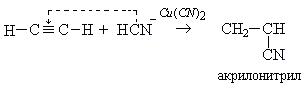
Полимеризацией акрилонитрила получают синтетическое волокно полиакрилонитрил (ПАН):
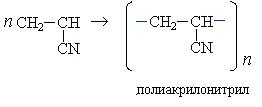
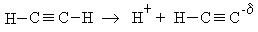
Проявление кислотных свойств ацетилена объясняется именно за счет особенностей sp-гибридизации, когда электроны π-связи сильно притягиваются ядрами атома углерода и атомы водорода практически не удерживаются ими. Кислотность ацетилена можно сравнить в следующих рядах:
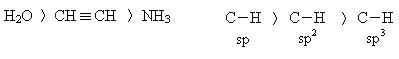
1. Взаимодействие с натрием:
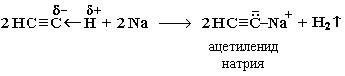
2. Взаимодействие с амидом натрия:
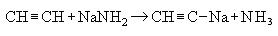
3. Взаимодействие ацетилена (или ) с аммиачными растворами оксида серебра или хлорида меди (I). При взаимодействии ацетилена с аммиачными растворами оксида серебра или хлорида меди выпадают осадки нерастворимых ацетиленидов:
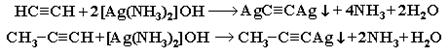
Образование белого осадка ацетиленида серебра (или красно-коричневого – ацетиленида меди ) служит качественной реакцией на концевую тройную связь.
Ацетилениды разлагаются при действии кислот:

В сухом состоянии ацетилениды тяжелых металлов чувствительны к ударам и легко взрываются.
Если тройная связь находится не на конце цепи, то кислотные свойства отсутствуют (нет подвижного атома водорода) и ацетилениды не образуются:
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Источник: studopedia.ru
Свойства алкинов
Это вещества еще с меньшим количеством углерода, чем у алканов и алкенов . Тройная связь определяет и строение молекул, и общую формулу, и химические свойства алкинов.
Для атомов тройной связи характерна Sp-гибридизация. Т.е. тройная связь — это комбинация одной σ- и двух Π-связей:
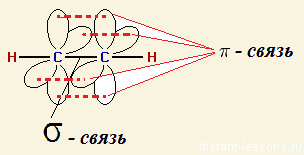
Общая формула:
n = числу атомов углерода.
Название углеводородов строятся из двух частей.
Первая часть «говорит» о количестве атомов углерода, вторая — о тройной связи. У алкинов вторая часть — всегда -ин.
- в качестве основной цепи выбирается та, в которой находится тройная связь, не зависимо от ее размера,
- нумерация идет с того конца, к которому ближе тройная связь
- после окончания -ин ставится номер атома, после которого идет тройная связь.
Изомерия
Соответственно, для алкинов характерны 2 вида изомерии:
- Структурная — изомерия положения тройной связи и изомерия радикалов
- Межклассовая — алкины изомерны акладиенам.
Химические свойства алкинов:
1. Тройная связь, как и двойная , все присоединяет, разрывается, образует двойную связь, если реагент дан в избытке, то реакция может идти до образования одинарной связи:

2. Гидратация — взаимодействие с водой — реакция Кучерова :

3. Качественные реакции алкинов:
Ацетилениды серебра и меди (I) легко образуются и выпадают в осадок при пропускании ацетилена через аммиачный раствор оксида серебра или оксида меди (I) . Эта реакция служит для обнаружения алкинов с тройной связью на конце цепи:

Алкины окисляются различными окислителями, в частности перманганатом калия. При этом раствор перманганата калия обесцвечивается, что служит указанием на наличие тройной связи. При окислении обычно происходит расщепление тройной связи и образуются карбоновые кислоты, перманганат восстанавливается до Mn(2+) — в кислой среде, MnO2 — в щелочной:
С4H6 + [O] → 2CH3COOH
СnH2n-2 + (3n-1)2 O2 → nCO2 + (n-1) H2O
Здесь записано уравнение в общем виде, т.к. во многих задачах требуется определить состав углеводорода — в таких случаях любые реакции лучше записывать в таком — общем виде.
Получение алкинов:
- Из неорганических соединений: CaC2 + 2H2O → Ca(OH)2 + C2H2
- дегидрогалогенирование: СH3-СHBr2 +2KOH (этанол, t) →C2H2 + 2KBr + 2H2O
Пример олимпиадного вопроса (2015 г)
![]()
Общая формула СnH2n-2, что соответствует либо алкинам, либо алкадиенам
Структурные изомеры алкинов:
- СH≡С-СH2-СH3 бутин-1;
- CH3-C≡C-CH3 бутин-2;
Межклассовые — алкадиены:
- СH2=СH-СH=СH2 — бутадиен-1,3
- CH2=C=CH-CH3 — бутадиен-1,2
- в ЕГЭ это вопрос А13 и А14— Строение и свойства углеводородов
- в ГИА (ОГЭ) это B2— Первоначальные сведения об органических веществах: предельных и непредельных углеводородах
Обсуждение: «Свойства алкинов»
Viktoria says:
10.02.2014 в 12:37
Лолита, поясните, пожалуйста, первое задание теста. Исходя из ответов, приведенных ниже, продуктами реакции СаС2+Н2О являются гидроксид кальция и метан. Но верным ответом будет гидроксид кальция и ацетилен?
Лолита Окольнова says:
10.02.2014 в 12:45
Да, продуктами будут гидроксид кальция и ацетилен : CaC2 + 2H2O = Ca(OH)2 + C2H2.
В ответах опечатка закралась. Исправили . Спасибо большое, что обратили внимание!
Andrei says:
02.04.2020 в 12:56
Ацетиленид меди (I) получается при пропускании ацетилена через оксид меди (I) или хлорид меди (I)? А то в тексте написано, что через хлорид, а в уравнении дан оксид
Источник: distant-lessons.ru