Используется в том случае когда нужно удалить покрытие серебра для каких либо целей при этом не растворяя его в кислоте которая может повредить материал .
Для травления серебра электролизом вам потребуется :
1 Материал с которого нужно снять серебро ( провода , по серебренные пластинки и т.д )
2 Любая из этих солей нитрат натрия NaNO 3 , нитрат калияKNO 3 , нитрат аммония NH 4 NO 3
3 Блок питания с постоянным током .
4 Подходящая ёмкость для травления серебра
Описание процесса
В заранее приготовленную ёмкость по размерам материала заливают горячей водой с добавлением нитрата аммония , помещают предмет с которым нужно провести травление и подключают к источнику питания с постоянным током .
Причём материал подключается к положительному разъёму (анод)на блоке питании , а в качестве (катод) или минус используется любой графитовый стержень , если нежелательно востановление металла на катоде рекомендуется в ванне поставить перегородку с небольшим переходом в виде трубки причём трубка должна быть заполнена жидкостью .
Как сделать надпись на металле. Травление металла хлорным железом
Применение .
Применяют для удаления нежелательного серебра на покрытии , а также в некоторых областях промышленности для травления плат .
Вы читаете, статья на тему травление серебра электролизом
Похожие страницы:
Что такое анодное разложение золота Один из самых применяемых в производственных масштабах способ получения золота из его сплавов как с благородными.
КАКИЕ БЫВАЮТ СОЛИ СЕРЕБРА Амид серебра (AgNH2) Антимонид серебра(I) (Ag3Sb) Арсенат серебра(I) (Ag3AsO4) Арсенид серебра(I) (Ag3As).
Нитрат серебра это бесцветные кристаллы которые очень быстро растворяются в воде и некоторых других растворителях, обладает токсичными свойствами. Попадание на.
Электрохимический способ очистки золота или Электрохимический аффинаж золота Используют для получения золота очень высокой пробы , а именно кто может.
СЕРЕБРО ИЗ РАДИОДЕТАЛЕЙ Множество радиодеталей содержит в своём составе серебро , им покрываются внешние и внутренние части для устранения коррозии.
СУЛЬФИД СЕРЕБРА (I) (Ag2S) Свойства . В чистом состоянии имеет серо — чёрный цвет , природный в зависимости от примесей имеет.
Понравилась статья поделись ей
Leave a Comment
Для отправки комментария вам необходимо авторизоваться.
Источник: znaesh-kak.com
Травление серебра в домашних условиях
Так как подобные вопросы возникают нечасто, пусть будет общая тема, мало ли кому еще что понадобится.
Меня же конкретно интересует чем можно стравить серебро с керамики. Вариант с азотной кислотой конечно известен, но ее нет посему отпадает. Множество уверений что хлорное железо тоже травит серебро — не травит, уж не знаю почему, только окрасило в плотный светло-коричневый цвет. Чем еще можно попробовать, учитывая что никаких химмагазинов нет и соответственно, реактивы отсутствуют, только бытовая химия.
Травление металла в домашних условиях. Оригинальный кулон. DIY Часть 1
17.01.2011, 16:10
«Царская водка» — смесь азотной и соляной кислот, уберет все без труда.
17.01.2011, 16:13
Я вроде черным по белому и русским языком написал:
Вариант с азотной кислотой конечно известен, но ее нет посему отпадает.
17.01.2011, 16:44
К сожалению, кроме азотной, подходит нагретая концентрированная серная кислота (кстати с медью то же реагирует).
Если бы серебро окислялось от всего подряд, драгметаллом оно бы не было.:super:
17.01.2011, 16:48
В горячей концентрированной серной кислоте серебро тоже растворяется. Серная кислота — это та, что используется в автомобильных аккумуляторах.
17.01.2011, 16:57
Серная кислота — это та, что используется в автомобильных аккумуляторах.
Спасибо, кэп. :ржач:
Хм, пожалуй надо было на форуме химиков поспрашивать.
Ок, чтобы не читать очевиднейшие ответы, спрошу иначе — кто все-таки травил серебро в хлорном железе? Может ли быть причиной пассивности такого раствора то, что прежде в нем немного травили медь (но для меди раствор очень даже еще активный)?
P.S. Можно еще в соляной кислоте с гидроперитом, но кислот НЕТ.
17.01.2011, 17:17
Попробуйте снять серебро гальванически, если это покрытие на подслое (например, на меди).
Если серебро нанесено диффузионно (вжиганием в керамику), ничто не поможет.
17.01.2011, 17:23
Дело пожалуй в растворе хлорного железа. Серебро в ряду активности стоит после меди. Поэтому и травиться будет дольше.
17.01.2011, 17:26
гальванически
Проблема в том, что так покрытие не снимешь целиком, протравливается кусками — далее остаются «отключенные» от напряжения островки, не будешь же каждое пятнышко отдельно запитывать. -|
Дело пожалуй в растворе хлорного железа. Серебро в ряду активности стоит после меди. Поэтому и травиться будет дольше.
Тут даже не дольше — вообще не травилось! Может и вправду из-за присутствия меди в растворе. Попробую сделать чистый раствор ХЖ, посмотрю что получится.
17.01.2011, 17:29
Я когда то давно травил в хлорке. Помню, что реакция шла медленнее, я грел раствор.
17.01.2011, 17:34
«Царская водка» — смесь азотной и соляной кислот, уберет все без труда.
Серебро в царской водке не растворяется
17.01.2011, 17:36
Проблема в том, что так покрытие не снимешь целиком, протравливается кусками
Лечится постепенным погружением в раствор. При этом подвеска подключается в высшей точке серебряного полигона.
При большой плотности тока и медленном погружении процесс идет крайне интенсивно, прямо на границе раздела сред.
17.01.2011, 17:42
Лечится постепенным погружением в раствор. При этом подвеска подключается в высшей точке серебряного полигона.Хм, как вариант учту, спасибо!
Я когда то давно травил в хлорке.
В «хлорке» — это что? Настой хлорной извести? Гипохлорит натрия? Соляная кислота?
Приготовил свежий раствор ХЖ, посмотрим, будет ли толк.
17.01.2011, 17:43
Меня же конкретно интересует чем можно стравить серебро с керамики.
Вариант с азотной кислотой конечно известен, но ее нет посему отпадает. Множество уверений что хлорное железо тоже травит серебро — не травит, уж не знаю почему, только окрасило в плотный светло-коричневый цвет. Чем еще можно попробовать, учитывая что никаких химмагазинов нет и соответственно, реактивы отсутствуют, только бытовая химия.
Мои женщины как-то решили снять налет сернистого серебра со своих цепочек и положили их на ночь в баночку с нашатырным спиртом.Хорошо,что цепочки оказались посеребренными, иначе, степень их огорчения была-бы больше.Наутро из баночки были вынуты медные цепочки,мне осталось им только посочувствовать 😥
17.01.2011, 17:51
нашатырным спиртом
Аммиачный раствор? Наверняка в хозмагах должен быть, посмотрю.
17.01.2011, 17:59
Ок, чтобы не читать очевиднейшие ответы, спрошу иначе — кто все-таки травил серебро в хлорном железе?
В советское время существовала промышленная технология изготовления печатных плат так называемым позитивным методом. Так вот при этом методе на медной поверхности заготовки из фольгированного стеклотекстолита формировался рисунок проводников, закрытых гальваническим серебром. Далее шло травление в хлорном железе. Пробельные места (медь) стравливались, проводники, покрытые серебром, оставались нетронутыми. Отсюда мораль: хлорным железом — нечего и пытаться.
17.01.2011, 18:09
Точнее — 9%(afair) водный раствор аммиака.
17.01.2011, 18:09
Добрый вечер ! Концентрированная азотка с подогревом , пару секунд и всё готово ! Да , только на улице . Беречь легкие надо !
17.01.2011, 18:11
Отсюда мораль: хлорным железом — нечего и пытаться.
Угу. Только почему то в половине справочников указано наоборот.
Однако в окислительной среде (в азотной, горячей концентрированной серной кислоте, а также в соляной кислоте в присутствии свободного кислорода) серебро растворяется: Ag + 2HNO3(конц.) = AgNO3 + NO2↑ + H2O. Растворяется оно и в хлорном железе, что применяется для травления:
Ag + FeCl3 = AgCl + FeCl2
17.01.2011, 18:14
Я, когда мне нужна серная к-та (да и азотная тоже), иду на рынок, где торгуют автозапчастями. Там у нас это все почему-то есть в продаже.
17.01.2011, 18:17
Там у нас это все почему-то есть в продаже.
И у нас есть. В виде готового электролита. Такой концентрацией никакое серебро не травится, хоть кипяти, проверено. Что до азотной, то мне сложно объяснить, что она на авторынке может делать.
17.01.2011, 18:25
Не нужно копипастить выдержки из химических энциклопедий, ок? Вопрос вполне четко поставлен, остальное флуд.
17.01.2011, 18:42
Угу. Только почему то в половине справочников указано наоборот.
Что бы там ни было указано в каких-то справочниках — я во время оно работал технологом в цехе печатных плат и как «травится» серебро в хлорном железе наблюдал ежедневно. Хочу заметить, что AgCl — нерастворимое вещество. Т.е. в приведенной Вами реакции поверхность серебра будет тут же покрыта нерастворимой пленкой, и все на этом и кончится.
17.01.2011, 18:56
Хочу заметить, что AgCl — нерастворимое вещество. Т.е. в приведенной Вами реакции поверхность серебра будет тут же покрыта нерастворимой пленкой, и все на этом и кончится.
Для растворения металла необходимо сочетание процессов окисления и комплексообразования (последнее как правило растворяет продукт окисления т.е. предотвращает пассивацию). В случае серебра мощными комплексообразовател ями являются аммиак (как уже было сказано), а также тиасульфат (фиксаж для ч/б фотопроцессов) ну и самый самый — цианид:ржач:
17.01.2011, 19:15
Хочу заметить, что AgCl — нерастворимое вещество. Т.е. в приведенной Вами реакции поверхность серебра будет тут же покрыта нерастворимой пленкой, и все на этом и кончится.
Да я и не спорю — сам имел «удовольствие» это наблюдать. Теперь еще эту дрянь нужно снять с поверхности.
Для растворения металла необходимо сочетание процессов окисления и комплексообразования (последнее как правило растворяет продукт окисления т.е. предотвращает пассивацию).
Я уже упомянул соляную кислоту + перекись водорода. Очень быстро вытравливает медь, может и серебро.
В случае серебра мощными комплексообразовател ями являются аммиак (как уже было сказано)
То есть, чистый раствор? Или в сочетании с окислителем?
17.01.2011, 19:41
Я уже упомянул соляную кислоту + перекись водорода. Очень быстро вытравливает медь, может и серебро.
То есть, чистый раствор? Или в сочетании с окислителем?
Смесь соляной кислоты и перекиси можно попробовать заменить крепким раствором гипохлорита (Белизна), для снятия хлоридной пленки можно все это добро поместить в УЗ-баню. Ну а для цианида окислителем выступает как правило кислород воздуха, т.е. обычный (если это уместное прилагательное:ржач: ) раствор в широкой чашке и.т.п. Золото растворяется в расвторе цианида со свистом.
17.01.2011, 19:56
Смесь соляной кислоты и перекиси можно попробовать заменить крепким раствором гипохлорита (Белизна)
Ок, это менее всего проблема. Только я не понял — гипохрорит натрия заменит и окислитель и растворитель окиси одновременно?
для снятия хлоридной пленки можно все это добро поместить в УЗ-баню Это уже экзотика.
Ну а для цианида
Это уже самоубийственная экзотика. :ржач: Тут кислот нет, буду я еще о цианидах задумываться.
17.01.2011, 20:27
UN7RX, полагаю, что Вам не удастся снять серебро без сильной химии (при серебрении не металлов обычная технология: травление поверхности и образование микропор для лучшего сцепления, осаждение олова в растворе хлористого олова и гальваническое нанесение серебра) — из микропор слабая химия серебро с оловом не возьмёт 🙁 Тонкую шкурку и алмазный нардфиль Вам в руки 🙂
17.01.2011, 20:36
Тонкую шкурку и алмазный надфиль Вам в руки
Шкурка на крайний случай, не хотелось бы царапать поверхность. -( А надфиль алмазный тут бесполезен, одно движение и он забит намертво серебром.
17.01.2011, 20:38
Однажды жонушка решила почистить золотую цепочку , полжила в баночку налила БЕЛЕЗНЫ ,и на ночь утром достала несколько кусочков серого цвета 💡
17.01.2011, 20:46
чем можно стравить серебро с керамики.
А если попробовать нагреть на газе.
17.01.2011, 21:32
Добавлено через 20 минут(ы):
позвонил брату , когда-то 3 курса на химфаке продержался (был самым красивым :smile:) . первый ответ :Общая химия Некрасова 2-х томник ,второй серная кислота и бихромат калия (хромпик , применялся в фотографии ), получается адская смесь ,жрет все . они мыли химпосуду этой гадостью. но опять кислота конценрат 😐
17.01.2011, 22:37
Ок, это менее всего проблема. Только я не понял — гипохрорит натрия заменит и окислитель и растворитель окиси одновременно?
Белизна представляет собой сильно-щелочной раствор гипохлорита натрия, который на свету а также в присутствии серебра разлагается (в первом приближении) на атомарный кислород и хлориды. Кислород окисляет, хлориды связывают в комплекс типа 2-. Но. если вы пользуете хлорид железа (в этом случае окислитель Fe3+) то на выходе у вас практически нерастворимый FeAgCl3, в случае с белизной — более растворимая натриевая соль Na2AgCl3. Если скорость растворения не устраивает — то тогда на пол-часа в гипохлорит, промывка в воде, на пол-часа в тиосульфат и до растворения — извращение конечно же редкостное, но в отсутсвии азотки.
kkozak Общая химия Некрасова 2-х томник — знатная книга
17.01.2011, 23:27
Ну, я не знаю. У вас там в Жезказгане есть могучее предприятие «Жезказганцветмет», не может быть, чтобы на нем азотку не применяли. В ЦЗЛ гарантированно будет в мелкой расфасовке.
18.01.2011, 04:33
У вас там в Жезказгане есть могучее предприятие «Жезказганцветмет», не может быть, чтобы на нем азотку не применяли.
Дык, ясный фиг, там все есть! :crazy: Но знали б Вы во что сейчас превратились «входы-выходы» на всех подразделениях комбината — форт Нокс плачет от зависти. :ржач:
Tolikus, обалдеть, этак такой курс химии изучим! 🙂 Спасибо друзья, вся эта информация будет интересна и полезна наверняка не только мне.
26.01.2011, 18:21
UN7RX,так чем-же закончилась эпопея по снятию покрытия?
26.01.2011, 19:15
Доброго времени суток. Когда то довольно серьезно занимался фото.
Для ослабления передержанных негативов используется красная кровяная соль.
Сам негатив в основном бромистое серебро.
Поцесс довольно быстрый.
Сейчас копну древний справочник по фото выложу формулу.
Доброго времени суток. Когда то довольно серьезно занимался фото.
Для ослабления передержанных негативов используется красная кровяная соль.
Сам негатив в основном бромистое серебро.
Поцесс довольно быстрый.
Сейчас копну древний справочник по фото выложу формулу.
Добавлено через 9 минут(ы):
Так, со справочником видимо пролет. Наверное в гараже.
Но полезная штука интернет
зайдите по ссылке, может это вам подойдет
Добавлено через 6 минут(ы):
А вот и формула K3[Fe(CN)6].
26.01.2011, 19:17
SergeyTT,сошлифовал, механически. 🙂
ra9sn, какое отношение это имеет к ТРАВЛЕНИЮ металлов? Зачем нам «ослабление передержанных негативов»?
26.01.2011, 19:19
Можно в раствор тиосульфата натрия (фото фиксаж, можно в рентген кабинете попросить) положить, серебро стравить должно
26.01.2011, 19:22
Есть у меня подозрение, что сегодня традиционной фотографией, не цифровой, у нас занимаются экстремалы одиночки. Во всяком случае, многочисленные фотоателье давно и прочно перешли на цифру.
26.01.2011, 19:34
При проявлении пленки голлоидное серебро превращается в металлическое. И если выдержка была большая
негатив очень темный. И отпечатать с него бывает не возможно.
Вот зтой солью и удаляют часть металлического серебра.
Процесс очень быстрый.
Можно в раствор тиосульфата натрия (фото фиксаж, можно в рентген кабинете попросить) положить, серебро стравить должно
Тоже верно. Но долго )))) Тиосульфат натрия, сульфит натрия. Но долго, долго))))
Добавлено через 9 минут(ы):
Рентген кабинеты на цифру еще не перешли. ))))) Там это добро должно быть у рентген-техника
26.01.2011, 23:31
SergeyTT,сошлифовал, механически. 🙂
Источник: www.cqham.ru
Декоративное травление металла
Как известно, металл довольно трудно обрабатывать в домашних условиях без специальных навыков и инструментов, тем более, если это такой твёрдый металл, как сталь. Тем не менее, можно призвать на помощь химию: существует такой химический процесс – электролиз. Он протекает на электродах при прохождении электрического тока через растворы электролитов. Т.е. если в качестве электрода взять металлическую заготовку, в качестве электролита использовать обычную солёную воду, то при прохождении через неё тока металл начнёт стравливаться, проще говоря, атомы с поверхности металла начнут «улетать». Таким образом, для обработки металла не всегда нужны какие-то особые навыки и инструменты, ведь за нас всё может сделать электричество.

- Пластиковая или стеклянная ёмкость.
- Поваренная соль.
- Металлическая пластинка.
- Источник питания 5 — 12 вольт.
- Соединительные провода.
Электрохимическая гравировка на металле
Шаг 1. Из металлической пластинки вырежем прямоугольный кусочек, который на котором и будет в дальнейшем вытравлена надпись. Достать металлическую пластинку толщиной 1-2 мм можно в любом строительном магазине, я купил самую дешёвую стальную проушину.

Вырезанный из неё кусок:

Шаг 2. Тщательно зашкуриваем поверхности заготовки, сначала крупной наждачной бумагой, затем мелкой. Поверхность должна стать блестящей, покрытой множеством мелких царапин. Также нужно пройтись наждачной бумагой по краям и рёбрам пластинки. После зашкуривания металл необходимо обезжирить спиртом, растворителем или просто тщательно промыть горячей водой с мылом. После этого прикасаться к поверхностям жирными руками нельзя.

Шаг 3. На лазерном принтере распечатываем рисунок, который будет увековечен на металле и переносим на металл с помощью лазерно-утюжной технологии, которая не раз описывалась в интернете. Распечатывать нужно в зеркальном отображении. Если под рукой нет лазерного принтера, с тем же успехом можно нарисовать рисунок лаком для ногтей или несмываемым маркером. Закрашенная область останется нетронутой, а голый металл подвергнется электролизу, т.е. попросту стравится.




Шаг 4. Теперь, когда заготовка полностью готова к травлению, нужно взять неметаллическую ёмкость, налить в неё воды и насыпать соли. От концентрации соли сильно зависит скорость травления, чем больше соли – тем быстрее идёт процесс. При слишком большой скорости травления есть риск повреждения защитного слоя лака или тонера от принтера, рисунок получится не качественным.
Оптимальное соотношение – столовая ложка соли на стакан воды. В ёмкости нужно закрепить анод, т.е. саму металлическую заготовку и катод – простой кусок металла. Чем больше его площадь, тем выше будет скорость травления. Наглядно установка для травления показана на картинке ниже:
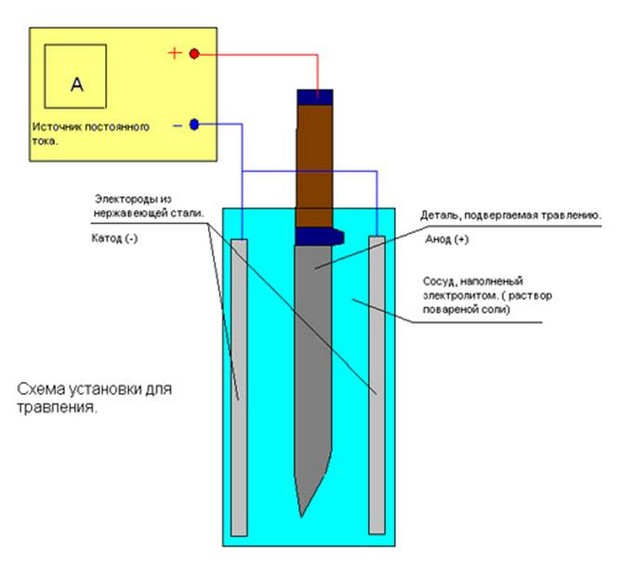
Плюс от источника питания (анод) подключается к заготовке, а минус (катод) в раствор. При этом желательно установить несколько минусовых контактов со всех сторон от заготовки, тогда травление пройдёт равномерно со всех сторон.

Несколько слов об источнике питания. Я использую компьютерный блок питания, а точнее его 12-ти вольтовую линию. Чем больше напряжение – тем выше скорость травления. Можно использовать и обычное зарядное для сотового телефона, на его выходе 5 вольт, этого напряжения будет вполне достаточно.
Не стоит повышать напряжение более 12-ти вольт, иначе процесс будет идти слишком активно, защитный слой лака отпадёт, а раствор перегреется. Правильно подключив все провода, включаем блок питания. От минусового контакта (катода) сразу же начнут идти пузыри, это означает, что процесс идёт. Если пузыри стали идти от заготовки, значит нужно поменять полярность питания.

После нескольких минут травления на поверхности раствора образуется пенка противного жёлто-зелёного цвета.

Минут через 30-40 заготовку можно доставать из раствора, предварительно отключив питание. Она будет вся покрыта чёрным налётом, это нормально.

Шаг 5. Теперь остаётся лишь очистить металл от налёта, стереть тонер или лак, по желанию ещё раз зашкурить поверхность. Чёрный налёт легко удаляется под струёй обычной воды, лак или тонер смывается ацетоном либо жидкостью для снятия лака. Теперь чётко видно, что буквы на металле стали рельефными, сама металлическая поверхность после травления стала матовой.
Источник: sdelaysam-svoimirukami.ru