Добро пожаловать, Гость!
Готовимся к сдаче ЕГЭ по химии
Инструкция
— Выберите один из вариантов в каждом из 18 вопросов;
— Нажмите на кнопку «Показать результат»;
— Скрипт не покажет результат, пока Вы не ответите на все вопросы;
— Загляните в окно рядом с номером задания. Если ответ правильный, то там (+). Если Вы ошиблись, там (-);
— За каждый правильный ответ начисляется 1 балл;
— Оценки: менее 9 баллов — НЕУДОВЛЕТВОРИТЕЛЬНО, от 9 но менее 13.5 — УДОВЛЕТВОРИТЕЛЬНО, 13.5 и менее 18 — ХОРОШО, 18 — ОТЛИЧНО;
— Чтобы сбросить результат тестирования, нажать кнопку «Сбросить ответы».
Источник: examchemistry.com
Тест по химии для 10 класса: Решение экспериментальных задач на получение и распознавание органических веществ
Тест по химии Решение экспериментальных задач на получение и распознавание органических веществ для 10 класса с ответами. Тест состоит из 10 заданий с выбором ответа.
1 Семейство сахаров, фруктоза, лактоза, сахароза, глюкоза
1. Бромная вода обесцвечивается при взаимодействии
1) с бензолом
2) с фенолом
3) с метанолом
4) с этиленом
5) с гексаном
2. Раствор перманганата калия обесцвечивается без нагревания при взаимодействии
1) с ацетиленом
2) с дивинилом
3) с октаном
4) с диметиловым эфиром
5) с глицерином
3. Свежеприготовленный осадок гидроксида меди(II) образует ярко-синий раствор
1) с этанолом
2) с глицерином
3) с фруктозой
4) с этаналем
5) с уксусной кислотой
4. Аммиачный раствор оксида серебра [Ag(NH3)2]OH даёт реакцию «серебряного зеркала»
1) с метановой кислотой
2) с этановой кислотой
3) с глюкозой
4) с ацетиленом
5) с ацетоном
5. Глицерин не реагирует с веществами, формулы которых
6. При брожении глюкозы не образуются
1) масляная кислота
2) пропанол-1
3) этанол
4) уксусная кислота
5) молочная кислота
7. Реактивы, с помощью которых можно отличить метановую кислоту от этановой
8. Укажите вещества, которые дают:
а) синее окрашивание с раствором иода;
б) фиолетовое окрашивание с раствором хлорида железа(III).
1) сахароза
2) толуол
3) фенол
4) крахмал
5) целлюлоза
9. Какие реакции идут при получении из целлюлозы:
а) глюкозы;
б) тринитроцеллюлозы?
1) нитрования
2) разложения
3) гидролиза
4) этерификации
5) замещения
10. Муравьиная кислота не реагирует с веществами
Ответы на тест по химии Решение экспериментальных задач на получение и распознавание органических веществ для 10 класса
1-24
2-12
3-23
4-13
5-15
6-24
7-15
8-43
9-34
10-23
Источник: ustaliy.ru
Кислотный гидролиз сахарозы
Сахароза

Привычный сладкий сахар, используемый в быту, называется сахарозой. Это олигосахарид, относящийся к группе дисахаридов. Формула сахарозы – C12H22O11.
Строение
В состав молекулы входят остатки двух циклических моносахаридов – α-глюкоза и β-фруктоза. Структурная формула вещества состоит из циклических формул фруктозы и глюкозы, соединённых атомом кислорода. Структурные единицы связаны вместе гликозидной связью, образующейся между двумя гидроксилами.
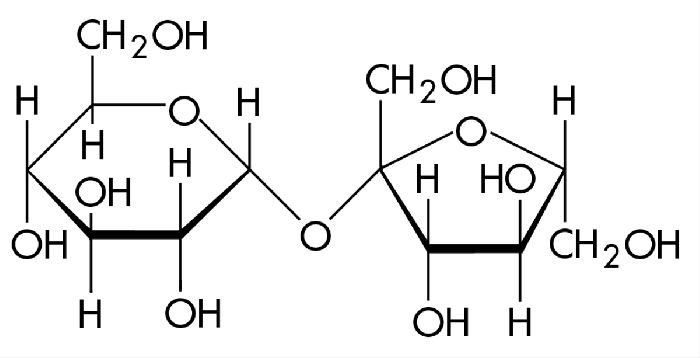
Молекулы сахарозы образуют молекулярную кристаллическую решетку.
Получение
Сахароза – наиболее распространённый в природе углевод. Соединение входит в состав фруктов, ягод, листьев растений. Большое количество готового вещества содержится в свёкле и сахарном тростнике. Поэтому сахарозу не синтезируют, а выделяют с помощью физического воздействия, вываривания и очищения.

Свёклу или сахарный тростник мелко натирают и помещают в большие котлы с горячей водой. Сахароза вымывается, образуя сахарный раствор. В нём присутствуют различные примеси – красящие пигменты, белки, кислоты. Чтобы отделить сахарозу, в раствор добавляют гидроксид кальция Ca(OH)2.
В результате образуется осадок и сахарат кальция С12Н22О11·CaO·2Н2О, через который пропускают диоксид углерода (углекислый газ). В осадок выпадает карбонат кальция, а оставшийся раствор выпаривают до образования кристалликов сахара.
Физические свойства
Основные физические характеристики вещества:

- молекулярная масса – 342 г/моль;
- плотность – 1,6 г/см 3 ;
- температура плавления – 186°С.
Если расплавленное вещество продолжить нагревать, сахароза начнёт разлагаться с изменением окраски. При застывании расплавленной сахарозы образуется карамель – аморфное прозрачное вещество. В 100 мл воды при нормальных условиях можно растворить 211,5 г сахара, при 0°С – 176 г, при 100°С – 487 г. В 100 мл этанола при нормальных условиях сахар можно растворить только 0,9 г сахара.
Попадая в кишечник животных и человека, сахароза под действием ферментов быстро распадается на моносахариды.
Химические свойства
В отличие от глюкозы сахароза не проявляет свойства альдегида за счёт отсутствия альдегидной группы -CHO. Поэтому качественная реакция «серебряного зеркала» (взаимодействие с аммиачным раствором Ag2O) не идёт. При окислении гидроксидом меди (II) образуется не красный оксид меди (I), а ярко-синий раствор.
Основные химические свойства описаны в таблице.
Реакция
Описание
Уравнение
Качественная реакция на наличие гидроксильных групп
Реагирует с гидроксидом меди (II) с образованием сахарата меди ярко-синего цвета
Реакция идёт при нагревании в присутствии катализатора (серной или соляной кислоты). Сахароза разлагается на молекулы фруктозы и глюкозы
Сахароза не способна окисляться (не является восстановителем в реакциях) и называется невосстанавливающим сахаром.
Применение
Сахар в чистом виде используется в пищевой промышленности для изготовления искусственного мёда, сладостей, кондитерских изделий, алкоголя. Сахарозу используют для получения различных веществ: лимонной кислоты, глицерина, бутанола.
В медицине сахарозу используют для изготовления микстур и порошков, чтобы скрыть неприятный вкус.
Что мы узнали?
Сахароза или сахар – дисахарид, состоящий из остатков глюкозы и фруктозы. Обладает сладким вкусом, легко растворяется в воде. Вещество выделяют из свёклы и сахарного тростника. Сахароза обладает меньшей активностью, чем глюкоза. Подвергается гидролизу, реагирует с гидроксидом меди (II), образуя сахарат меди, не окисляется.
Сахар используют в пищевой, химической промышленности, медицине.
Источник: obrazovaka.ru