Алканы не окисляются перманганатом калия при нормальных условиях, вследствие этого раствор не обесцвечивается.
2) Качественная реакция на алкены.
При взаимодействии алкена с водным раствором перманганата калия при комнатной температуре происходит обесцвечивание раствора (реакция Вагнера):
Качественная реакция на непредельные углеводороды, в том числе и на алкены. Реакция может идти и в гетерогенной системе между газообразным или жидким алкеном и водным раствором брома (бромной водой), при этом бромная вода, имеющая желтую окраску, обесцвечивается.
3) Качественная реакция на алкины.
Алкины, так же как и алкены обесцвечивают раствор перманганата калия и бромную воду:
3CH ≡ CH + 8KMnO4 → 3KOOC − COOK + 8MnO2↓ + 2KOH + 2H2O
Алкины с тройной связью у крайнего атома углерода, реагируют с аммиачным раствором оксида серебра Ag[(NH3)2]OH или с аммиачным раствором хлорида меди (I) Cu[(NH3)2]Cl
Алкины у которых тройная связь в середине (R – С ≡ С – R) в эту реакцию не вступают. Такая способность алкинов – замещать атом водорода на атом металла, подобно кислотам – обусловлена тем, что атом углерода находится в состоянии sp -гибридизации и электроотрицательность атома углерода в таком состоянии выше, чем в состоянии sp 3 , sp 2 — гибридизации. Вследствие этого атом углерода сильнее обогащается электронной плотностью, и протон водорода становится подвижным. Эти реакции позволяют отличить алкины с концевой тройной связью от алканов, алкенов и алкинов с тройной связью в середине углеродной цепи.
№ 37. Органическая химия. Тема 11. Алкины. Часть 8. Реакции полимеризации и замещения алкинов
4) Качественные реакции на спирты.
Спирты по количеству гидроксильных групп бывают одно-, многоатомными. Для одно- и многоатомных реакции качественные различны.
Качественные реакции на одноатомные спирты:
Окисление спирта оксидом меди (II). Для этого пары спирта пропускают над раскаленным оксидом меди.
Черный цвет проволоки меняется на красный. Появляется запах альдегида.
Качественная реакция на многоатомные спирты.
Качественной реакцией на многоатомные спирты, содержащие гидроксильные группы у соседних атомов углерода, является их взаимодействие со свежеосажденным гидроксидом меди (II). Ярко-синее окрашивание раствора в результате образования комплексного соединения свидетельствует о наличии многоатомных спиртов.
2 СН – ОН + Сu(OH)2 → СН – О O − CH + 2Н2О
5) Качественные реакции на фенол.
Качественной реакцией на фенол является его взаимодействие с раствором хлорида железа (III), в результате которого образуется интенсивно окрашенное комплексное соединение фиолетового цвета.
Взаимодействие фенола с бромной водой также является качественной реакцией на фенол. Образуется осадок желтоватого цвета при пропускании фенола в водный раствор брома − 2,4,6-трибромфенол:
6) Качественная реакция на альдегиды.
Качественная реакция предназначена для выявления соединений, содержащих альдегидную группу. Аммиачный раствор оксида серебра (реактив Толленса) окисляет альдегиды до соответствующих карбоновых кислот, которые в присутствии аммиака образуют аммонийные соли. Сам окислитель при этой реакции восстанавливается до металлического серебра. За тонкий серебряный налет на стенках пробирки, эта реакция получила название реакции «серебряного зеркала»:
7 ВАЖНЕЙШИХ РЕАКЦИЙ, которые тебе нужно знать (Алкины)
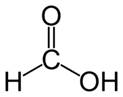
Реакцией серебряного зеркала также можно выявить метановую (муравьиную) кислоту HCOOH. Муравьиная кислота — единственная из карбоновых кислот, содержащая одновременно альдегидную и карбоксильную группы:
В ходе реакции метановая кислота окисляется до угольной, которая разлагается на углекислый газ и воду:
Помимо реакции серебряного зеркала существует также реакция с гидроксидом меди (II). Для этого к свежеприготовленному гидроксиду меди (II) добавляют альдегид и нагревают смесь:
Выпадает оксид меди (I). Cu2O — осадок красного цвета.
При добавлении альдегида к раствору фуксинсернистой кислоты раствор окрашивается в светло-фиолетовый цвет.
7) Качественные реакции на карбоновые кислоты.
Качественные реакции на предельные одноосновные карбоновые кислоты:
1. Изменение цвета индикатора (лакмус на красный, метилоранжевый на красный, фенолфталеин остается бесцветным)
R–COOH ↔ R–COO – + H +
2. Сильные карбоновые кислоты вытесняют слабые кислоты из их солей. Выделяющийся углекислый газ, вызывает помутнение известковой воды:
Эта реакция позволяет отличить карбоновые кислоты от фенолов, также обладающих кислотными свойствами.
Качественная реакция на метановую кислоту HCOOH.
При добавлении концентрированной серной кислоты к раствору муравьиной кислоты образуется угарный газ и вода:
Угарный газ можно поджечь. Горит синим пламенем:
2CO + O2 2CO2
Качественная реакция на многоосновные кислоты:
Качественная реакция на щавелевую кислоту H2C2O4 (HOOC−COOH). При добавлении к раствору щавелевой кислоты раствор соли меди (II) выпадет осадок оксалата меди (II)
Щавелевая кислота так же, как и муравьиная, разлагается концентрированной серной кислотой:
Качественная реакция на непредельные кислоты:
Обесцвечивают бромную воду:
R− CH = CH − RCOOH + Br2 → R− CHBr – CHBr − RCOOH
Обесцвечивают раствор перманганата калия:
3R− CH = CH − RCOOH + 2KMnO4 + 4H2O → 3R− CH(OH) − CH(OH) − RCOOH +
8) Качественные реакции на амины.
На амины качественных реакций нет (за исключением анилина). Можно доказать наличие амина окрашиванием лакмуса в синий цвет. Если же амины нельзя выявить, то можно различить первичный амин, от вторичного путем взаимодействия с азотистой кислотой HNO2.
Для начала нужно ее приготовить, а затем добавить амин:
Первичные дают азот N2:
Вторичные — алкилнитрозоамины — вещества с резким запахом (на примере диметилнитрозоамина):
Третичные амины в мягких условиях с HNO2 не реагируют.
Анилин образует осадок при добавлении бромной воды:
Анилин также можно обнаружить по сиреневой окраске при добавлении хлорной извести.
9) Качественные реакции на углеводы.
Качественные реакции на глюкозу:
Глюкоза – альдегидоспирт. Как и все альдегиды, глюкоза вступает в реакцию «серебряного зеркала» c образованием аммонийной соли глюконовой кислоты.
Взаимодействие с гидроксидом меди (II) приводит к образованию алкоголята меди (характерное синее окрашивание). Реакцию проводят при комнатной температуре (реакция на многоатомные спирты).
При нагревании глюкоза окисляется до глюконовой кислоты (реакция на альдегидную группу)
Качественная реакция на крахмал:
Крахмал в присутствии иода окрашивается в темно-синий цвет. При нагревании окраска исчезает, при охлаждении появляется вновь.
10) Качественная реакция на белки.
Белки выявляются в основном на реакциях, основанных на окрасках.
Ксантопротеиновая реакция. При действии на белки концентрированной азотной кислотой образуется желтая окраска, связанная с нитрованием ароматических колец в соответствующих аминокислотах (на примере тирозина):
Обнаружение серосодержащих аминокислот:
Белок + (CH3COO)2Pb —NaOH →PbS↓ (осадок черного цвета).
Биуретовая реакция для обнаружения пептидной связи (CO-NH)
Белок + CuSO4 + NaOH → фиолетовое окрашивание.
Источник: poisk-ru.ru
Качественные реакции органической химии
В этой статье я опишу некоторые качественные реакции органических соединений. Их огромное количество, ведь органических соединений гораздо больше: свыше 27 000 000 органических на 500 000 неорганических. Разница очевидна.
В органической химии качественные реакции определяют преимущественно вещества, а если быть точнее, то представителей класса веществ (алканы, алкены и т.д.).
1. Качественная реакция на алканы. Определить, что какое-то вещество в смеси или в чистом виде алкан, несложно. Для этого газ либо поджигают — горение алканов сопровождается синим пламенем, либо пропускают через раствор перманганата калия. Алканы не окисляются перманганатом калия на холоду, вследствие этого раствор не будет изменять окраску.
2. Качественная реакция на алкены. Чтобы убедиться в наличии алкена, нужно пропустить его в раствор перманганата калия (реакция Вагнера). В ходе реакции раствор обесцветится, выпадает бурый диоксид марганца MnO2 (реакция на примере этилена):
3C2H4 + 2KMnO4 + 4H2O ——> 3CH2OH-CH2OH + 2KOH + 2MnO2↓
Так же, алкены обесцвечивают бромную воду:
C2H4 + Br2 ——> C2H4Br2
Бромная вода обесцвечивается, образуется дибромпроизводное.
3. Качественная реакция на алкины. Алкины можно выявить и по реакции Вагнера или с помощью бромной воды:
Алкины с «наружной» тройной связью реагируют с аммиачным раствором оксида серебра (гидроксид диаминсеребра (I)) (реактив Толленса):
C2H2 + 2[Ag(NH3)2]OH ——-> Ag2C2↓ + 4NH3↑ + 2H2O
Получившийся ацетиленид серебра (I) выпадает в осадок.
Данная качественная реакция действует только на алкины с «наружной» тройной связью. Алкины, у которых тройная связь в середине (R-C-=C-R) в эту реакцию не вступают.
Такая способность алкинов замещать протон на атом металла, подобно кислотам, обусловлено тем, что атом углерода находится в состоянии sp-гибридизации и электроотрицательность атома углерода в таком состоянии такая же, как у азота. В следствии этого, атом углерода сильнее обогощается электронной плотностью и протон становится подвижным.
4. Качественная реакция на альдегиды. Одна из самых интересных качественных реакций в органической химии — на альдегиды, предназначена исключительно для выявления соединений, содержащих альдегидную группу. К альдегиду приливают аммиачный раствор оксида серебра, реакция идет при нагревании:
CH3-CHO + 2[Ag(NH3)2]OH —t—> CH3-COOH + 2Ag↓ + 4NH3↑ + H2O
Если опыт проведен грамотно, то выделяющееся серебро покрывает колбу ровным слоем, создавая эффект зеркала. Именно поэтому реакция называется реакцией серебряного зеркала.
Примечание: реакцией серебряного зеркала также можно выявить метановую (муравьиную) кислоту HCOOH. При чем тут кислота, если мы говорим про альдегиды? Все просто: муравьиная кислота — единственная из карбоновых кислот, содержащая одновременно альдегидную и карбоксильную группы:
В ходе реакции метановая кислота окисляется до угольной, которая разлагается на углекислый газ и воду:
HCOOH + 2[Ag(NH3)2]OH —t—> CO2↑ + 2H2O + 4NH3↑ + 2Ag↓
Помимо реакции серебряного зеркала существует также реакция с гидроксидом меди (II) Cu(OH)2. Для этого свежеприготовленному гидроксиду меди (II) добавляют альдегид и нагревают смесь:
CuSO4 + 2NaOH ——> Na2SO4 + Cu(OH)2↓
CH3-CHO + 2Cu(OH)2 —t—> CH3-COOH + Cu2O↓ + 2H2O
Выпадает оксид меди (I) Cu2O — осадок красного цвета.
Еще один метод определения альдегидов — реакция с щелочным раствором тетраиодомеркурата (II) калия, известный нам из предыдущей статьи как реактив Несслера:
CH3-CHO + K2[HgI4] + 3KOH ——> CH3-COOK + Hg↓ + 4KI + 2H2O
При добавлении альдегида к раствору фуксинсернистой кислоты раствор окрашивается в светло-фиолетовый цвет.
5. Качественные реакции на спирты. Спирты по количеству гидроксильных групп бывают одно-, двух-, многоатомными. Для одно- и многоатомных реакции различны.
Качественные реакции на одноатомные спирты:
Простейшая качественная реакция на спирты — окисление спирта оксидом меди. Для этого пары спирта пропускают над раскаленным оксидом меди. Затем полученный альдегид улавливают фуксинсернистой кислотой, раствор становится фиолетовым:
CH3-CH2-OH + CuO —t—> CH3-CHO + Cu + H2O
Спирты идентифицируются пробой Лукаса — конц. раствор соляной кислоты и хлорида цинка. При пропускании вторичного или третичного спирта в такой раствор образуется маслянистый осадок соответствующего алкилхлорида:
CH3-CHOH-CH3 + HCl —ZnCl2—> CH3-CHCl-CH3 + H2O
Первичные спирты в реакцию не вступают.
Еще одним известным методом является иодоформная проба:
CH3-CH2-OH + 4I2 + 6NaOH ——> CHI3↓ + 5NaI + HCOONa + 5H2O
Качественные реакции на многоатомные спирты.
Наиболее известная качественная реакция на многоатомные спирты — взаимодействие их с гидроксидом меди (II). Гидроксид растворяется, образуется хелатный комплекс темно-синего цвета. Обратите внимание на то, что в отличии от альдегидов многоатомные спирты реагируют с гидроксидом меди (II) без нагревания.
6. Качественные реакции на карбоновые кислоты. На карбоновые кислоты обычно подчеркивают образование цветных осадков с тяжелыми металлами. Но наиболее осуществимая качественная реакция на метановую кислоту HCOOH. При добавлении концентрированной серной кислоты H2SO4 к раствору муравьиной кислоты образуется угарный газ и вода:
HCOOH —H2SO4—> CO↑ + H2O
Угарный газ можно поджечь. Горит синем пламенем:
Из многоосновных кислот рассмотрим качественную реакцию на щавелевую. При добавлении к раствору щавелевой кислоты раствор соли меди (II) выпадет осадок оксалата меди (II):
Cu 2+ + C2O4 2- ——> CuC2O4↓
Щавелевая кислота также, как и муравьиная, разлагается концентрированной серной кислотой:
H2C2O4 —-H2SO4—> CO↑ + CO2↑ + H2O
7. Качественные реакции на амины. На амины качественных реакций нет (за исключением анилина). Можно доказать наличие амина окрашиванием лакмуса в синий цвет. Если же амины нельзя выявить, то можно различить первичный амин от вторичного путем взаимодействия с азотистой кислотой HNO2. Для начала нужно ее приготовить, а затем добавить амин:
NaNO2 + HCl ——> NaCl + HNO2
Первичные дают азот N2:
CH3-NH2 + HNO2 ——> CH3-OH + N2↑ + H2O
Вторичные — алкилнитрозоамины — вещества с резким запахом (на примере диметилнитрозоамина):
CH3-NH-CH3 + HNO2 ——> CH3-N(NO)-CH3 + H2O
Анилин C6H5NH2 можно обнаружить по сиреневой окраске при добавлении хлорной извести.
8. Качественные реакции на фенол. Фенол лучше всегообнаруживает хлорид железа (III) — образуется фиолетовое окрашивание раствора. Этот лучший метод обнаружения фенола, т.к. реакция очень чувствительна.
Также фенол наряду с анилином дает осадок желтоватого цвета при пропускании в водный раствор брома — 2,4,6 — трибромфенол:
C6H5OH + 3Br2 ——> C6H2OH(Br)3↓ + 3HBr
Фенолы дают фенол-альдегидные смолы при реакции фенола с альдегидом в кислой среде. При этом образуется мягкие пористые массы фенол-альдегидных смол (реакция поликонденсации).
9. Качественная реакция на алкилхлориды. Вещества, содержащие хлор, могут окрашивать пламя в зеленый цвет. Для этого нужно обмакнуть медную проволоку в алкилхлориде и поднести к пламени (проба Бельштейна).
10. Качественная реакция на углеводы. Большинство углеводов имеют альдегидные и гидроксильные группы, поэтому для них характерны все реакции альдегидов и многоатомных спиртов.
Существует способ, который помогает различить глюкозу от фруктозы. Этот способ носит название проба Селиванова. Для того, чтобы различить эти углеводы, к ним приливают смесь резорцина и соляной кислоты. Реагирует со смесью фруктоза, при этом раствор окрашивается в малиновый цвет.
Крахмал в присутствии иода окрашивается в темно-синий цвет. При нагревании окраска исчезает, при охлаждении появляется вновь.
11. Качественная реакция на белки. Белки выявляются в основном на реакциях, основанные на окрасках.
Ксантопротеиновая реакция. Данная реакция обнаруживает ароматические аминокислоты, входящие в белки (на примере тирозина):
(OH)C6H4CH(NH2)COOH + HNO3 —-H2SO4——> (OH)C6H3(NO2)CH(NH2)COOH↓ + H2O — выпал осадок желтого цвета.
(OH)C6H3(NO2)CH(NH2)COOH + 2NaOH ——-> (ONa)C6H3(NO2)CH(NH2)COONa + H2O — раствор становится оранжевым.
Обнаружение серосодержащих аминокислот:
Белок + (CH3COO)2Pb —NaOH—> PbS↓ (осадок черного цвета).
Биуретовая реакция для обнаружения пептидной связи (CO-NH):
Белок + CuSO4 + NaOH ——> красно-фиолетовое окрашивание.
Спецефический запах при горении:
Белок —-обжиг—-> запах паленой шерсти
Источник: studopedia.su
Качественные реакции органической химии
Это означает, что качественные реакции — это реакции с ощутимым эффектом -цвет, запах, изменение состояния вещества. «Селективность» — означает, что желательно, чтобы такая реакция на данный класс веществ или на данное вещество была уникальна. Высокая чувствительность — даже очень небольшое количество вещества должно проявляться в такой реакции.
С уникальностью в органической химии немного проблематично, но тем не менее, есть достаточно много реакций для определения того или иного вещества.
Итак, классы органических соединений и соответствующие им качественные реакции:
| Класс органических соединений | Качественные реакции |
| Алканы | У алканов нет качественных реакций. Их определяют методом исключения |
| Алкены | 1. Обесцвечивание бромной воды: 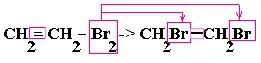 2. Изменение окраски раствора перманганата калия: 3СH2=CH2 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2 + 2KOH 2. Изменение окраски раствора перманганата калия: 3СH2=CH2 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2 + 2KOH 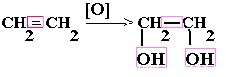 |
| Циклоалканы | Обесцвечивание бромной воды: 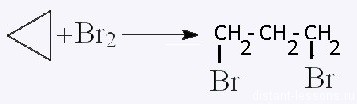 |
| Алкины | 1. Обесцвечивание бромной воды, 2. Образование ацетиленидов серебра и меди: 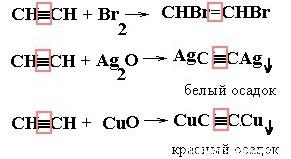 3. Изменение окраски перманганата калия: (KMnO4 → MnO2) C2H2 → HOOC-COOH 3. Изменение окраски перманганата калия: (KMnO4 → MnO2) C2H2 → HOOC-COOH |
| Алкадиены | Т.к. алкадиены содержат 2 двойные связи, то они так же как и алкены, обесцвечивают бромную воду |
| Арены | 1. Взаимодействие с бромом (в присутствии катализатора) 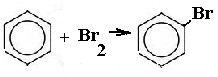 2.реакция с аммиачным раствором цианида никеля (II).Выпадает осадок комплексного соединения бензоцианоаммината никеля Ni(CN)2NH3(C6H6). 2.реакция с аммиачным раствором цианида никеля (II).Выпадает осадок комплексного соединения бензоцианоаммината никеля Ni(CN)2NH3(C6H6). |
| Спирты | Реакция с оксидом меди — в осадок выпадает медь: 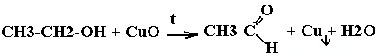 |
| Многоатомные спирты | С гидрокисдом меди (II) — Cu(OH)2 образуется комплекс синего цвета |
| Альдегиды | Реакция «серебряного зеркала» и реакция «медного зеркала»: 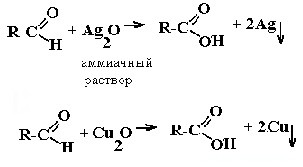 |
| Кислоты органические | Дают окрашенные соли тяжелых металлов — см. таблицу растворимости |
| Амины | Качественных реакций нет (только анилин — имеет характерный запах) |
Как вы видите, все вещества, имеющие кратные связи (кратные=двойные и тройные), обесцвечивают бромную воду. Многие из них изменяют окраску раствора перманганата калия. Поэтому эти вещества надо разделять по их индивидуальным, характерным только для них качественным реакциям.
Здесь перечислены самые основные качественные реакции органической химии. Если говорить о высокомолекулярных соединениях — белках, жирах, углеводах, то для них качественные реакции определяются функциональными группами, входящими в состав. Зная функциональную группу, вы легко сможете подобрать реактив, т.к. в таблице они разобраны именно по классам.
Таблица качественных реакций для газов
Таблица качественных реакций для щелочных металлов:
Т.к. все соединения щелочных металлов хорошо растворимы в воде, то их определяют по цвету пламени:
(указан так же цвет пламени некоторых щелочно-земельных металлов)
| желто-зеленое | фиолетовое | кирпично-красное | ярко-красное | желтое | карминово-красное |
| Ba 2+ | K + | Са 2+ | Li + | Na + | Sr 2+ |
Таблица качественных реакций
— цвета осадков
| Осадки белого цвета | Качественная реакция |
| Белый творожистый нерастворимый в воде; нерастворимый в HNO3 | Ag + + Cl — → AgCl↓ качественная реакция на соли серебра; качественная реакция на хлорид-ионы; |
| Белый осадок нерастворимый в кислотах | Ba 2+ + SO4 -2 → BaSO4↓ качественная реакция на соли бария; качественная реакция на сульфат-ионы; |
| Белый осадок образуется при пропускании газа без цвета с резким запахом через известковую воду; растворяется при пропускании избытка газа; растворяется в кислотах | Сa(OH)2 + SO2 = CaSO3↓ + H2O · избыток SO2: CaSO3↓ + H2O + SO2 = Ca(HSO3)2; · растворение в кислотах: CaSO3 + 2H + → SO2↑ + H2O + Ca 2+ |
| Белый осадок образуется при добавлении щелочи; растворяется в избытке щелочи | Al 3+ + 3OH — = Al(OH)3↓ Zn 2+ + 2OH — = Zn(OH)2↓ · избытокщелочи: Al(OH)3 + NaOH =Na[Al(OH)]4; · избытокщелочи: Zn(OH)2 +2NaOH =Na2[Zn(OH)]4; |
| Белый осадок образуется при пропускании газа без цвета и запаха через известковую воду; растворяется при пропускании избытка газа; растворяется в кислотах | Сa(OH)2 + CO2 = CaCO3↓ + H2O · избыток CO2: CaCO3↓ + H2O + CO2 = Ca(HSO3)2; · растворение в кислотах: CaCO3 + 2H + → CO2↑ + H2O + Ca 2+ |
| Осадок светло-желтого цвета (осадок кремового цвета) образуется при приливании AgNO3; нерастворим в HNO3; | Ag + + Br — → AgBr↓ качественная реакция на бромид-ионы; (качественная реакция на соли серебра); |
| Осадок желтого цвета образуется при приливании AgNO3; нерастворим в HNO3; | Ag + + I — → AgJ↓ качественная реакция на иодид-ионы; (качественная реакция на соли серебра); |
| Осадок желтого цвета образуется при приливании AgNO3; растворим в кислотах; | 3Ag + + PO4 3- → Ag3PO4↓ |
| Осадки коричневых цветов | Качественная реакция |
| Осадок бурого цвета образуется при взаимодействии с растворами щелочей; | Fe 3+ +3OH — → Fe(OH)3↓ качественная реакция на соли железа |
| Осадки синих цветов | Качественная реакция |
| Осадок голубого цвета (осадок синего цвета) образуется при взаимодействии с растворами щелочей | Cu 2+ +2OH — → Cu(OH)2↓ качественная реакция на соли меди (II) |
| Осадок синего цвета образуется при взаимодействии с раствором красной кровяной и желтой кровяной соли | 3Fe 2+ + 2[Fe(CN)6] 3- → Fe3[Fe(CN)6]2↓ качественная реакция на соли железа (II) — с красной кровяной солью; 4Fe 3+ + 3[Fe(CN)6]4 -4 → Fe4[Fe(CN)6]3↓ качественная реакция на соли железа (III) — с желтой кровяной солью; |
| Осадки черного цвета | Качественнаяреакция |
| Осадок черного цвета Образуется при взаимодействии с сульфидами или с H2S | Fe 2+ + S 2- → FeS↓ Ni 2+ + S 2- → NiS↓ Cu 2+ + S 2- → CuS↓ Pb 2+ + S 2- → PbS↓ Hg 2+ + S 2- → HgS↓ Ag + + S 2- → Ag2S↓ качественная реакция на сульфид-ионы |
Источник: studopedia.ru