Химические свойства моносахаридов обусловлены особенностями их строения.
Рассмотрим химические свойства на примере глюкозы.
Моносахариды проявляют свойства спиртов и карбонильных соединений.
а) Как и у всех альдегидов, окисление моносахаридов приводит к соответствующим кислотам. Так, при окислении глюкозы аммиачным раствором гидрата окиси серебра образуется глюконовая кислота (реакция «серебряного зеркала»).
| D- глюкоза | + 2[Ag(NH3)2]OH → | аммониевая соль D- глюконовой кислоты | + 2Ag↓ + 3NH3↑+ H2O |
Эти реакции являются качественными на глюкозу как альдегид.
Соль глюконовой кислоты – глюконат кальция – известное лекарственное средство.
б) Реакция моносахаридов с гидроксидом меди при нагревании так же приводит к альдоновым кислотам.
| D- галактоза | + 2Cu(OH)2 → | D- галактоновая кислота | + Cu2O↓ + 2H2O |
Химия, 12-й класс, Глюкоза
Эти реакции являются качественными на глюкозу как альдегид.
в) Более сильные окислительные средства окисляют в карбоксильную группу не только альдегидную, но и первичную спиртовую группы, приводя к двухосновным сахарным (альдаровым) кислотам. Обычно для такого окисления используют концентрированную азотную кислоту.
| D- глюкоза | HNO3(конц.) –––––––→ | сахарная (D- глюкаровая) кислота |
Восстановление сахаров приводит к многоатомным спиртам. В качестве восстановителя используют водород в присутствии никеля, алюмогидрид лития и др.
| D- глюкоза | LiAlH4 + H2 ––––→ | D- сорбит |
3. Несмотря на схожесть химических свойств моносахаридов с альдегидами, глюкоза не вступает в реакцию с гидросульфитом натрия (NaHSO3).
1. Алкилирование (образование простых эфиров).
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу.
| , D- глюкопираноза | + СH3ОН | HCl(газ) ––––→ | метил-α, D- глюкопиранозид | + H2О |
При использовании более сильных алкилирующих средств, каковыми являются, например, йодистый метил или диметилсульфат, подобное превращение затрагивает все гидроксильные группы моносахарида.
| СH3I ––––→ NaOH | пентаметил-α, D- глюкопираноза |
2. Ацилирование (образование сложных эфиров).
При действии на глюкозу уксусного ангидрида образуется сложный эфир – пентаацетилглюкоза.
| ––––––––→ | пентаацетил-α,D- глюкопираноза |
3. Как и все многоатомные спирты, глюкоза с гидроксидом меди (II) на холоду с образованием глюконата меди (II) дает интенсивное синее окрашивание – качественная реакция на глюкозу как многоатомный спирт.
ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ
ярко синий раствор
III. Специфические реакции
1. Горение (а также полное окисление в живом организме):
Кроме приведенных выше, глюкоза характеризуется и некоторыми специфическими свойствами — процессами брожения. Брожением называется расщепление молекул сахаров под воздействием ферментов (энзимов). Брожению подвергаются сахара с числом углеродных атомов, кратным трем. Существует много видов брожения, среди которых наиболее известны следующие:
а) спиртовое брожение
б) молочнокислое брожение
| C6H12O6 → 2CH3– | CH–СОOH(молочная кислота) | OH |
в) маслянокислое брожение
Упомянутые виды брожения, вызываемые микроорганизмами, имеют широкое практическое значение. Например, спиртовое – для получения этилового спирта, в виноделии, пивоварении и т.д., а молочнокислое – для получения молочной кислоты и кисломолочных продуктов.
Фруктоза вступает во все реакции, характерные для многоатомных спиртов, однако реакции альдегидной группы, в отличие от глюкозы, для нее не характерны.
Химические свойства рибозы C5H10O5 аналогичны глюкозе.
Д) Биологическая роль глюкозы.
3. Дисахариды.
Олигосахариды — углеводы, молекулы которых содержат от 2 до 8-10 остатков моносахаридов, соединенных гликозидными связями. В соответствии с этим различают дисахариды, трисахариды и т. д.
Дисахариды — сложные сахара, каждая молекула которых при гидролизе распадается на две молекулы моносахаридов. Дисахариды наряду с полисахаридами являются одним из основных источников углеводов в пище человека и животных. По своему строению дисахариды являются гликозидами, в которых две молекулы моносахаридов соединены гликозидной связью.
Строение
1. Молекулы дисахаридов могут содержать два остатка одного моносахарида или два остатка разных моносахаридов;
2. Связи, образующиеся между остатками моносахаридов, могут быть двух типов:
а) в образовании связи принимают участие полуацетальные гидроксилы обеих молекул моносахаридов. Например, образование молекулы сахарозы;
б) в образовании связи принимают участие полуацетальный гидроксил одного моносахарида и спиртовый гидроксил другого моносахарида. Например, образование молекул мальтозы, лактозы и целлобиозы.
Для установления строения дисахаридов необходимо знать: из каких моносахаридов он построен, какова конфигурация аномерных центров у этих моносахаридов (- или -), каковы размеры цикла (фураноза или пираноза) и с участием каких гидроксилов связаны две молекулы моносахарида.
Дисахариды подразделяются на две группы: восстанавливающие и невосстанавливающие.
Среди дисахаридов особенно широко известны мальтоза, лактоза и сахароза.
Мальтоза (солодовый сахар), являющаяся α-глюкопиранозил-(1-4)-α-глюкопиранозой, образуется в качестве промежуточного продукта при действии амилаз на крахмал (или гликоген), содержит два остатка α-D-глюкозы. Название сахара, чей полуацетальный гидроксил участвует в образовании гликозидной связи, оканчивается на «ил».
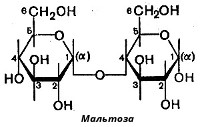
В молекуле мальтозы у второго остатка глюкозы имеется свободный полуацетальный гидроксил. Такие дисахариды обладают восстанавливающими свойствами.
К восстанавливающим дисахаридам относится, в часности, мальтоза (солодовый сахар), содержащаяся в солоде, т.е. проросших, а затем высушенных и измельченных зернах хлебных злаков.
Мальтоза составлена из двух остатков D- глюкопиранозы, которые связаны (1–4) -гликозидной связью, т.е. в образовании простой эфирной связи участвуют гликозидный гидроксил одной молекулы и спиртовой гидроксил при четвертом атоме углерода другой молекулы моносахарида. Аномерный атом углерода (С1), участвующий в образовании этой связи, имеет - конфигурацию, а аномерный атом со свободным гликозидным гидроксилом (обозначен красным цветом) может иметь как α- (α- мальтоза), так и β- конфигурацию (β- мальтоза).
Мальтоза представляет собой белые кристаллы, хорошо растворимые в воде, сладкие на вкус, однако значительно меньше, чем у сахара (сахарозы).
Как видно, в мальтозе имеется свободный гликозидный гидроксил, вследствие чего сохраняется способность к раскрытию цикла и переходу в альдегидную форму. В связи с этим, мальтоза способна вступать в реакции, характерные для альдегидов, и, в частности, давать реакцию «серебряного зеркала», поэтому ее называют восстанавливающим дисахаридом. Кроме того, мальтоза вступает во многие реакции, характерные для моносахаридов, например, образует простые и сложные эфиры.
| СH3I ––––→ NaOH | |
| мальтоза | Октаметилмальтоза |
Дисахарид лактоза (молочный сахар) содержится только в молоке и состоит из D-галактозы и D-глюкозы. Это — α-глюкопиранозил-(1-4)-глюкопираноза:
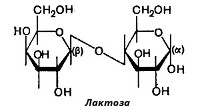
Поскольку в молекуле лактозы имеется свободный полуацетальный гидроксил (в остатке глюкозы), она принадлежит к числу редуцирующих дисахаридов.
Одним из наиболее распространенных дисахаридов является сахароза (тростниковый или свекольный сахар) − обычный пищевой сахар. Молекула сахарозы состоит из одного остатка D-глюкозы и одного остатка D-фруктозы. Следовательно, это − α-глюкопиранозил-(1-2)-β-фруктофуранозид:
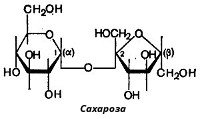
В отличие от большинства дисахаридов сахароза не имеет свободного полуацетального гидроксила и не обладает восстанавливающими свойствами.
К невосстанавливающим дисахаридам относится сахароза (свекловичный или тростниковый сахар). Она содержится в сахарном тростнике, сахарной свекле (до 28% от сухого вещества), соках растений и плодах. Молекула сахарозы построена из α, D- глюкопиранозы и β, D- фруктофуранозы.
В противоположность мальтозе гликозидная связь (1–2) между моносахаридами образуется за счет гликозидных гидроксилов обеих молекул, то есть свободный гликозидный гидроксил отсутствует. Вследствие этого отсутствует восстанавливающая способность сахарозы, она не дает реакции «серебряного зеркала», поэтому ее относят к невосстанавливающим дисахаридам.
Среди природных трисахаридов важное значение имеют немногие. Наиболее известна рафиноза, содержащая остатки фруктозы, глюкозы и галактозы, которая находится в больших количествах в сахарной свекле и во многих других растениях.
В целом олигосахариды, присутствующие в растительных тканях, разнообразнее по своему составу, чем олигосахариды животных тканей.
Все они имеют ту же эмпирическую формулу С12Н22О11, т.е. являются изомерами.
Сахароза – белое кристаллическое вещество, сладкое на вкус, хорошо растворимое в воде.
Для сахарозы характерны реакции по гидроксильным группам. Как и все дисахариды, сахароза при кислотном или ферментативном гидролизе превращается в моносахариды, из которых она составлена.
Дисахариды – типичные сахароподобные углеводы; это твердые бесцветные кристаллические вещества, очень хорошо растворимое в воде, имеющие сладкие вкус.
Из дисахаридов наибольшее значение имеет сахароза C12H22O11:
Молекула сахарозы состоит из остатков молекул глюкозы и фруктозы.
Дата добавления: 2017-06-13 ; просмотров: 11473 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Источник: poznayka.org
Химик.ПРО – решение задач по химии бесплатно
Реакцию серебряного зеркала используют как качественную для открытия альдегидов. Альдегидная группа глюкозы окисляется до карбоксильной группы, и глюкоза превращается в глюконовую кислоту.
Запишем качественную реакцию глюкозы (C6H6O6) с аммиачным раствором оксида серебра (I) (реакцию серебряного зеркала):
![]()
Учитывая, что молярная масса глюкозы (C6H6O6) равна 174 г/моль, а молярная масса серебра 108 г/моль (смотри таблицу Менделеева), по уравнению реакции найдем сколько грамм глюкозы (C6H6O6) необходимо, для реакции серебряного зеркала:

для получения осадка массой 4,32 г необходимо х г глюкозы (сколько грамм глюкозы)
для получения осадка массой 216 г необходимо 174 г глюкозы (сколько грамм глюкозы)
![]()
Следовательно, для реакции серебряного зеркала необходимо сколько грамм глюкозы (C6H6O6) — 3,48 г.
Ответ:
масса глюкозы равна 3,48 грамм.
Источник: himik.pro
Лабораторная работа на тему свойства простых и сложных углеводов
Цель: экспериментально изучить физические и химические свойства простых и сложных углеводов. Оборудование: колба круглодонная, горелка, стакан, штатив, прокладка огнезащитная. Реактивы: нитрат серебра (AgNO3), концентрированный раствор аммиака (NH4OH), глюкоза, (С6Н12О6), раствор сульфата меди (СuSO4), гидроксид натрия (NaOH), сахароза (С12Н22О11), мальтоза (С12Н22О11).
Опыт 29. Реакция глюкозы с аммиачным раствором оксида серебра
К приготовленному аммиачному раствору оксида серебра добавили раствор глюкозы и подогрели смесь на водяной бане. Уравнение реакции: AgNO3 + NH4OH → [Ag(NH3)2] OH + NH4NO3 Наблюдения: на стенках колбы отметили образование металлического серебра. Вывод: Глюкоза в молекуле имеет альдегидную группу, которая окисляется до карбоксильной в присутствии аммиачного раствора серебра. Это качественная реакция на присутствие альдегидной группы у моносахаридов (реакция «серебряного зеркала»). Такую реакцию используют в промышленности для серебрения зеркал, изготовления колб для термосов, елочных украшений.
Опыт 30. Открытие в моносахаридах гидроксильных групп
В пробирку налили немного раствора глюкозы и добавили 3-4 капли 2% раствора CuSO4 и 2-3 мл 10% раствора NaOH. К образовавшемуся осадку голубого цвета прилили несколько капель затем еще добавили немного раствора глюкозы. Уравнение реакции: Наблюдения: отметили полное растворение голубого осадка гидроксида меди, появилось васильковое окрашивание раствора от образующегося комплексного соединения – глюконат меди. Вывод: Глюкоза как многоатомный спирт, проявляя слабые кислотные свойства по отношению к гидроксиду меди, образует растворимую комплексную соль глюконата меди. Это качественная реакция на многоатомные спирты, на присутствие соседних гидроксильных групп в молекуле соединения.
Опыт 31. Восстанавливающие свойства моносахаридов
В пробирку налили немного раствора глюкозы и добавили 3-4 капли 2% раствора CuSO4 и 2-3 мл 10% раствора NaOH. К образовавшемуся осадку голубого цвета прилили несколько капель затем еще добавили немного раствора глюкозы.
Затем пробирку подогрели на спиртовой горелке Уравнение реакции: 2CuOH Cu2O + H2O Наблюдения: отметили полное растворение голубого осадка гидроксида меди, появилось васильковое окрашивание раствора от образующегося комплексного соединения – глюколят меди. При нагревании пробирки с синим раствором, окраска менялась, сначала на жёлтую CuOH — гидроксида меди(I) неустойчивого соединения, которое при продолжительном нагревании, разлагается образуя Cu2O — оксид меди (I) красного цвета. Эта реакция, так же является качественной реакцией на альдегиды. Вывод: Благодаря присутствию альдегидной группы в молекуле, глюкоза является восстанавливающим моносахаридом, для которой характерны «реакция серебряного зеркала» и взаимодействие с фелинговой жидкостью (восстановление синего Cu(OH)2 до желтого CuOH и далее оранжевого Cu2O).
Опыт 32. Открытие гидроксильных групп в дисахаридах
В пробирку налили 3-4 капли 2% раствора CuSO4 и 2-3 мл 10% раствора NaOH. Образовавшийся осадок голубого цвета разделили на две части: в одну добавили несколько капель раствора сахарозы, во вторую раствор мальтозы. и перемешали. Затем каждую из пробирок нагрели в пламени спиртовой горелки.
Уравнения реакций: CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4 Наблюдения: Осадок растворился в двух пробирках, появилось васильковое окрашивание раствора от образующегося комплексного соединения – сахарата меди (II) и мальтата меди.. Вывод: реакция с гидроксидом меди является качественной реакцией на многоатомность спиртов с соседними ОН-группами. Таким образом данная реакция доказывает на присутствие гидроксильных групп в молекулах дисахаридов: мальтозы и сахарозы.
Опыт 33. Восстанавливающие свойства дисахаридов
В пробирку налили 3-4 капли 2% раствора CuSO4 и 2-3 мл 10% раствора NaOH. Образовавшийся осадок голубого цвета разделили на две части: в одну добавили несколько капель раствора сахарозы, во вторую раствор мальтозы. и перемешали. Затем каждую из пробирок нагрели в пламени спиртовой горелки.
Уравнения реакций: CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4 Наблюдения: Осадок растворился в двух пробирках, появилось васильковое окрашивание раствора от образующегося комплексного соединения – сахарата меди (II) и мальтата меди. При нагревании, в пробирке с сахаратом меди видимых изменений не произошло, во второй – синяя окраска раствора менялась, сначала на жёлтую CuOH — гидроксида меди(I) неустойчивого соединения, которое при продолжительном нагревании, разлагается образуя Cu2O — оксид меди (I) красного цвета. Вывод: Мальтоза – это альдегидо-спирто-гликозид, является восстанавливающим дисахаридом, т.к содержит в молекуле альдегидную группу и дает все характерные реакции восстановления («реакция серебряного зеркала», c гидроксидом меди при нагревании окисляется до карбоксильной группы). Сахароза не содержит альдегидной группы, следовательно является невосстанавливащим дисахаридом Общий вывод: Экспериментальным путем изучили химические свойства моносахаридов и дисахаридов, установили их молекулярное строение с помощью характерных качественных реакций по спиртовой и альдегидной группе.
Похожие ответы, выполненные работы
- Контрольная работа по химии, ТГУ
- Лабораторная работа на тему кислородсодержащие соединения
- Лабораторная работа по дисциплине…
- Тест по дисциплине «Общая и неорганическая…
- Помощь с контрольными заданиями по химии, ОФ ПГУТИ
- Контрольная работа по дисциплине «Общая и…
- Тест по дисциплине «Общая и неорганическая…
- Защита трубопроводов от коррозии
- Лабораторная работа по дисциплине…
- Помощь онлайн по русскому языку на тему…
или напишите нам прямо сейчас
Источник: the-distance.ru