Под атомно-кристаллической структурой понимают взаимное расположение атомов, существующее в кристалле. Кристалл состоит из атомов (ионов), расположенных в определенном порядке, который периодически повторяется в трех измерениях.
В кристаллах существует не только ближний, но и дальний порядок размещения атомов, т.е. упорядоченное расположение частиц в кристалле сохраняется на больших участках кристаллов.
Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узлах которой располагаются атомы (ионы), образующие металл (твердое кристаллическое тело).
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, получил название элементарной кристаллической ячейки.
Подавляющее число технически важных металлов образуют одну из следующих решеток: кубическую объемно-центрированную, кубическую гранецентрированную и гексагональную (рис. 9).
Кристаллические решетки. 10 класс.
В кубической объемно-центрированной решетке атомы расположены в узлах ячейки и один атом — в центре объема куба (рис. 9, а). Кубическую объемно-центрированную решетку имеют металлы: а-железо, хром, ниобий, вольфрам, ванадий и др.
В кубической гранецентрированной решетке атомы расположены в углах куба и в центре каждой грани (рис. 9, б). Этот тип решетки имеют металлы: у-железо, никель, медь, золото и др.

Рис. 9. Кристаллические решетки металлов и схемы упаковки атомов: а — объемно-центрированная кубическая (о. ц. к.); б — гранецентрированная кубическая (г. ц. к.); в — гексагональная плотноупакованная (г. п. у.)
В гексагональной решетке (рис. 9, в) атомы расположены в углах и центре шестигранных оснований призмы и три атома в средней плоскости призмы. Эту упаковку атомов имеют следующие металлы: магний, цинк и др.
Некоторые металлы имеют тетрагональную решетку.
Размеры кристаллической решетки характеризуются величинами периодов, под которыми понимают расстояние между ближайшими параллельными атомными плоскостями, образующими элементарную ячейку (рис. 9). Период решетки измеряется в ангстремах (А).
Период решетки металлов находится в пределах от 1 до 7 А.
Источник: bstudy.net
Кристаллические решетки, их типы. Полиморфные превращения
Металлы имеют кристаллические решетки различных типов. Чаще всего встречаются: кубическая объемно-центрированная (ОЦК), кубическая гранецентрированная (ГЦК), гексагональная плотноупакованная (ГПУ) кристаллические решетки.
Показанные на рис. 1.4 наименьшие объемы кристаллов называются элементарными кристаллическими ячейками, с помощью которых представляют атомное строение металлов.
Самый простой способ понять ХИМИЮ — Типы Кристаллических Решеток и Свойства Вещества
В элементарной ячейке кубической объемно-центрированной решетки (рис. 1.4, а) содержится девять атомов: восемь располагаются по узлам ячейки и один атом — в центре. Такой тип решетки
имеют литий, калий, рубидий, ванадий, молибден, вольфрам, ниобий, тантал, a-железо и другие металлы.

Рис. 1.4. Элементарные кристаллические ячейки: а — кубическая объемно-центрированная; б—кубическая гранецентрированная; в — гексагональная плотноупакованная
В элементарной ячейке кубической гранецентрированной решетки (рис. 1.4,6) находится четырнадцать атомов, которые расположены в углах ячейки и в центре каждой грани. Этот тип решетки имеют свинец, никель, серебро, золото, медь, алюминий, платина, кальций, у-железо, церий, а-кальций и др.
В элементарной ячейке гексагональной плотноупакованной решетки (рис. 1.4, в) содержится семнадцать атомов, которые располо- жены в углах ячейки, центрах шестигранных оснований призмы, и три атома в средней плоскости призмы. Такую решетку имеют магний, цинк, кадмий, рений, бериллий, гафний, титан (а-фаза), осмий и др.
Размеры кристаллической решетки характеризуются расстоянием между центрами соседних атомов, находящихся в вершинах элементарных ячеек, называемым параметром или периодом решетки. Кубическую решетку характеризует один параметр — длина ребра куба а, а гексагональную — два параметра а и с или их отношение с/а.
Плотность различных кристаллических решеток разная и характеризуется координационным числом К, под которым понимают число атомов, находящихся на равном и наименьшем расстоянии отданного атома. Координационное число для кубической объемно-центрированной решетки равно восьми (A’S), и коэффициент заполнения (отношение объема, занятого атомами, к объему всей ячейки) равен 68%. Для гранецентрированной и гексагональной кристаллических решеток координационное число равно двенадцати (К2), а коэффициент заполнения — 74%.
Полиморфизмом или аллотропией называют способность металла в твердом состоянии при изменении температуры перестраивать свою кристаллическую решетку. Полиморфные превращения сопровождаются выделением или поглощением теплоты, а также изменением свойств металла. Различные аллотропические
состояния называют модификациями. Каждой модификации свойственно оставаться устойчивой лишь в пределах определенного для данного металла интервала температур. Аллотропические формы обозначаются греческими буквами а, р, у и т.д.
На кривых охлаждения и нагрева переход из одного состояния в другое характеризуется остановкой (для чистых металлов) или изменением характера кривой (для сплавов). При аллотропических превращениях, кроме изменения свойств (теплопроводности, электропроводности, механических, магнитных и др.), наблюдаются изменения объема металла и растворимости (например, углерода в железе). Аллотропические превращения свойственны многим металлам (железу, олову, титану и др.).

Рис. 1.5. График полиморфных превращений железа
Железо известно в двух полиморфных модификациях — а и у.
На рис. 1.5 приведена кривая охлаждения, характеризующая его аллотропические превращения. В интервале температур 911—1392 °С железо имеет кубическую гранецентрированную решетку g-железа (Fe ), а от 0 до 911 °С й от 1392 до 1539 °С — объемно- центрированную решетку а-железа (Fea). Выше 768 °С железо немагнитно, а ниже — обладает магнитными свойствами.
Источник: studref.com
НПП «ЭЛСИТ»
Главная  СПРАВОЧНИК
СПРАВОЧНИК  Термообработка
Термообработка  Строение металлов и сплавов. Основы теории термообработки
Строение металлов и сплавов. Основы теории термообработки
Строение металлов и сплавов. Основы теории термообработки
Чтобы понимать, как подобрать подходящее для той или иной операции высокотемпературной обработки оборудование? следует понимать базовые основы металловедения и теории термообработки. В данной статье мы расскажем о строении металлов и сплавов. Индукционный нагрев замечательно справляется со всеми видами высокотемпературной обработки, и, поняв строение металлов, Вы узнаете, почему токи высокой частоты отлично нагревают металл.
Строение металлов
В твердом состоянии любой металл обладает кристаллическим строением. Для этого вида строения характерна упорядоченность расположения ионов (атомов). Элементарные ячейки периодически повторяются в пространстве, образуя кристаллическую решетку. Внутри кристаллической решетки располагаются положительно заряженные ионы, или как их называют по-другому – атомные ядра.
Вокруг атомных ядер в постоянном движении находятся отрицательно заряженные частицы – электроны. Количество электронов, находящихся между ионами и определяет уровень теплопроводности металла.
Ионы (атомы) внутри кристаллической решетки находятся в непрерывном тепловом колебании. Если температура повышается, то амплитуда колебаний атомов резко возрастает, если температура понижается, то амплитуда замедляется. Плавка металла разрушает кристаллическую решетку, выпуская ионы в беспорядочное движение в пространстве.
Элементарная ячейка – это главный элемент кристаллической решетки. Увидеть ее вы можете на изображении 1. Изображена решетка в виде куба. Однако можно заметить, что каждый атом этой решетки одновременно принадлежит восьми соседним элементарным ячейкам.

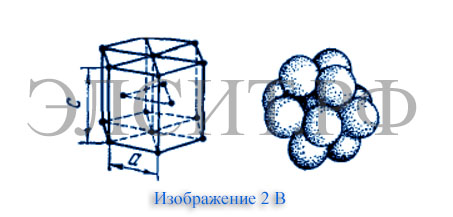
На изображении 2 вы можете увидеть наиболее распространенные типы кристаллических решеток.
а) Объемно-центрированная решетка. Как видно из рисунка восемь атомов данного типа решетки располагается в углах куба, а один находится в центре. Данная кристаллическая решетка свойственна следующим металлами – натрий, литий, свинец, вольфрам и т.п.

б) Гранецентрированная решетка. Внимательно рассмотрев ее изображение, вы заметите, что восемь атомов данного типа решетки расположено в уголках куба, а в центре каждой из шести граней размещается еще по одному атому. Свойственна гранецентрированная кубическая решетка следующим металлам: медь, серебро, алюминий, золото и т.п.

в) Гексагональная решетка имеет расположение атомов в углах и центре основания призмы. При этом три атома располагаются в средней плоскости призмы. Характерен данный вид кристаллической решетки следующим металлам: титан, магний, цинк, бериллий и другие металлы.
Индукционный нагрев способен проникать в кристаллические решетки металла, равномерно распределяя тепло и не нарушая их структуру. Автоматизированное программное обеспечение, которым снабжена каждая установка ЭЛСИТ позволяет контролировать процесс обработки, чтобы не нарушить структуру кристаллической решетки.
Дефекты кристаллической решетки
Ничто в нашем мире не идеально. Кристаллы металлов не обладают идеально правильным расположением атомов внутри кристаллической решетки. Практически всегда внутри кристаллов встречаются различные несовершенства (дефекты строения). В некоторой степени дефекты кристаллической решетки определяют физические и механические свойства металлов.
Дефекты строения кристаллической решетки можно подразделить на три вида: точечные, поверхностные и линейные.
Среди точечных дефектов наиболее распространенными являются – вакансии. На изображении 3 вы можете заметить вакансии. Вакансии представляет собой дефект кристалла с отсутствующим внутри кристаллической решетки атомом.
Еще одним точечным дефектом является дислоцированный атом. Дислоцированный атом – это дефект кристаллической решетки, при котором один из атомов выходит из равновесия. Вы можете наблюдать данный дефект на изображении 4.

Ни вакансии, ни дислоцированный атом не остаются без движения. Их непрерывное перемещение внутри кристаллической решетки называется диффундированием. Так как энергия между атомами распределяется неравномерно, вакансия может передвигаться внутри атома до тех пор, пока не выйдет из него на поверхность кристалла. Дислоцированные атомы и вакансии искажают кристаллическую решетку, по этой причине свойства кристалла могут меняться.
При проведении термообработки важно учитывать все эти факторы. Индукционный нагрев в некоторых случаях может помочь избавиться от дефекта кристаллической решетки, равномерно распределив тепло по всей поверхности кристалла.
Наиболее распространенными линейным дефектом кристаллической решетки является дислокация. Дислокация – это нарушение правильного кристаллического строения металла. На изображении пять вы можете разглядеть дислокацию атомов.
а) Дислокация расположена на левом краю кристалла.
б) Центральное расположение дислокации.
в) Дислокация расположена на правом краю кристалла.

Поверхностные дефекты появляются на границе зерен или субзерен, если атомы обладают не таким правильным расположением, как внутри зерна. Как правило, по границам зерен скапливаются дислокации и вакансии.
На изображении 6 вы можете разглядеть поверхностные дефекты кристаллической решетки, разделяющие зерно на блоки.

Сплавы металлов — структура
На сегодняшний день производители все чаще стали использовать при создании металлических изделий не чистые металлы, а сплавы. Сплавы металла – это вещества, которые образовались в результате затвердения расплава, состоящего из нескольких компонентов. Компонентами формирования сплавов служат только металлы или металлы с небольшим количеством примесей.
Металлические сплавы подразделяются на двойные, тройные и т.п. (по количеству входящих в них компонентов), а также на черные и цветные металлы (в зависимости от того, какой металл лежит в основе сплава).
Если строение металлов понять проще, то строение сплавов существенно отличается. Строение металлического сплава довольно сложное.
Существует несколько видов сплавов, в зависимости от характера взаимодействия его компонентов друг с другом.
- Химическое соединение – сплавы металлов, элементы которого могут вступать друг с другом в химическое взаимодействие, тем самым создавая новую кристаллическую решетку. Образовавшееся химическое соединение обладает уже совсем другими свойствами, чем компоненты, вошедшие в его состав.
- Механическая смесь – сплавы металла, компоненты которого не растворяются, находясь в твердом состоянии, а также не вступают друг с другом в химическое соединение. Как правило, механическая смесь не изменяет кристаллические решетки металлов, входящих в сплав.
- Твердый раствор – сплав, образовавшийся во время охлаждения жидкого раствора сплава, компоненты которого сохранили растворимость, а при кристаллизации смогли образовать единую кристаллическую решетку.
Твердые растворы также подразделяются на два главных типа: внедрения и замещения. Если посмотреть на изображение 7, то вы отметите на первой картинке, как атомы растворимого компонента начали замещать атомы растворителя. При этом никогда не ясно, в каком соотношении атомы заменят друг друга.
Однако важно отметить, что необходимо соблюдение двух главных условий, чтобы началась замена атомов. Первое – оба компонента должны иметь схожие кристаллические решетки. Второе – размеры атомов входящих в состав сплава компонентов должны различаться лишь незначительно (не более 8%).

Атомы, входящие в состав твердых растворов внедрения, значительно отличаются друг от друга по размерам. Справа на изображении 7 вы можете заметить, как атомы одного компонента внедряются в пустоты кристаллической решетки другого.
Во время формирования твердого раствора кристаллическая решетка искажается, а ее параметры меняются. В большинстве случаев атомы распределяются беспорядочно, однако бывают случаи, когда она размещаются внутри кристаллической решетки упорядоченно (при медленном охлаждении расплава меди и золота). Твердые растворы с равномерно распределенными атомами внутри кристаллической решетки называются сверхструктурными.
Индукционный нагрев одинаково хорошо справляется и с чистыми металлами и с их сплавами.
Источник: xn--h1afsf5c.xn--p1ai